Свойства природных газов и лёгких углеводородных жидкостей
ГЛАВА IV
СВОЙСТВА ПРИРОДНЫХ ГАЗОВ И ЛЁГКИХ УГЛЕВОДОРОДНЫХ ЖИДКОСТЕЙ
SO
98 99 99,5 99,8
95
Г
/
/
/
12 13У //«
¦ li ill in И Hi tii/li lilililii/ikiiiiili.iib
U.5 i К,9
ukidimlmilmJ
«0 50 60 70 80 90
Общее содержание, % пол
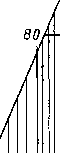
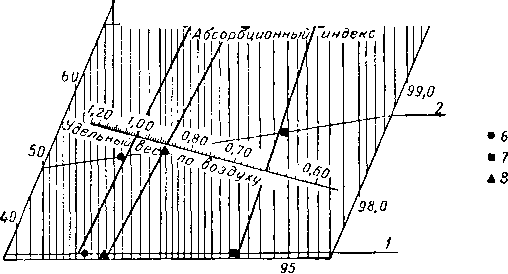
Рис. IV. 1. Линейная диаграмма для определения относительного удельного веса по составу природных газов [IV. 57].
1 — метан; 2 — этан: 3 — пропан; 4— бутаны; 5 — пентаны; 6 —<
проба 3; 7 — проба 4; 8 — проба 5-
Знание свойств и поведения природного газа, будь то чистый метан или смесь легких углеводородов (часто с добавками неуглеводородных газов — азота, углекислоты и сероводорода), позволяет более рационально решать вопросы его добычи, переработки н транспорта. Компоненты природного газа обычно находятся в газообразном состоянии, но иногда могут существовать как жидкости или твердые тела. Наиболее важным является вопрос о фазовом состоянии, в котором находятся компоненты природного газа. В этой главе будут рассмотрены следующие свойства природных газов и их компонентов;
коэффициент диффузии; коэффициент сжимаемости газов; плотность газов и жидкостей; поверхностное натяжение; термодинамические свойства:
а) теплоемкость,
б) скрытая теплота парообразования,
в) энтальпия смеси; теплотворная способность; пределы воспламеняемости; критические свойства; вязкость;
теплопроводность.
Состав природных газов некоторых месторождений приведен в табл. I. 5 и I. 8. Методы анализа газов приведены в главе VI в связи с рассмотрением равновесия системы жидкость — пар. В общем по своему составу природные газы сходны между собой. Для большинства газов концентрации компонентов изменяются в довольно узких пределах. Использование удельного веса газа в качестве характеризующего параметра зависит от того, насколько газы сходны по составу. Легатский, Тук и Гранди (Legatski, Tooke and Grundy) [VI. 57] дали диаграмму, на которой состав любого газа выражается прямой линией (рис. IV. I).
Физические свойства чистых углеводородов даны В табл. П. I (см. приложение).
§ 1. МОЛЕКУЛЯРНАЯ ТЕОРИЯ ГАЗОВ И ЖИДКОСТЕЙ
Свойства газов и жидкостей обусловлены природой молекул и сил межмолекулярного взаимодействия. Кинетическая теория газов, разработанная в XIX в. Джоулем, Клаузиусом, Больцманом и Максвеллом, трактует газовое состояние как «совокупность молекул, каждая из которых движется в произвольном направлении, при* чем движение одной молекулы совершенно не контролируется силами других молекул, несмотря на то, что как скорость, так и направление ее движения могут резко меняться всякий раз, когда она сталкивается с другой молекулой или ударяется о стенки сосуда» [IV. 45]. В первом приближении газ можно рассматривать как совокупность частиц, не имеющих объема и не взаимодействующих между собой. Поведение газов при низких давлениях согласуется с теорией, основанной на этих простых предположениях. Постепенно, по мере накопления данных о несоответствии между теорией и наблюдаемым поведением реальных газов, это предположение видоизменялось. При этом более точно учитывался объем молекул и сил межмолекулярного взаимодействия. Позднее современная механико-статистическая теория, развитая на основе квантовой теории молекул, установила связь между всей совокупностью свойств газов и сил межмолекулярного взаимодействия [IV. 41].
Чтобы связать количество одного вещества с количеством другого, в теории материи было использовано понятие моля. Масса одного атома кислорода была произвольно принята за 16 (моль кислорода Ог за 32), а относительная масса других элементов или молекул была определена как их атомные или молекулярные веса. Закон Авогардо устанавливает, что равные объемы различных газов при одинаковой температуре и одинаковом давлении содержат одинаковое число молекул. Это число равно 6,02ХЮ23 молекул в 1 г-моль вещества (32 г кислорода) при 0° С и атмосферном давлении (22 414 см3). I кг-моль кислорода весит 32 ООО г и состоит из 1000X6,02ХЮ23 = 6.02ХЮ26 молекул.
(IV. 2)
Существуют два обычно применяемых метода приведения уравнения состояния идеальных газов (IV. 1) к виду, удобному для определения pVT (соотношений реальных газов). Один из них состоит в том, что в уравнение состояния идеальных газов вводится коэффициент сжимаемости г:
PV=znRT.
Этот газовый закон является общим для любнх газов. Коэффициент сжимаемости является функцией температуры, давления и состава газа и выражается в зависимости от этих переменных графически или аналитически.
Метод определения коэффициента сжимаемости по графикам будет детально изложен в соответствующем разделе ‘. Необходимо отметить, что в технических расчетах используется обычно именно этот метод для определения коэффициента сжимаемости газа.
Другой метод реальных соотношений газов заключается в применении уравнения состояния, учитывающего собственный объем молекул и силы молекулярного взаимодействия. Такое уравнение состояния реальных газов впервые было дано Ван-дер-Ваальсом в виде
(IV. 3)
Р +
V*
(IV. 1)
RT Р ~ ]/ i
1 —
IT3
где р — давление; V — объем; п — число молей; R — газовая постоянная; Т—абсолютная температура. Значение газовой постоянной R при различных размерностях давления, температуры и объема приведено в табл. IV. 1. При давлении, близком к атмосферному, поведение газов подчиняется законам идеального газа, так что давление или объем системы могут быть подсчитаны по данным значениям температуры и массы. При этом относительная ошибка будет составлять не более 5%. В тех случаях, когда требуется более точный подсчет или если газ находится при высоком давлении, уравнение идеального газа неприменимо.
Таблица IV. I Константы газового закона pV = nRT
Значения R для различных размерностей
| Размерность давления р | Размерность температуры Т |
Размерность объема V | R для п = 1 МОЛЬ |
| am | °К (°С + 273,16) | Л | 0,082055 |
| psia | °R (°F + 460) | куб. футы |
10,73 |
| фунт/кв. фут | °R (°F + 460) |
куб. футы | 1545,0 |
R для воздуха, когда п = 1 фунту
фунт/кв. фут |°R (°F + 460) | куб. футы | 53,2
Используя данные по pVT-соотношению для индивидуальных углеводородов и для природных газов, можно определить их отклонение от законов идеального газа (библиография по этому вопросу дается в работах [IV. 61, IV. 80, I. 2, I. 9]).
1. УРАВНЕНИЕ СОСТОЯНИЯ
Газовый закон, связывающий давление, температуру и объем для газа, в котором не учитывают объем молекул и пренебрегают силами межмолекулярного взаимодействия, известен как уравнение состояния идеального или совершенного газа:
pV = nRT,
Это уравнение хорошо согласуется с экспериментальными данными для газов, плотность которых не превышает двух третей от плотности газа при критических условиях. В уравнении (IV. 4) а, Ь, с, А0 и В0 являются постоянными для данных компонентов природного газа (см. табл. IV. 2).
Бенедикт, Уебб и Рабин (Benedict, Webb and Rubin) [IV. 10] дали уравнение состояния легких углеводородов в виде
p = RTd+ (BoRT-^Ao — Щ d2 + {bRT — a) d^ +
ГИЗ js
+ aad° +~ [(I + yd2) ], (IV. 5)
где d — молярная плотность, а параметры A0, So, Co, a, Ь, с, а н 7 являются величинами, постоянными для индивидуальных веществ. Для смесей эти параметры являются функцией состава смеси. Значения этих параметров для различных индивидуальных углеводородов и
В этом уравнении Ь — собственный объем молекул газа; а — сила притяжения молекул. Значения констант а и Ь уравнения Ван-дер-Ваальса приведены в табл. IV. 2.
В свое время было предложено несколько видов ураЕ -нения состояния реальных газов, причем константы в этих уравнениях вычислялись на основании экспериментальных данных. Часто пользуются уравнением Битти — Бриджмена (Beattie—Bridgeman) [IV. 7. IV. 90].
1 См. раздел «Сжимаемость природного газа». — При».
V + Ba\\-v
¦ b) = RT.
-в
(IV. 4)
Vi
о
о
о
о
о
Коэффициенты для индивидуальных углеводородов Таблица IV.2
LO
00
CN О CN (N О тГ О ^
г- —
о
05
от
со —
| X | О |
|||||||
| «I | СО СМ О | ю |
ю | |||||
|
& | Ю СМ — о о о о | оо | г- | г— | 00 |
оо | ||
| 0) | ООТСОООСМООО | г- | тГ |
г- | Tf1 |
h- | ||
| с |
^ОЮСОСОСОЮОО | г- |
ю | тг |
ю | со | ||
| о | ОТСООТтГСОЮОТОСО | г- | см |
о | ю |
00 | от |
ю |
| СП |
O-NNON^ | ю |
со | ю |
оо | |||
| ci о’ N -н’ О СО О* -н |
со | о |
о | —Г |
см |
со О оо
оотгтгсмОгсмсо-
Г- СМ ОО ОТ СО 00 —«с О^-нОФОСО^О' оо сГ o' о о-^о-ю —
| о |
о | ю | |||||
| ст | от | от |
|||||
| ст | со | от |
со | от | |||
|
ст | ю | со |
см |
со | |||
| о | h- | от | С^5 |
оо | со | ¦^г | |
| от |
со | см | CU |
о | оо | ||
|
со | со | о |
о | —« | о | — |
<о
>»Х УС U О Ч п X X Ь*
см
СМ _ тГ СО Ю О Tt'Tt'^COCO—‘ООО ЮСООТтГСОООО ООГ'-СМОТСМГ'-СОтГО Г-СОСОтГ^СОООГ'-О q-(Mcoooiwq тр 00 о” о" О О —1* о —' СО ю —.
| см |
о | о |
о | о | ||
| Tt" |
от | |||||
| ю | см | от | от |
со | ||
|
00 | от |
h- | со |
00 | от | |
| 00 | 00 | со | 00 |
Tt" | со | |
| от | см |
тГ | ю |
см | Tt" |
|
| от | со | см | со |
о^ | оо | |
| со | о |
о | —- |
о | —Г |
—1 |
О тГ
— ю
СО СМ
см eg 00 00 СМ ОТ
о о'
г- —. Г- оо
СМ Г-
ю со О tF ю оо о о
см
<о
СМ
со см ю г-
тг —. Ю 00 со —
<М от
o' о
от
см
со со — ю 00 от со со.
(IV. 14)
Г- оо от Ю от со
ОТ Tf
— см со со
ю
00
.тГ (N N
о о о о о
О —
00 со оо ^
tF Г"» О СО СМ СО
о” о"
Г-- со — см тг ю со см
Г- СО
см ю
ООО
о..
о
о
о о
СО О —. см ю
СО ^ Ю
о.ово со о —*
о о
ООО
Г- 00 о Ю СО о
СМ СО тГ1
см о от OO't
СО Ю ’t О СО
О от О СО Ю СО
— со о о
ю СО от СО от
со —
~ о
<м _
........
< fe сз <о а г-
TF о О СМ (ММОГ^О) Г--СООТСМСОСОООО МЛЮ - - NCOO MMlOai-¦ Ю СМ СО О rfCOLOr^-—'ТРСО^ОО ОО-'-ОСООСЧ-н
О О т* о о o' o' o' —^ со
<о
ю О Ю О от (МЮОО — ОС^ООЮ О<М<М00Г'-0Т00-^ <М<ОСОГ-тГ<МтГООТ со—¦lOOlCOOrr^-—-ю О—•ОТСТОСОСМОТОТ
сбо ооо о —o' о см to
О О
со со о о о ю —•ЮЮООСГ-'-О С0СМСМЮГ--О—-О СМГ--СМ00СМГ--атГ--О СООТГ--ОСМтГСЧОО
оо оо ю о от —^сосм <td(ddddod(N
г- от СО тГ СМ Ю Ю —1 СО СОООООО — ОТО OCN—'Г^-ТГСОСОО Г'-ЮСМОТООГ'-СМЮОТ rt-oo—'СО—-h-OlOOl
СМ О СО О О О О cS
О тГ 3 1Л О — О ОООГ--ОТГ--О—-О ЮСПОЮ-н TtOcOO СМО“>СМТГЮСОГ'-ЮО -H-HlON-HfOTfjcoO
doV4'ddw^cn о — —
со —
—> Ю СО —* СО СО ОТ
00ЮСО—•Г'-Г'-ООтГ
§г--г--ототсосмооо
Г--СО—-О—*—•—'СО
—со —1 —00 Ю
'¦""''¦'ToJco
о
о
Ю от Tf ю о • Ю со о CM Tt" о о см о
О — СО
О О О О о о
.. - _ - . о
СО N W со Tt о --* со
г- - . г- а I о СО,
00
N О Ю 00 'f
00 1Л Ф О) со
N СО N -н СМ
Гч М -н оо
от, lO
о —« —• —• СМ
Ю
Г- со г-- от со
Г- <М Ю <0 тГ
Ю Г- Г-- оо от О от СО —' Г"4-тг гЛ от см —• o' —^ О —Г СМ
— со оо со оо со со —
Ю N (М СО СО
со — О ОТ О
см от Ю СО
со —• со от
со
см см со оо
(О СО N -Н
со о — со СО оо ю со ю —« со <о
Ss
я * ё У
•0-т ft § я
и &
Й-е ^ у
*=t ч
1) о
V
к13 х X ? *
• 5
о я —. а
‘ с
х 3 а о ч> >> S к
где х — моляр
Ao,i и т. д. — числовые значения констант соответствующих компонентов.
Если смесь углеводородов состоит из большого числа компонентов, то подсчитывать параметры смеси по приведенным выше формулам вследствие их громоздкости не является наилучшим методом.
Мартин и Хоу (Martin and Hou) [IV. 59] вывели сложное, но надежное уравнение состояния индивидуальных углезодородов. Это уравнение включает десять констант, числовые значения которых могут быть получены по критическим данным pVT и по наклону кривой упругости пара в критической точке.
Эти уравнения состояния позволяют экстраполировать данные, получаемые экспериментально, и предсказывать отклонение поведения этих газов от законов идеального газа. Эти уравнения являются математической основой для предсказания термодинамических свойств системы в виде pVT-соотношений.
Вывод уравнений состояния, основанный на механико-статистической теории [IV. 41, IV. 12], предполагает, что причиной отклонения реальных газов от законов идеального газа является наличие сил межмолекуляр-ного взаимодействия.
Уравнение состояния с вириальными коэффициентами
р— - = | ? _l R
RT г + v + у2 + y3
дает коэффициент сжимаемости в виде степенного ряда. В этом уравнении В, С и D называются соответственно двойным, тройным и четверным вириальными коэффициентами. Вириальные коэффициенты являются функцией только температуры и зависят главным образом от молекулярных взаимодействий, в которых одновременно участвуют соответственно две, три и четыре молекулы. Определять вириальные коэффициенты и коэффициенты сжимаемости можно более точно лишь для газов, состоящих из простых молекул, таких, как кислород и азот [IV'. 36]. На системы природных газов уравнение (IV. 14) пока не было распространено. Методы статистической механики могут быть с успехом использованы для определения таких свойств, как плотность, вязкость и теплопроводность.
2. СКОРОСТЬ ДВИЖЕНИЯ И ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
Молекулы индивидуальных газов имеют широкий предел скоростей и движутся ва всевозможных направлениях. Распределение молекул по скоростям их движения впервые было дано Максвеллом (Maxwell)) [IV. 45, IV. 89]. Качественно это распределение показано на рис, IV. 2.
|
В0 — ^ ¦*/ !’ |
(IV. 6) |
| Ао — Ki)2< | (IV. 7) |
| Co = (S^.)2, |
(IV. 8) |
| (IV. 9) | |
| «“(SV/-)’- |
(IV. 10) |
| (IV. 11) | |
|
“=(SWS)S- | (IV. 12) |
| 7 = (S^)2. |
(IV. 13) |
| доли компонентов в смеси, | з Во,»» |
некоторых других газов приведены в табл. IV. 2. Для определения численных значений этих параметров для смеси углеводородов пользуются следующими формулами:
| л |
V | ||||||||||||
| / |
Л | ||||||||||||
| / | \\ | ||||||||||||
| V |
|||||||||||||
| ‘ / / | 1 |
\ | \ |
||||||||||
| d € | /о | ?. | V |
||||||||||
| ? | 3 | \ |
|||||||||||
| // | \ |
\ | |||||||||||
| // If | \ | ||||||||||||
| i | f |
4 S | |||||||||||
| / | 4 X |
— |
200
Скориста молекул, м/сек
0,22 ы 0,20 2 0,18 ll 0,16 0,1 и
5 °
“5 §- 0,12
с^-о 0,10 0,08
‘n *
3 ? 0,06 *<§
^ 0.0U
^ 0,02 U
Рис. IV. 2. Распределение молекул по скоростям [IV. 89].
1 — наиболее вероятная скорость; 2 — средняя скорость; 3 — среднеквадратичная скорость.
В зависимости от концентрации или плотности газа его молекулы будут проходить большее или меньшее расстояние, прежде чем они столкнутся с другими молекулами. Поскольку известно распределение молекул по скоростям, известно и соотношение между числом молекул и расстоянием, пройденным с данной скоростью. Среднее расстояние, которое проходит молекула между двумя столкновениями, называется средней длиной свободного пробега молекул.
Чапмен и Каулинг (Chapman and Couling) [IV. 24] дали следующую формулу для средней длины свободного пробега молекул;
для слу-
X =-J—= = , (IV. 15)
N Tta2/2 AV
где X — средняя длина свободного пробега молекул в см; N — число молекул в 1 см3; а — диаметр молекулы в см. При выводе этой формулы предполагалось, что молекула представляет собой гладкий упругий шар.
Диаметр молекулы водорода, найденный Чапменом и Каулингом, равен 2,73ХЮ-8 см. Так как при нормальных условиях (температуре 0°С и давлении 1 ат) в одном моле газа содержится 6,02ХЮ23 молекул, а объем одного моля равен 22,414 см3, то в 1 см3 число молекул составит 2.68Х1019. Поэтому средняя длина свободного пробега молекул при давлении 1 ат
X =- °’225
-- = 1,12 х Ю~5 см-
2,68 X 1019 X 2,73 х 10~1Ь
(IV. 16)
Для водорода в 1 см3 при нормальных условиях (0° С и 1 ат) общее число столкновений в секунду составляет 2,05ХЮ29, а частота столкновения одной молекулы 1,5Х 1010 в 1 сек. Время между столкновениями равно, 6,6X10-4 сек [IV. 24]. Средняя длина свободного пробега молекул не зависит ни от массы молекулы, ни от температуры, если температура не влияет на диаметр молекулы. Так, средняя длина свободного пробега молекул для всех газов при атмосферном давлении составляет порядка 10-5см, что в 200—400 раз больше диаметра молекул (см. табл. IV. 3). Этот факт является обоснованием хаотического движения молекул при выводе формулы (IV. 16). Средняя длина свободного пробега молекул зависит от числа молекул в данном объеме и для идеальных газов является обратно пропорциональной давлению. При давлении 100 ат средняя длина свободного пробега молекул, рассчитанная по формуле (IV. 15), становится соизмеримой с диаметром молекул. Следовательно, эта формула справедлива только при малых значениях давления. При давлении 0,01 мм рт. ст. средняя длина свободного пробега молекул достигает 1 см.
Таблица IV. 3
Значения диаметров и средних длин свободного пробега молекул
| Вещество | Диаметр ст, А* | Средняя длина свободного пробега X, см X 10® | |
|
вычисленная** при нормальных условиях (0° С и I атм) | нз дан ных тече ния газа | ||
| 3,35—3,88 |
0,75—0,56 | 0,64 |
|
| 3,54—3,81 |
0,67—0,58 | 0,40 | |
| Пропан........ |
4,21—4,42 | 0,473—0,430 |
0,28 |
|
н-Бутан........ | 4,5—4,82 | 0,415—0,362 | |
| Этилен ........ |
3,70—3,35 | 0,614—0,749 |
|
| Пропилен....... |
4.02—4,32 | 0,52—0,45 | |
| Водород ........ | 2,57—2,73 |
1,27—1,125 | 1,45 |
| 3,36—3,68 |
0,74—0,62 | 0,83 | |
| 1,90 | 2,33 | 2,33 | |
|
Углекислый газ .... |
3,996 | 0,53 |
0,53 |
1 ангстрем (А) =10 ° см.
0,225 0,225 х 10“
= 8,4 X 10-
N о2 2.68 х 101* х t>2 чая. когда X выражается в см, а а в ангстремах (см х 10 ®).
Молекулы углеводородов сложнее молекул водорода, и поэтому их диаметр точно не известен. Разные методы измерения диаметра молекул углеводородных газов дают различные значения. В табл. IV. 3 значения вычисленных средних длин свободного пробега молекул рассчитаны по приведенным в этой таблице значениям диаметров молекул. Средняя длина свободного пробега молекул при давлении, отличном от атмосферного, может быть найдена путем деления средней длины свободного пробега молекул при атмосферном давлении на абсолютное давление, выраженное в атмосферах.
На рис. II. 16 приведены значения проницаемости пористой среды для различных газов. Опыты, на основании которых построен этот график, более отчетливо показывают соотношение длин свободного цробега молекул различных газов, чем данные, приведенные в табл. IV. 3. Подсчитывая А0 в уравнении (II. 7) для различных газов, взятых из рис. II. 16, можно выразить длины свободного пробега молекул с помощью следующего соотношения:
Ьг X,
(IV. 17)
Значения длин свободного пробега молекул, определяемые на основании данных по течению газа (см. табл. IV. 3), рассчитывались по формуле (IV. 17). При этом значение X для гелия принималось как стандартное. В табл. IV. 3 показано удовлетворительное соотношение между вычисленными значениями X и значениями, полученными из опытов по течению газа.
Если два индивидуальных газа привести в соприкосновение, то молекулы одного газа будут проникать в область, занятую другим газом, и наоборот. Этот процесс, посредством которого газовая среда становится однородной по составу, называется диффузией.
Процессы диффузии имеют большое значение в некоторых областях газовой промышленности. Процесс диффузии, например, определяет время, необходимое для полного смешения двух газов в лабораторных уста* повках высокого давления. Если в пористой среде происходит вытеснение одного газа другим, то молекулярная диффузия вызывает смешение этих газов на границе их раздела. Если газ движется через пористую среду, поверхность которой смочена жидкостью, достижение равновесия между газовой и жидкой фазами зависит от процессов диффузии.
0,0043 Т3/г
D = •
№
Коэффициент диффузии может быть установлен по поведению молекул [IV. 5, IV. 24, IV. 39]. Пиллиленд дает выражение для коэффициента диффузии при атмосферном давлении в следующем виде:
\Ма Мв)
(IV. 20)
где Т—абсолютная температура в °К (273+°С); Мл и Мв — молекулярные веса газов А и В; VA и VB — молярные объемы газов в точке кипения при нормальном давлении в см3/моль; Р—общее давление в ат; D—коэффициент диффузии газа в см21сек.
Коэффициент диффузии обратно пропорционален давлению, т. е. произведение коэффициента диффузии на плотность дает постоянную величину. Значение
| 1 |
-1- | 2 |
Рис. IV. 3. Схема прибора для исследования процесса диффузии.
Коэффициенты диффузии могут быть определены на приборе, схематически изображенном на рис. IV. 3. Сосуд 1 заполнен чистым водородом, а сосуд 2 смесью водорода с углекислым газом. Молекулы углекислого газа будут стремиться перейти в сосуд 1 по трубке, соединяющей эти сосуды. Если размеры сосудов значительно больше размера соединяющей их трубки, непрерывно перемешивается содержимое сосудов для поддержания однородного состава газа на разных концах трубки, то процесс диффузии углекислого газа будет установившимся. Такой процесс диффузии описывается следующим уравнением (закон Фика):
dn
(IV. 18)
dt dx
где n — число молекул диффундирующего компонента; t — время; А — площадь; с—концентрация диффундирующего компонента; х — расстояние, на которое происходит диффузия; D — коэффициент диффузии.
Пример. Коэффициент диффузии С14Ог в водороде при 100° С равен 0,341 см2/сек [IV. 25]. Определить скорость диффузии при 100° С через трубку с поперечными размерами 2x2 мм и длиной 2 см, если в сосуде 1 концентрация С14Ог в водороде составляет 0,1% мол., а в сосуде 2 концентрация Си02 в водороде равна 1,0%;
dx-^’........—' - 1
2>0
cm2/cmJ
X
dt
0,009 х 273
моль/см3 = 2,0 X 10 10 моль/сек.
X
22414х 373
Если диффузия происходит с большой скоростью, процесс может быть неустановившимся, так как концентрация диффундирующих молекул на разных концах трубки непрерывно изменяется. Тогда применяется второй закон Фика для неустановившегося процесса диффузии:
dn t?2c dt~ дх*'
(IV. 19)
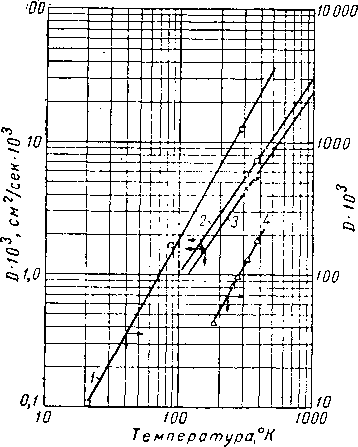
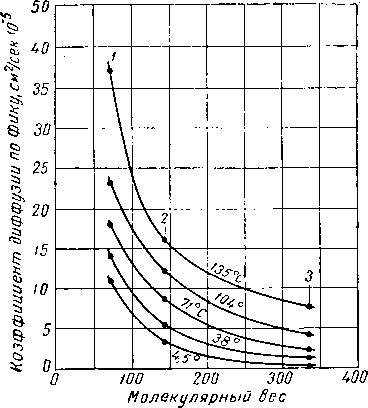
Рис. IV. 4. Влияние температуры на коэффициент диффузии при атмосферном давлении.
/ — самодиффузия Н2; 2—С,403 в СО г +
+Н2; 3 — С,4Оа в С02 + СзНв; 4 — самодиф
фузия СО*
показателя степени абсолютной температуры в уравнении (IV. 20) зависит от типа молекулы. Для упругих молекул сферической формы показатель степени равен 3/2.
Чоу и Мартин (Chou and Martin) [IV. 25] изучали диффузию углекислого газа, содержащего С14, в смесях СОг — Нг и СОг — СзНз. Результаты этих исследований при р=1 ат, представленные на рис. IV. 4 в ви-дг зависимости коэффициента диффузии от температуры, показывают, что эта зависимость такая же, как и самодиффузия водорода [IV. 39]. В табл. IV. 4 даны значения коэффициентов диффузии для некоторых газов при атмосферном давлении.
Данные Чоу и Мартина, представленные на рис. IV. 5, подтверждают, что произведение коэффициента диффузии на плотность есть величина практически постоянная. Результаты исследования этих же авторов, приведенные на рис. IV. 6, иллюстрируют влияние состава бинарной системы на коэффициент диффузии. Из других работ в этой области следует отметить работу Джефриса и Дрикамера (Jeffries and Drickamer) [IV. 46| для системы метан — ТСН3 (место одного атома водо-
Значения коэффициентов диффузии газов при атмосферном давлении
|
Система | т, °с |
D* по Фику, смг/сек |
| Водород в воздухе ...... | 25 | 0,410 |
| Водород в водороде ...... | 0 | 1,29 |
| С02 в воздухе....... . | 25 | 0,164 |
| С02 в метане ........ | 0 | 0,147 |
| Метан в воздухе....... |
0 | 0,196 |
| Водород в С02........ |
0 | 0,53 |
| Водород в метане ...... |
0 | 0,63 |
|
Водород в этане ....... |
0 | 0,46 |
|
Октан в воздухе....... |
25 | 0,060 |
| Бензол в воздухе...... |
25 | 0,088 |
| С»Ю2 в С1202+С3Н8: Мольные % C3HS: 20,3 .... |
100 | 0,0054 |
| 44,1 .... | 100 |
0,0051 |
| 77 .... | 100 |
0,0047 |
|
С1403 в С1202+Н2: Мольные % Н2: 21...... | 100 |
0,0073 |
|
56,8..... | 100 |
0,0113 |
| 73,4..... | 100 | 0,0144 |
| 93,6..... | 100 | 0,0244 |
|
Метан в метане....... |
19 | 0,214 |
• Данные взяты из [IV.5, IV.25, IV. 121 а].
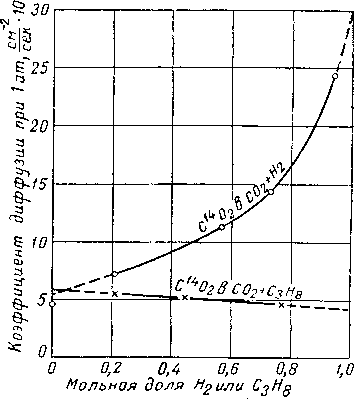
Рис. IV. 6. Влияние концентрации коэффициент диффузии [IV. 25].
too
30
е>
? ^ о
5 о
!?
<ь
”?^10 2 е-
^60
CN
I,
• о
300
с§"
100 200 Ц-а.вление, ат
|
пХ»2 |
<© I СГ) сЛ п 1 |
хНг- 0,936 | |||||||
|
Хн-> | = 0,73 U |
ОСн^" |
-0.73U | ||||||
| Хц7-0,568 |
-Г Хц2-0,5Б8 |
||||||||
| С | J | ” 1 |
||||||||
|
хн? = 0,2Ю |
О | Хн^-0,210 | |||||||
0 2 4 6 8 0
Мольная плотность, моль/л
| О | О ^У. N | ||||
| •Л N |
\^ | •ч |
|||
|
7 | к \ |
||||
| О 50°с *25°С л 0°С |
\ | \ | |||
Рис. IV. 7. Диффузия в системе СН4 ¦ ТСНз [IV. 46].
0 100 200 Давление, am
Рис IV. 5. Коэффициент диффузии С|402 в системе С1202 + Н2 при температуре 100° С [IV. 25].
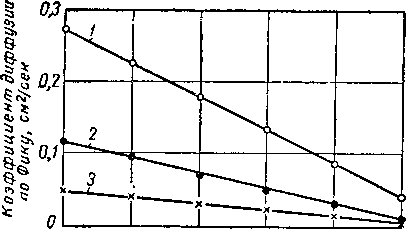
Рис. IV. 8. Коэффициент диффузии в системе метан — я-гексан [IV. 22].
/ — метан при 21° С и I ат\ 2 — метан при 21° С и 2,8 ат; з — гексан при 21° С и I ат.
0 0,20 ОАО 0,60 0,80 1,00
ВесоВпя'доля гексана
|
0 1 | 1,0 | |
0 | | 1,0 | 1 | |
1,0 | | 0 | | |
| Давление 1,03 ат | ||||||
|
0,0417 | 0,2725 |
0,0572 | 0,3571 | |||
| 0,0476 |
0,0072 | 0,0633 |
0,0101 | |||
| 0,0320 | 0,1100 |
0,0430 | 0,1402 | |||
| 0,0361 |
0,0105 | 0,0467 |
0,0143 | |||
| 0,0162 | 0,0369 |
0,0271 | 0,0594 |
|||
| 0,0180 | 0,0079 | 0,0293 | 0,0134 | |||
Давление 4,2 ат
| 0,0044 |
0,0885 | 0,0090 |
0,1070 | 0,0177 |
0,1457 | 0,0258 |
0,1800 |
| 0,0106 |
0,0006 | 0,0153 |
0,0013 | 0,0235 |
0,0029 | 0,0308 |
0,0045 |
| 0,0027 |
0,0271 | 0,0055 |
0,0330 | 0,0090 |
0,0454 | 0,0163 |
0,0579 |
| 0,0062 |
0.0007 | 0,0090 |
0,0015 | 0,0140 |
0,0028 | 0,0188 |
0,0053 |
| 0,001-1 |
0,0083 | 0,0034 |
0,0128 | 0,0078 |
0,0207 | 0,0126 |
0,0288 |
| 0,0029 |
0,0005 | 0,0053 |
0,0014 | 0,0096 |
0,0036 | 0,0288 |
0,0126 |
1,0
Метан в я-гексане я-Гексан в метане Этан в я-гексане . я-Гексан в этане . Пропан в я-гексане я-Гексан в пропане
Метан в я-гексане я-Гексан в метане Этан в я-гексане . я-Гексан в этане . . Пропан в я-гексане я-Гексан в пропане
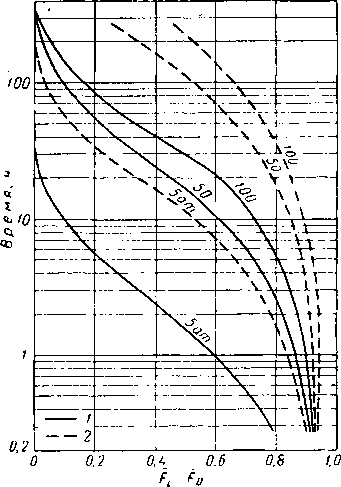
Рис. IV. 9. Смешение газов в цилиндрических сосудах посредством диффузии [IV. 84].
/ — гелий — метан (D0 = 0,564); 2 — бутаи — воздух (D0 *= 0,081)
кулами больших размеров требуется продолжительное виемя, если две части сосуда были заполнены первоначально разными газами. В действительности при достижении гомогенности при нагнетании одного компонента в сосуд, занятый другим компонентом, смешение будет происходить быстрее, чем также будет способствовать наличие естественных конвекционных потоков. Тем не менее для ускорения смешения газов, нагнетаемых в сосуд.
особенно при работе с высокими давлениями, желательно интенсифицировать перемешивание, напрнмер, путем нагревания нижней части сосуда.
Вопрос о диффузии в пористых материалах возник в связи с явлением проскальзывания *. В порястых средах диффузия меньше, чем в открытом пространстве, из-за сопротивлений, вызываемых разветвленной сетью каналов. О’Герн (O’Hern) [IV. 62] на основании опытов но диффузии углекислого газа через пористый образец, полученный спеканием металлического порошка (пористость 0,398), вычислил коэффициент, учитывающий диффузию в пористой среде (отношение коэффициента диффузии в свободном пространстве к коэффициенту диффузии в пористой среде7). Этот коэффициент для данного образца высокой проницаемости при атмосферном давлении оказался равным 3,94. Процесс диффузии в пористой среде тесно связан с такими параметрами, как средняя длина свободного пробега молекул и размеры пор пористой среды. Поэтому следует ожидать, что с ростом давления коэффициент, учитывающий особенности диффузии в пористой среде, будет уменьшаться.
6. КОЭФФИЦИЕНТ ДИФФУЗИИ ГАЗА
Уайлк (Wilke) [IV. 95] связывает коэффициенты диффузии для газа в жидкостях с комплексом
Т
— = °К • сек!см2 • спз
как функцию молярного объема с коэффициентом растворения в качестве параметра.
Коэффициент диффузии газа для жидкостей в 108—109 раз меньше коэффициентов диффузии для газов при
1 ат. Существующее правило, что произведение коэффициента диффузии на плотность фазы есть величина практически постоянная, может быть грубо приемлемым при переходе от газообразных систем к жидким. Например, для водорода при 25° С и 1 ат
1 4 X 2 х 273 D? = 22400 X 298 = 0>000012 г/см-сек,
а для водорода в воде при 25° С, Dp = 0,0000099.
Величина коэффициента диффузии для ряда органических веществ в бензоле и в метиловом спиръе при 15° С колеблется в пределах от 0,78 X Ю-5 до 2,64 X 10~5 см2 j сек.
Таблица IV .6
Значения коэффициентов диффузии метана в жидких углеводородах*
| Жидкий углеводород |
Тем пера тура, °С | Молярная доля метана в жидкости | Увеличение объема жидкости , % | Коэффициент диффузии, см10/сек х Ю5 |
|
Изопентан ........ | 30 | 0,1068 | 6,15 |
13,3 |
|
я-Пентан......... | 30 |
0,1016 | 5,43 |
13,2 |
|
я-Гексан......... | 30 |
0,1098 | 4,45 |
10,2 |
|
Циклогексан....... | 30 | 0,0638 | 3,14 |
4,7 |
| я-Гептан ......... | 30 | 0 0960 | 3,74 |
8,36 |
| 30 | 0,0403 | 2,26 |
5,47 | |
| Керосин ......... | 30 |
0,0956 | 2,15 |
3,33 |
| Нефти: | 60 | 0,0760 |
1,91 | 5,38 |
| Бартлесвиллская..... |
30 | 0,0895 |
1,6 | 1,71 |
| Сугерландская ...... |
30 | 0,0856 |
1,5 | 1,11 |
| Смаковерская....... |
30 | 0,0886 |
1,2 | 0,71 |
| Бредфордская....... |
60 | 0,0777 |
1,68 | 4,83 |
| 30 | 0,0883 | 2,11 | 3,03 |
* По данным Хилла и Леси (Hill and Lacey) [IV. 38].
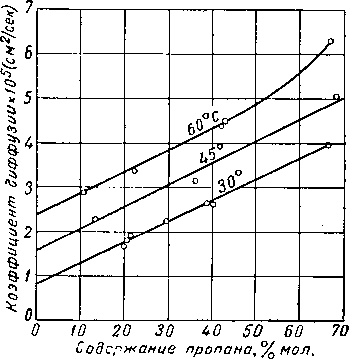
Рис. IV. 10. Коэффициенты диффузии процана в керосине [IV. 38].
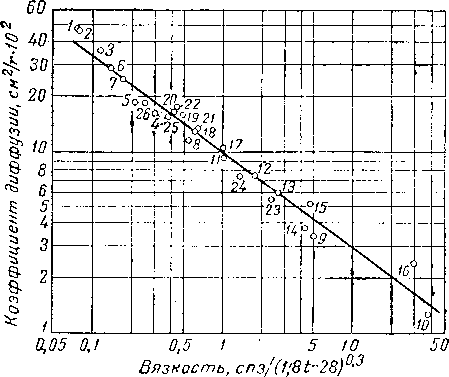
Рис. IV. 11. Соотношение между коэффициентом диффузии метана, вязкостью жидкости и температурой [IV. 38].
Леси (Lacey) с соавторами [IV. 38. IV. 69] измеряли коэффициенты диффузии метана и пропана в жидких углеводородах. На рис. IV. 10 представлены коэффициенты диффузии пропана в керосине, а в табл. IV. 6 приведены значения коэффициентов диффузии метана в различных жидкостях.
На рис. IV. 11 представлена зависимость коэффициента диффузии метана от отношения вязкости жидкости к величине (1,8/ — 28)0'3, где t — температура в °С.
Седж (Sage) с соавторами [IV. 74] изучали коэффициенты диффузии в системах метан — декан, метан — пентан и метан — белая нефть в широких пределах изменения температуры, давления и концентраций метана (рис. IV. 12).
Рис. IV. 12. Влияние молекулярного веса менее летучего компонента на коэффициент диффузии метана в жидкой фазе при 70 ат [IV. 74].
/ — метан •—» н-пентан; 2 — метан — н-декан; 3 «—• метан —?
светлая нефть.
Исследования pVT— соотношения газов при давлениях выше 200 ат были начаты Андрыосом и Амагатом (Andreus and Amagat) еще в 1870 г. [1.9]. Сидней Юнг (Sidney Young) [IV. 97] провел исследование по определению удельных объемов насыщенных паров 30 чи-
стых веществ для определения изменения отношения —j-
Работа Амагата для этилена [IV. 4], опубликованная в 1892 г., и работа Юнга для изопентана [IV. 75] дали ценные сведения о сжимаемости углеводородных газов.
Барелл и Робертсон (Burell and Robertson) в 1916 г. исследовали сжимаемость природных газов при невысоких давлениях [IV. 18]. Работы Коупа, Лйиса и Вебера (Соре, Lewis and Weber) [IV. 28] и Брауна, Саудер-са и Смита [IV. 15], проведенные около 1930 г., вызвали повышенный интерес к вопросу сжимаемости газов. В этом же году Бервалд и Джонсон (Berwald and Johnson) [IV. 11] установили отклонение поведения природного газа от закона Бойля, а Седж и Леси исследовали объемное поведение индивидуальных углеводородов [I. 16, 1.17, IV. 76] и их смесей, в частности метана и этана [IV. 77], при температурах от 21 до 237° С и при давлении до 700 ат. Отклонения поведения природных газов от законов идеальных газов, установленные на основании исследований, проведенных Холкомбом, Стен-дингом и Катцем (Holcomb, Standing and Kazt), [IV. 14, IV. 60, IV. 87], были приняты в качестве временного стандарта американской ассоциации природного газолина [IV. 60].
Седж и Леси (Sage, Lacey) и другие [I. 16, I. 17, IV. 76] исследовали поведение углеводородных газов на основании данных остаточных парциальных объемов.
1. ТЕОРЕМА СООТВЕТСТВЕННЫХ СОСТОЯНИИ
Теорема соответственных состояний, предложенная Ван-дер-Ваальсом, является частью его теоретических обработок состояний газов и жидкостей, начатая с момента опубликования его тезисов в 1873 г. Теорема эта гласит, что два вещества при соответствующих условиях будут иметь подобные свойства в зависимости от некоторых основных свойств, таких, как критическое давление и критическая температура. Например, при температуре, равной удвоенной критической температуре,
и при давлении, в четыре раза превышающем критическое, метан и этан будут иметь одно и то же значение коэффициента z, учитывающего отклонение от законов идеального газа. Такое сравнение приведено в табл. IV. 7, из которой видно, что различие в сжимаемости составляет всего 0,3%. Отношение температуры к критической температуре (в данном случае равное 2:1) называется приведенной температурой Тт. Точно так же отношение давления к критическому давлению называется приведенным давлением рт. Таким образом, теорема соответственных состояний устанавливает, что при одинаковых приведенных давлениях и температурах различные углеводороды будут иметь одинаковые коэффициенты сжимаемости.
Таблица IV.7 Соответственные состояния метана и этана
|
Наименование | Метан |
Этан |
|
Критическая температура, °К . . . . | 191,0 | 305,4 |
| Удвоенная критическая температу | ||
|
ра, °С .............. | 382,0 | 610,2 |
|
Критическое давление, am..... | 47,14 | 49,5 |
| Учетверенное критическое давление, | 188,5 |
|
| am............... |
198,3 | |
|
Коэффициент сжимаемости при |
||
| удвоенной критической температуре | ||
| и учетверенном критическом дав- |
0,959 | |
|
0,962 |
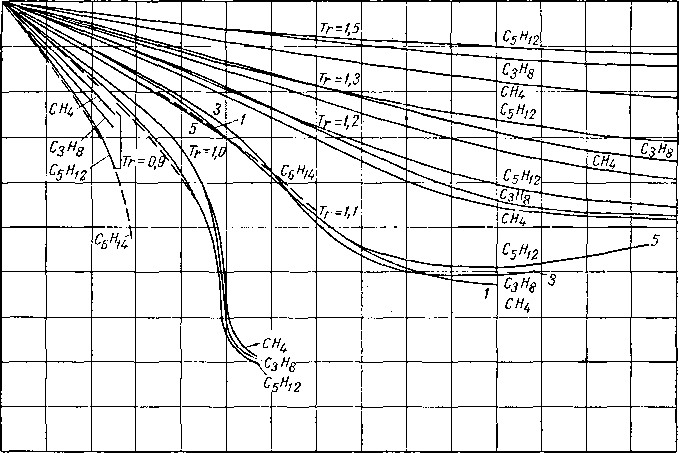
На рис. IV. 13 сравниваются коэффициенты сжимаемости для легких углеводородов парафинового ряда. Хотя в общем для индивидуальных компонентов кривые располагаются близко к друг другу, расхождения между ними выше тех, которые могли быть результатом экспериментальных ошибок.
Для вычисления фазового состояния индивидуального вещества с высокой степенью точности следует пользоваться надежными экспериментальными данными или более точными соотношениями.
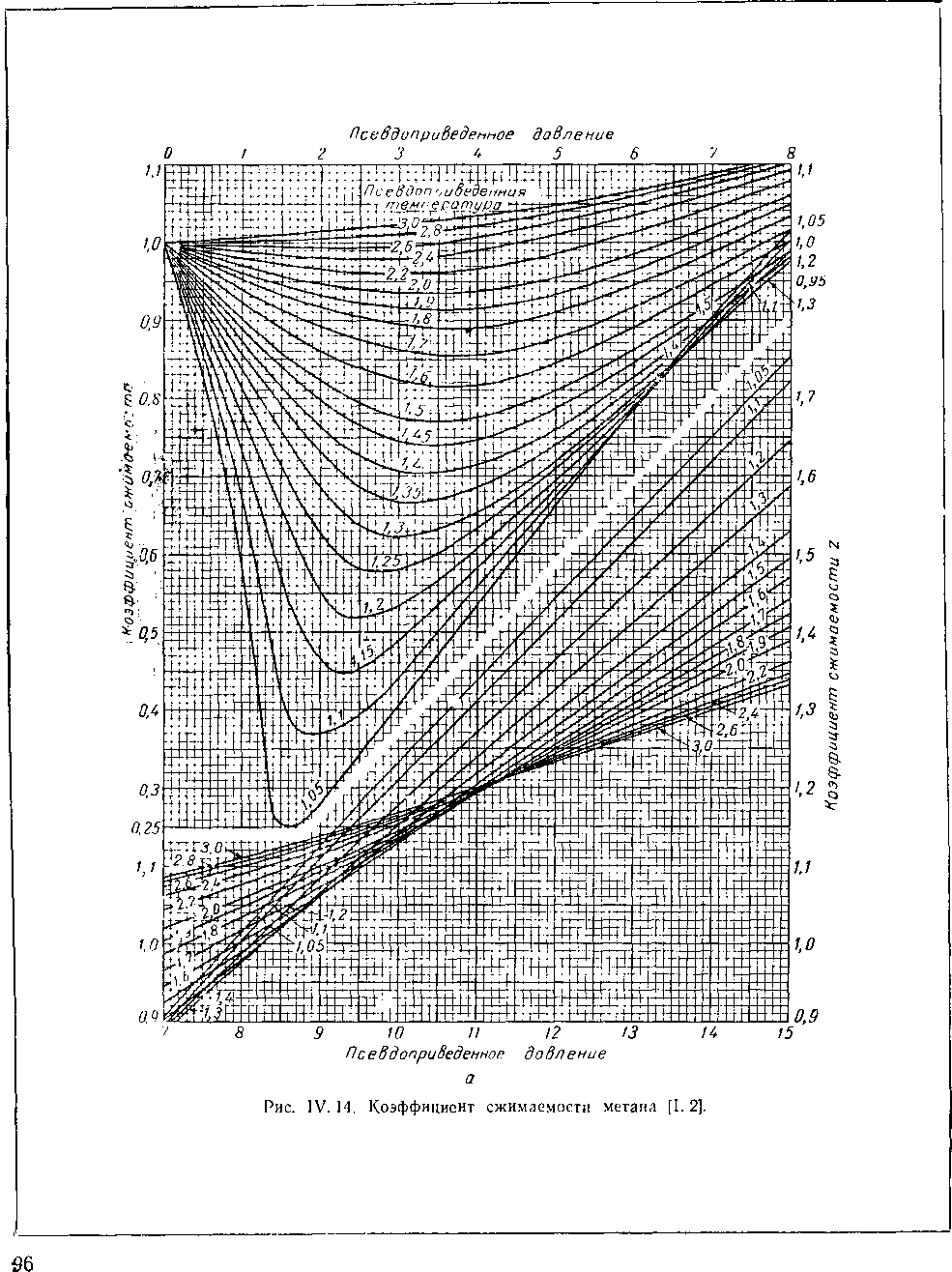
На рис. IV. 14 представлены коэффициенты сжимаемости для метана [I. 2].
0,9
ii
N 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 О
Коэффициент сжимаемости
О 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8 2,0 2,2 2,4 2,6 2,8 3,0
Приведенное давление Рг
Рис, IV. 13. Отклонение индивидуальных углеводородов от законов идеального газя.
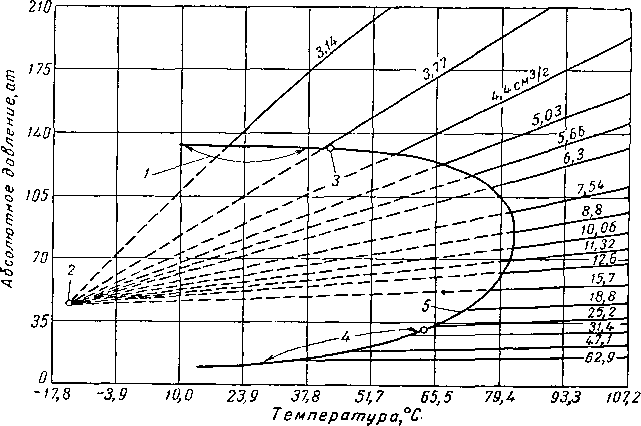
Рис. IV. 15. Диаграмма давление — температура, иллюстрирующая положение псевдокритической точки для системы СН4 — С4Н,0 при содержании 40% вес. метана [III. 62, III. 63].
/ — кривая точек кипения; 2— псевдокритическая точка; 3—критическая точка'
4 — кривая точек росы; 5— 70% мол. С\1, в системе СН4 —н.НчН,0.
Природные газы в основном состоят из метана с различными количествами этана, пропана, бутанов и т. д. Работа Кея (Kay) [IV. 54] дает возможность применить для смесей газов теорему соответственных состояний. Он предложил вместо критических давлений и температур, применяющихся для индивидуальных компонентов, использовать среднемольные критические давления и температуры для смесей газов. Эти среднемольные свойства называются псевдокритическими давлениями и псевдо-критическими температурами смесейЭти давления и температуры подобно точным критическим могут применяться для сравнения соответственных состояний, Псев-докритическая точка не имеет физического смысла, а является лишь приближенной точкой, в которой сходятся изохоры на диаграмме давление — температура. Важным является то обстоятельство, что эти изохоры прямолинейны. Рис. IV, 15 иллюстрирует справедливость этого положения для смеси, состоящей из 70% метана и 30% мол, бутана. На графике рис. IV. 15 показано также положение истинной критической точки смеси.
Сравнение коэффициентов сжимаемости метана, полученных по приведенным давлению и температуре, с коэффициентами сжимаемости природных газов и смеси метана с этаном [IV. 77] показывает, что кривые для метана более соответствуют кривым для природных газов.
Таблица IV.8
Расчет плотности природного газа по его составу,
представленному в таблице, при давлении 70 ат и температуре 32° С
| Компонент | Расчет nceBflonpHTH4ecKof | ТОЧКИ | |||||
|
моль ная доля У |
молекулярный вес |
Моли 1 |
Критическая температура |
Критическое давление, am | |||
| и Ы | О К | Ci |
Ci Cl | ||||
|
Углекислый газ . |
0,0040 | 44 |
0,17 | 305,4 |
1,2 | 75,2 |
0,30 |
| Метан...... | 0,9432 | 16 |
15,09 | 190,5 |
179,2 | 47,1 |
44,42 |
| Этан ....... | 0,0390 | 30 |
1,17 | 305 |
11,9 | 49,5 |
1,93 |
| Пропан..... | 0,0117 | 44 |
0,51 | 370 |
4,3 | 43,2 |
0,51 |
| Изобутан .... | 0,0008 |
58 | 0,04 |
408 | 0,4 |
36,9 | 0,03 |
| к-Бутан..... | 0,0013 | 58 | 0,07 |
425 | 0,6 |
38,6 | 0,05 |
| 1,0000 |
17,05 | 197,6 |
47,24 |
||||
Приведенное давление р, = — = тгггг = М8-
* п. 41 'Л4
Приведенная температура
Тг =. =. 11-^-~Ь-у
= 1,54
Удельный вес газа по, воздуху = 17,05/29,0 = 0,588.
Из рис. IV. 16 при Рг = 1,48 и Тг = 1,54 находим г = 0,872-
Коэффициент сжимаемости г> определенный при этих условиях Стивенсом и Фридманом (Stevens and Freidraan) [IV.601 равеи 0,875.
Плотность природного газа
1 Р 70 15 17,05 1 __
V ~ ZnRT = 1,033 0,872 0.082055 (273 + 32) ’ ''
Диаграмма, изображенная на рис. IV. 16, а была получена на основании данных на 1941 г. [IV. 87] для смесей газов при давлении до 700 ат. Сравнение этой диаграммы с более поздними [IV. 60] показало, что отклонение не превышает ±1,2%. Методика расчета плотности природного газа по коэффициенту сжимаемости, найденному из диаграммы (рис, IV. 16) для природного газа данного состава, иллюстрируется табл. IV. 8.
На рис, IV. 16 приведены результаты опытов по изучению коэффициента сжимаемости метана, проведенные Квалнесом и Гедди (Kvalnes and Gaddy) [IV. 53] при давлении от 700 до 1400 ат. Для удобства в табл. IV. 9 приведены значения критических давлений и температур некоторых компонентов природного газа.
Диаграмма на рис. IV. 17 [IV. 83а] позволяет судить об отклонении состояния природного газа от законов идеального газа при давлении, близком к атмосферному. Из этой диаграммы видно, что отклонение даже при таких малых значениях давления существенное. Для очень точных исследований состояния индивидуальных газов могут быть использованы данные Мак Кетта, Силь-берберга и Куо (Me Ketta, Silberberg and Kuo) [IV. 83], представленные на рис, IV. 18. Для смесей газов, находящихся при давлениях ниже 800 мм рт. ст., объемы можно принимать по правилу аддитивности.
Таблица IV.9
Критические свойства компонентов природных газов*
|
Компонент | Моле куляр ный вес | Крити ческая темпе ратура, •к | Крити ческое давле ние, am |
| 16,04 | 190,5 | 47,1 | |
|
30,07 | 305,4 |
49,5 | |
| 44,09 | 370,0 | 43,2 |
|
| Изобутан............ |
58,12 | 408,2 |
37,0 |
| к-Бутан ............ | 58,12 |
425,2 | 38,5 |
| Изопентан ........... |
72,15 | 461,0 |
33,8 |
|
к-Пентан............ | 72,15 | 469,7 | 34,2 |
| Изогексан 49**......... |
84,16 | 489,6 |
31,5 |
| Изогексан 60.......... | 84,16 |
498,0 | 30,9 |
| к-Гексан 68........... |
84,16 | 508,0 |
30,8 |
| Изопентан 79.......... | 98,18 |
521,2 | 29,2 |
| Изогептан 90.......... |
98,18 | 531,2 |
28,0 |
| н-Гептан 98 ........... | 98,18 |
540,4 | 27,8 |
| Изооктан 110.......... |
114,22 | 555,2 |
26,5 |
| Изооктан 116 ......... | 114,22 |
566,3 | 27,4 |
| н-Октан 126.......... |
114,22 | 569,5 |
25,3 |
|
128,25 | 595,2 |
23,2 | |
|
142,28 | 616,2 |
21,4 | |
| 4,0 | 5,0 | 2,3 |
|
| 29,0 |
132,2 | 38,3 | |
| 28,02 | 125,8 | 34,4 | |
|
Кислород............ | 32,0 | 154,2 | 51,0 |
| Углекислый газ......... | 44,01 | 304,2 |
75.1 |
|
Сероводород .......... |
34,08 | 373,6 |
91,4 |
* Данные взяты из [1.15]
•• Температура кипения в °С.
ПсевдоприВеденное давление г 3 4 5 6
коэффициент сти**ов*ости
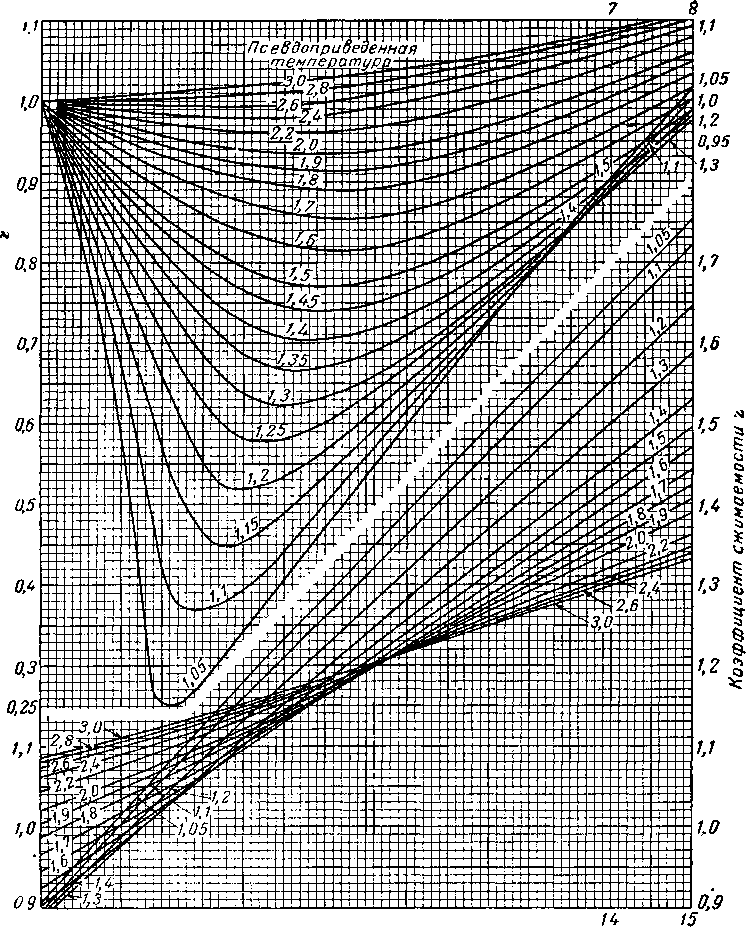
Рис. IV. 16. Коэффициент сжимаемости.
а — для природных газов до давления 700 ат\ в — для природных газов при давлениях от 700 до 1400 ат.
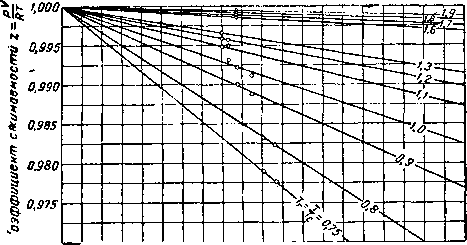
О 0D05 0,010 0,015 OJ025 0,025 0,030 0,035 0.040 0.045 0.050 Приведенное давление рг- ?¦
Рис. IV. 17. Коэффициенты сжимаемости природных газов при давлениях, близких к атмосферному [IV. 83 а].
15 16 17 18 19 20 21 22 23 2U 25 26 27 28 29 30
ПсевдоприВеденное давление
Коэффициент сжимаемости 2 • Коэффициент сжимаемости г
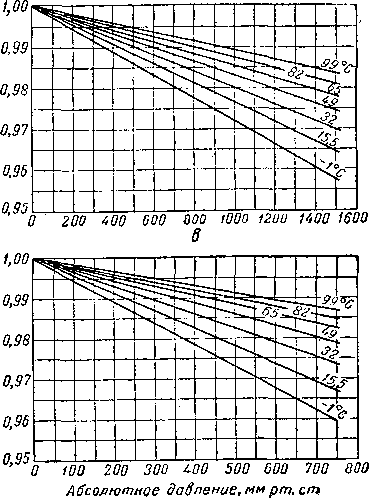
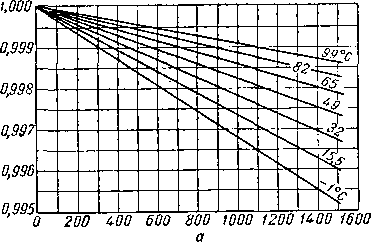
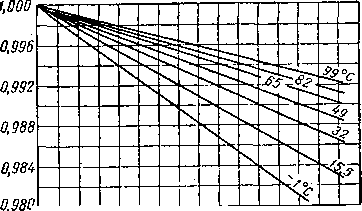
О 200 ЬОО 600 800 1000 >200 >400 1600
Абсолютное давление, мм рт. ст. 6
Рис. IV. 18. Коэффициенты сжимаемости индивидуальных углеводородов при давлении, близком к атмосферному [ IV.83]
а — изотермы сжимаемости метана; б—изотермы сжимаемости этана; в—изотермы сжимаемости пропана; е—изотермы сжимаемости к*бутана.
3. ВЛИЯНИЕ НЕУГЛЕВОДОРОДНЫХ КОМПОНЕНТОВ
Природные газы часто в больших количествах содержат углекислый газ, азот и сероводород. В связи с этим рассмотрим влияние неуглеводородных газов с точки зрения применимости теоремы соответственных состояний к природным газам. Исследования pVT-соотношеиий для смеси метана с азотом проводились Кейсом и Барк-сом (Keyes and Burks) [IV. 55], а для природного газа, содержащего 8,5 и 18,8% мол. азота, Эйлертсом, Карлсоном и Малленсом (Eilerts, Carlson and Mullens) [IV. 30].
В табл. IV. 10 приведены данные анализа некоторых природных газов, а в табл. IV. 11 сравниваются коэффициенты сжимаемости этих газов, определенные по приведенным давлениям и температурам (с использованием диаграммы рис. IV. 16), со значениями этих коэффициентов, определенными экспериментально.
Таблица IV. 10 Состав природных газов, содержащих азот*
|
Наименование | I аз 1 |
1 аз 2 | Газ 3 |
|
Удельный вес..... | 0,64Э | 0,675 | 0,706 |
| Псевдокритические: | |||
|
температура, °К . • |
208,4 | 201,8 |
193,3 |
| давление, am . . . | 46,8 |
45,9 | 44,5 |
| Молярные доли: | |||
| азот ....... |
0,0069 | 0,0855 |
0.1884 |
| метан ....... | 0,8771 |
0,8077 | 0,7169 |
| 0,0649 | 0,0598 | 0,0530 | |
|
пропан ...... | 0,0322 |
0,0297 | 0,0263 |
| изобутан ..... |
0,0076 | 0,0070 |
0,0062 |
|
н-бутан...... | 0,0058 | 0,0053 | 0,0047 |
| изопентан ..... |
0,0021 | 0,0019 |
0,0017 |
| н-пентан ...... | 0,0012 |
0,0111 | 0,00099 |
| гексаны, 135—56** . |
0,00070 | 0,00063 |
0,00058 |
| гексаны, 56—35 . . | 0,00036 |
0 00033 | 0,00029 |
| гептаны, 35—17 . . |
0,00034 | 0,00031 |
0,00028 |
| гептаны, 17—11 . . | 0,00012 |
0,00011 | 0,00010 |
| октаны и высшие |
0,00068 | 0,00062 |
0,00056 |
* Данные взяты нз [IV-30].
** Давление насыщенного пара в нм рт, cm. прн 0° С.
Таблица IV. 11 Сравнение рассчитанных и экспериментально определенных* значений коэффициентов сжимаемости газов, состав которых приведен в табл. IV. 10
| Абсо лютное | Коэффициент сжимаемости г | |||||
| газ I; |
0,7% М2 | Газ 2 |
8,5% N2 | газ 3; |
18,8% N2 | |
| давле-нне, am | расче т-ный |
экспери менталь ный |
расчет ный | экспери менталь ный | расчет ный | экспери менталь ный |
|
Температура 0° С | ||||||
| 98 112 126 140 210 280 350 | 0,685 0,658 0,640 0,634 0,687 0,802 0,932 | 0,6885 0,6593 0,6433 0,6369 0,6981 0,8103 0,9333 | 0,715 0,692 0,676 0,668 0,717 0,822 0,942 |
0,7270 0,7024 0,6871 0,6797 0,7258 0,8287 0.9443 | 0,748 0,736 0,720 0,713 0,750 0,853 0,970 | 0,7747 0,7557 0,7410 0,7343 0,7720 0,8660 0,9736 |
|
Абсо лютное |
Коэффициент сжимаемости z | |||||
| газ 1* | U,7% N3 | газ 2 | 8,5% N2 | газ 3; | 18.8% N2 | |
| давле ние, am | расчет ный |
экспери-менталь-н ы й |
расчет ный | экспери* менталь* н ый | расчет ный | экспери* менталь ный |
Температура 37,8° С
| 98 |
0,812 | 0,8213 |
0,832 | 0,8443 |
0,855 | 0,8706 |
| 112 | 0,797 |
0,8044 | 0,816 |
0,8299 | 0,843 |
0,8596 |
| 126 |
0,782 | 0,7896 |
0,805 | 0,8188 |
0,832 | 0,8518 |
| 140 | 0,773 |
0,7805 | 0,795 |
0,8102 | 0,825 |
0,8461 |
| 210 |
0,785 | 0,7901 |
0,810 | 0,8210 |
0,838 | 0 8584 |
| 280 | 0,858 |
0,8600 | 0,880 |
0,8864 | 0,910 |
0,9193 |
| 350 |
0,852 | 0,9516 |
0,960 | 0,9750 |
0,996 | 1,0031 |
Температура 87,8°С
| 98 |
0,896 | 0,9097 |
0,911 | 0,9234 |
0,922 | 0,9401 |
| 112 | 0,888 |
0,9009 | 0,903 |
0,9171 | 0,917 |
0,9362 |
| 126 |
0,872 | 0,8943 |
0,898 | 0,9125 |
0,912 | 0,9333 |
| 140 | 0,875 |
0,8899 | 0,892 |
0,9097 | 0,910 |
0,9317 |
| 210 |
0,876 | 0,8932 |
0,899 | 0,9164 |
0,918 | 0,9437 |
| 280 | 0,927 |
0,9356 | 0,947 |
0,9577 | 0,970 |
0,9849 |
| 350 |
0,998 | 1,005 |
1,012 | 1,0196 |
1,033 | 1,0459 |
Температура 137,8° С
| 98 |
0,941 | 0,9557 |
0,952 | 0,9640 | ||
| 112 |
0,938 | 0,9516 |
0,946 | 0,9625 | ||
| 126 |
0,935 | 0,9486 |
0,948 | 0,9615 |
0,952 | 0,9748 |
| 140 | 0,932 |
0,9472 | 0 945 |
0,9612 | 0,952 |
0,9761 |
| 210 |
0,939 | 0,9571 |
0,953 | 0,9733 |
0,970 | 0,9928 |
| 280 | 0,980 |
0 9890 | 0,998 |
1,0058 | 1,012 |
1,0269 |
| 350 |
1,022 | 1,0384 |
1,050 | 1,0547 |
1,064 | 1,0754 |
•Экспериментальные данные взяты из [IV. 30].
Из табл. IV. 11, видно, что значения коэффициентов сжимаемости, определенные путем расчета при высоких температурах и небольших давлениях, примерно на 2% меньше значений, полученных экспериментально.
Ример, Олдс, Седж и Леси (Reamer, Olds, Sage and Lacey) [IV. 72] исследовали сжимаемость смесей метана и углекислого газа при температуре от 37,8 до 237,8° С и при давлении до 700 ат. Значения коэффициентов сжимаемости при температурах 37,8 и 137,8° С приведены в табл. IV. 12. Сравнение коэффициентов сжимаемости, определенных экспериментально (табл. IV. 12) для газов, содержащих ие более 1—2% мол. СОг, с коэффициентами сжимаемости, рассчитанными по приведенным давлениям и температурам, показывает достаточно хорошее согласие этих данных. При более высоком процентном содержании СОг в газе различие становится существенным.
Коэффициенты сжимаемости для смеси метана и сероводорода (рис. IV. 19) исследованы Римером, Сед-жем и Леси [IV. 73]. Они же приводят значения удельных объемов смеси метан—сероводород при высоких концентрациях метана в смеси (табл. IV. 13)'.
метана и углекислого газа
| Давле ние, | Коэффициент сжимаемости г | ||
|
весовые доли метана | |||
| 0 | | 0,0852 | 0,19912 | 0,3583 |
0,6685 | |
Температура 37,8° С
| 0 |
1,000 | 1 0000 |
1,0000 | 1,0000 |
1,0000 |
| 14 |
0,941 | 0,9512 |
0,9606 | 0,9685 |
0,9760 |
| 28 |
0,875 | 0,8995 |
0,9202 | 0,9372 |
0,9525 |
| 42 |
0,798 | 0,8437 |
0,8788 | 0,9063 |
0,9296 |
| 56 |
0,704 | 0,7830 |
0,8360 | 0,8754 |
0,9075 |
| 70 |
0,580 | 0,7160 |
0,7920 | 0,8451 |
0,8869 |
| 87,5 |
0,315 | 0,6262 |
0,7350 | 0,8084 |
0,8634 |
| 105 |
0,255 | 0,5388 |
0,6830 | 0,7738 |
0,8428 |
| 122, |
0,272 | 0,4715 |
0,6402 | 0,7460 |
0,8259 |
| 140 |
0,299 | 0,4438 |
0,6100 | 0,7243 |
0,8131 |
| 175 |
0,355 | 0,4565 |
0,5890 | 0,7041 |
0,8027 |
| 210 |
0,411 | 0,4958 |
0,6055 | 0,7103 |
0,8081 |
| 245 |
0,465 | 0,5247 |
0,6400 | 0,7335 |
0,8260 |
| 280 |
0,519 | 0,5921 |
0,6820 | 0,7702 |
0,8565 |
| 315 |
0,572 | 0,6433 |
0,7276 | 0,8130 |
0,8937 |
| 350 |
0,624 | 0,6947 |
0,7755 • | 0,8584 |
0,9363 |
| 420 |
0,727 | 0,7976 |
0,8752 | 0,9531 |
1,0291 |
| 490 |
0,828 | 0,8982 |
0,9745 | 1,0502 |
1,1240 |
| 560 |
0,926 | 0,9995 |
1,0745 | 1,1469 |
1,2187 |
| 630 |
1,023 | 1,1012 |
1,1752 | 1,2448 |
1,3130 |
| 700 |
1,116 | 1,2035 |
1,2785 | 1,3414 |
1,4078 |
Температура 137,8° С
| 0 |
1,000 | 1,0000 |
1,0000 | 1,0000 |
1,0000 |
| 14 |
0,979 | 0,9834 |
0,9872 | 0,9901 |
0,9931 |
| 28 |
0,957 | 0,9668 |
0,9747 | 0,9805 |
0,9866 |
| 42 |
0,934 | 0,9503 |
0,9625 | 0,9713 |
0,9805 |
| 56 |
0,912 | 0,9339 |
0,9507 | 0,9627 |
0,9749 |
| 70 |
0,889 | 0,9179 |
0,9397 | 0,9545 |
0,9699 |
| 87,5 |
0,862 | 0,8987 |
0,9263 | 0,9453 |
0,9649 |
| 105 |
0,835 | 0,8810 |
0,9145 | 0,9379 |
0,9608 |
| 122,5 |
0,810 | 0,8643 |
0,9040 | 0,9313 |
0,9583 |
| 140 |
0,787 | 0,8487 |
0,8950 | 0,9267 |
0,9572 |
| 175 |
0,750 | 0,8247 |
0,8820 | 0,9217 |
0,9588 |
| 210 |
0,729 | 0,8125 |
0,8763 | 0,9226 |
0,9650 |
| 245 |
0,720 | 0,8100 |
0,8778 | 0,9289 |
0,9759 |
| 280 |
0,724 | 0,8154 |
0,8865 | 0,9404 |
0,9914 |
| 315 |
0,737 | 0,8290 |
0,9020 | 0,9571 |
1,0109 |
| 350 |
0,759 | 0,8483 |
0,9223 | 0,9788 |
0,0337 |
| 420 |
0,818 | 0,8992 |
0,9721 | 1,0306 |
1,0848 |
| 490 |
0,883 | 0,9592 |
1,0310 | 1,0877 |
1,1423 |
| 560 |
0,952 | 1,0243 |
1,0955 | 1,1495 |
1,2030 |
| 630 |
1,023 | 1,0921 |
1,1610 | 1,2148 |
1,2672 |
| 700 |
1,091 | 1,1605 |
1,2268 | 1,2817 |
1,3350 |
* Данные взяты из [IV. 72].
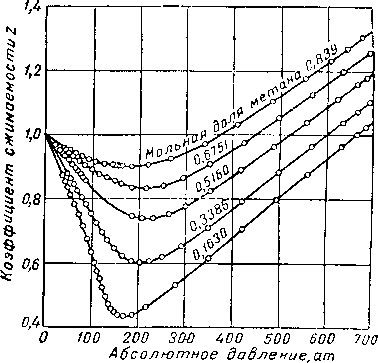
Рис. IV. 19. Коэффициенты сжимаемости для системы метан — сероводород [IV. 73].
Таблица IV.13
Мольные объемы смесей метана и сероводорода*
| Мольный |
объем | смеси, смг/моль | ||||||
|
Давле | при 4 | 4“ С | | при 37,8* С | | при 71,1° С j |
при 137,8° С | |||
| ние, ата | Мольная доля | метана |
в смеси | |||||
|
0,8 ) | 0,9 | 0,8 |
0,9 | 0,8 | 0,9 | 0,8 | 0,9 | |
| 14 | 1617 |
1625 | 1837 |
1844 | 2053 |
2060 | 2475 |
2480 |
| 28 |
772 | 782 |
892 | 900 |
1009 | 1015 |
1229 | 1232 |
| 42 | 491 |
501 | 573 |
586 | 660 |
666 | 813 |
817 |
| 56 |
348 | 360 |
421 | 434 |
485 | 493 |
606 | 610 |
|
70 | 263 |
277 | 327 |
335 | 381 |
393 | 481 |
486 |
| 87,5 |
194 | 211 |
252 | 261 |
298 | 306 |
382 | 386 |
|
105 | 150 |
169 | 202 |
211 | 243 |
251 | 316 |
321 |
| 122,5 |
122 | 138 |
167 | 177 |
204 | 213 |
269 | 274 |
|
140 | 103,5 |
117,5 | 142,8 |
152,5 | 176,4 |
184 | 234 |
239 |
| 157,5 |
91,4 | 103,5 |
124,9 | 134,2 |
154,8 | 162,5 |
206 | 212 |
|
175 | 83,4 |
93,7 | 111,5 |
120,6 | 138,0 |
145,6 | 186,1 |
190,6 |
| 192,5 |
77,7 | 86,4 |
101,5 | 109,8 |
125,2 | 132,7 |
169,0 | 179,9 |
| 210 | 73,4 |
80,9 | 94,0 |
101,3 | 115,1 |
122,0 | 155,0 |
160,0 |
| 245 |
67,3 | 73,0 |
83,5 | 89,5 |
100,7 | 106,1 |
134,0 | 138,6 |
| 280 | 63,2 |
67,6 | 76,0 |
81,0 | 90,3 |
95,4 | 119,0 |
123,5 |
| 315 |
60,1 | 63,8 |
70,8 | 75,1 |
82,9 | 87,3 |
107,6 | 111,8 |
| 350 | 57,8 |
61,0 | 67,0 |
70,8 | 77,5 |
81,1 | 99,0 |
102,6 |
| 420 |
54,6 | 57,6 |
61,8 | 64,7 |
69,8 | 72,8 |
87,0 | 90,0 |
| 490 | 52,2 |
54,3 | 58,2 |
60,4 | 64,5 |
67,0 | 78,7 |
81,2 |
| 560 |
50,5 | 52,2 |
55,5 | 57,4 |
61,0 | 63,0 |
72,7 | 75,0 |
| 630 | 49,0 |
50,5 | 53,3 |
55,1 | 60,5 |
60,0 | 68,2 |
70,2 |
| 700 |
47,7 | 49,1 |
51,6 | 53,1 |
55,8 | 57,4 |
75,8 | 66,4 |
* Данные взяты из [IV. 73].
Гексаны, гептаны и более тяжелые компоненты парафинового ряда как нормального, так и изомерного строения могут находиться в природном газе. При фракционном разделении такие индивидуальные компоненты трудно выделить в чистом виде, и поэтому часто они собираются в виде жидких фракций, для которых затем определяются удельный и молекулярный веса. Кей (Kay) [IV. 54] предложил метод определения псевдо-критически.х параметров жидких углеводородов, дополненный впоследствии Смитом и Ватсоном (Smith and Watson) [V. 86], для применения которого необходимо знать наклон кривой точек кипения, а также молеку-
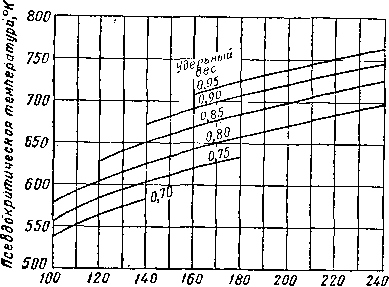
Иолекулярный вес-
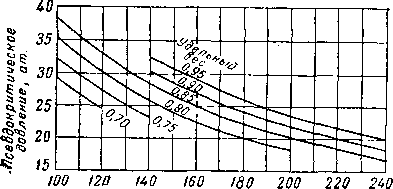
Молекулярный бес
4. ПСЕВДОКРИТИЧЕСКИЕ ПАРАМЕТРЫ ГЕПТАНОВ 5. ОПРЕДЕЛЕНИЕ ПСЕВДОКРИТИЧЕСКИХ
И БОЛЕЕ ТЯЖЕЛЫХ КОМПОНЕНТОВ ПАРАМЕТРОВ ПО УДЕЛЬНОМУ ВЕСУ ГАЗА
Рис. IV. 20. Псеодокритические давления и температуры для гептанов + высшие [IV. 60].
лярный и удельный веса жидкости. Потребовалось проведение ряда микродистилляций фракции конденсатов, содержащих гептан и более тяжелые углеводороды для составления графика (рис. IV. 20), с помощью которого можно определить взаимную связь между псевдокри-тическими свойствами и молекулярным и удельным весами. Считается, что применение этого графика для пентанов +, гексанов + и гептанов + является удовлетворительным !. Стендинг и Катц (Standing and Katz) [IV. 87] использовали этот график для сравнения коэффициентов сжимаемости насыщенных паров углеводородных жидкостей молекулярного веса до 157.
Псевдокритические параметры обычно применяются для расчета псевдокритических свойств природного газа подобно тому, как критические температуры и давления используются с той же целью для индивидуальных компонентов.
1 Пентаны 4- , гексан 4- . гептаны 4- обозначают пентаны и более тяжелые углеводороды, гексаны и более тяжелые, гептаны и более тяжелые. — Прим. ред.
Известно, что природные газы близки по составу [IV. 57]. Поэтому можно ожидать, что природные газы по крайней мере в пределах одного месторождения должны иметь такой состав, чтобы их псевдокритические температура и давление являлись функцией удельного веса газа. На рис. IV. 21 [IV. 60] приведены псевдокритические параметры в зависимости от удельного веса для
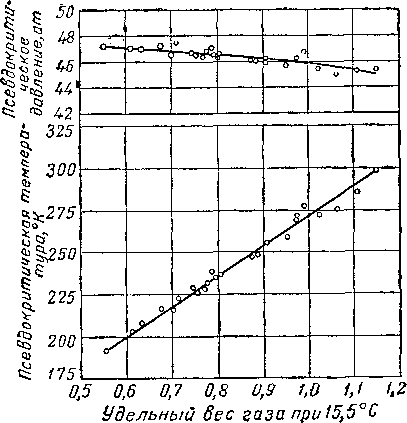
Рис. IV. 21. Псевдокритические свойства природных газов месторождения Оклахома Сити [IV. 60].
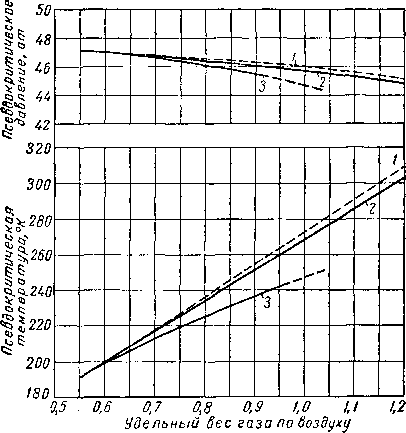
Рис. IV. 22. Псевдокритические свойства природных газов [I, 2].
1 — углеводородные газы (IV. 3); 2*— смесь газов [I.2J; 3 — Продукция газоконденсаторных скважин
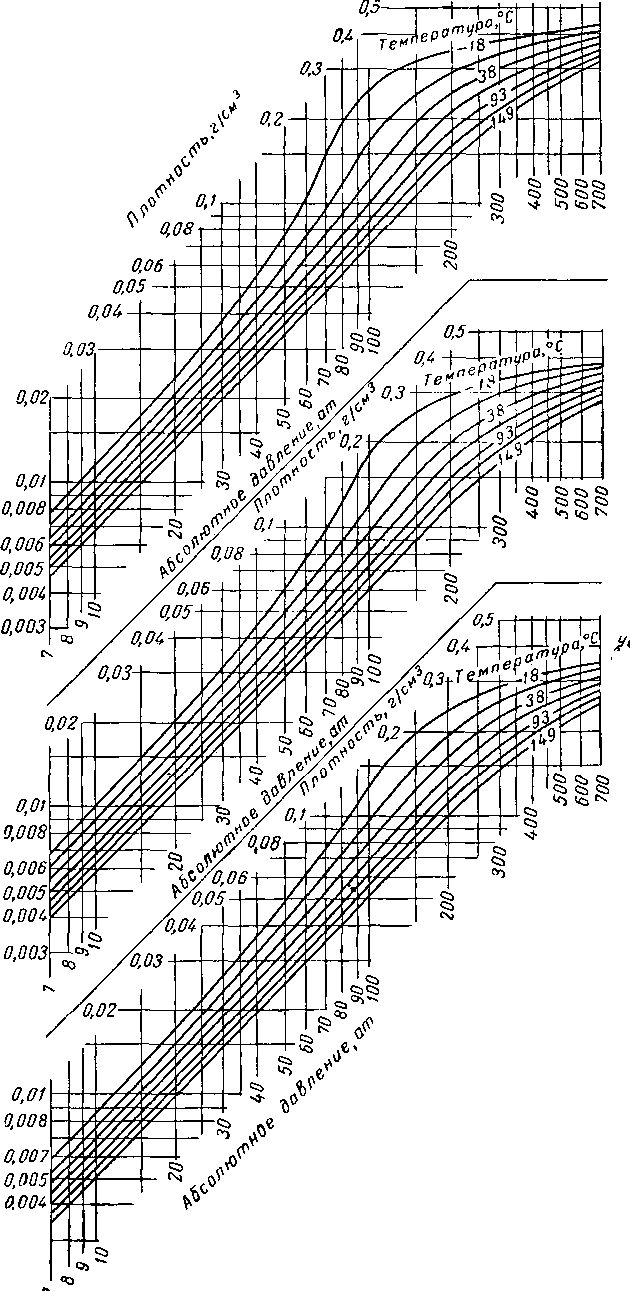
Удельный Вес газа по воздуху 0,8
Удельный вес газа по воздух и О,?
тельный оес газа по Воздуху 0,6
газов с промысла и газолинового завода месторождения Оклахома Сити. Кроме того, было установлено, что если газы содержат менее 2—3% неуглеводородных компонентов, значения их псевдокритических параметров ложатся на одну кривую при выражении в зависимости от удельного веса [I. 2, IV. 60, IV. 87].
Конденсатные газы, содержащие высокомолекулярные компоненты, увеличивающие их удельный вес, имеют кривые зависимости псевдокритических параметров от удельного веса, несколько отличные от кривых, соответствующих сухим газам [1.2]. Калифорнийская ассоциация природного газолина [IV. 3] приняла для практического пользования соотношение между относительным удельным весом газа по воздуху и его псевдокритически-ми параметрами, которое иллюстрируется графиком (рис. IV. 22).
Для газов, которые подчиняются зависимости, приведенной на рис. IV. 22, коэффициент сжимаемости или плотность являются функцией удельного веса газа, температуры и давления. Зависимость плотности природного газа в функции температурных давления представлена на рис. IV. 23. Следует отметить, что псевдокрити-ческие параметры для газов с относительным удельным весом 0,7 и 0,8 соответствуют конденсатным газам.
При изучении р^Г-соотношений некоторых природных газов было обнаружено, что при определенных условиях система состоит из двух фаз, но коэффициент сжимаемости всей системы имеет при этом то же значение, что и при однофазном состоянии. Для изучения вопроса применения коэффициента сжимаемости для определения плотности двухфазной системы при высоких давлениях было проведено рУГ-исследование смеси природного газа и природного газолина. Фазовая диаграмма для такой смеси приведена на рис. IV. 24. На ней имеются все те же области, что и на диаграмме для газа высокого давления. Влияние присутствия небольшого количества сжиженной фазы на общую плотность системы представляет большой интерес для проведения расчетов фазовых состояний.
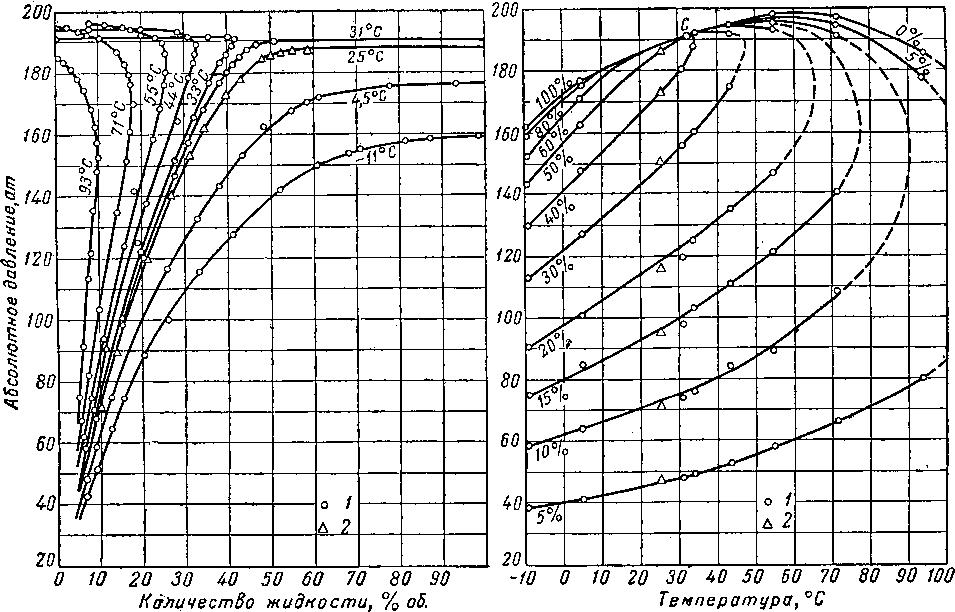
Рис. IV. 24. Диаграмма фазового состояния для системы природный газ — газолин [111, 28],
1 — первый опыт А; 2 — второй опыт В,
В табл. IV. 14 сравниваются рассчитанные и экспериментально измеренные значения плотности для смеси природный газ — природный газолин. Вычисления производились в предположении, что для подсчета плотности можно пользоваться уравнением состояния [IV. 2], включающем коэффициент сжимаемости.
В этой таблице значения объемного процентного содержания жидкости взяты из фазовой диаграммы, приведенной на рис. IV. 24. Анализ данных приведенных в табл. IV. 14, показывает, что формула [IV. 2], включающая коэффициент сжимаемости, может применяться для расчета плотности смеси в однофазной области (выше кривой точек кипения), на небольшом участке двухфазной области (ниже кривой точек кипения) и во всей двухфазной области при высоких температурах, когда система содержит небольшое количество жидкой фазы. Область, для которой эти расчеты могут производиться, ограничена значениями истинной приведенной температуры, равной 1,05 и выше.
Исследование фазового состояния системы метан-бутан также показывает, что при высоком давлении
Таблица IV. 14 Сравнение вычислительных и экспериментально измеренных значений плотностей жидкости в однофазной и двухфазной системах*
| Абсолют | Вычисленные значения |
Экспериментально измеренные значения | ||
| ное давление | Z |
плотность, г/см* |
плотность, г/сж12 |
содержание жидкой фазы, % |
Температура 4,5° С, псевдоприведенная температура 1,13, истинная приведенная температура 0,91
| 202 |
0,628 | 0,380 |
0,376 | Однофазная |
| 177 | 0,569 | 0,367 | 0,366 |
» |
| 172 |
0,556 | 0,364 |
0,361 | 60,5 |
| 153 | 0,511 |
0,353 | 0,320 |
43,2 |
| 105 |
0,43 | 0,287 |
0,204 | 20,7 |
| 47 | 0,680 |
0,083 | 0,082 |
6,6 |
Температура 31° С, псевдоприведенная температура 1,21, истинная приведенная температура 0,995
| 203 |
0,658 | 0,339 |
0,334 | Однофазная |
| 190 | 0,633 | 0,330 | 0,326 |
» |
| 189 |
0,631 | 0,328 |
0,323 | 46,7 |
| 184 | 0,662 |
0,324 | 0,314 |
41,7 |
| 177 |
0,609 | 0,319 |
0,300 | 38,3 |
| 147 | 0,558 |
0,289 | 0,246 |
28,0 |
| 99 |
0,542 | 0,200 |
0,157 | 15,2 |
| 68,5 | 0,660 |
0,114 | 0,103 |
8,9 |
Температура 71°С, псевдоприведенная температура 1,40, истинная приведенная температура 1,13
| 196 | 0,728 | 0,256 |
0,263 | Однофазная |
| 194 |
0,727 | 0,254 |
0,263 | 3,9 |
| 183 | 0,718 |
0,242 | 0,246 |
16,1 |
| 161 |
0,705 | 0,217 |
0,216 | 16,7 |
| 135 | 0,706 |
0,181 | 0,176 |
14,1 |
| 104 |
0,738 | 0,13 |
0,132 | 9,9 |
| 67,3 | 0,815 |
0,079 | 0,082 |
5,1 |
|
мпература 93,5° С, |
псевдоприведенная температура 1,49, | |||
| истинная приведенная температура |
1,20 | |||
| 207 |
0,788 | 0,235 |
0,243 | Однофазная |
| 184 | 0,774 | 0,213 | 0,221 |
1,4 |
| 158 | 0,769 | 0,208 |
0,215 | 1,5 |
| 157 | 0,764 |
0,184 | 0,188 |
9,4 |
| 136 |
0,769 | 0,158 |
0,159 | 8,7 |
| 114 | 0,787 |
0,129 | 0,130 |
7,4 |
| 91 |
0,814 | 0,100 |
0,102 | 5,9 |
| 75 | 0,842 |
0,079 | 0,082 |
4,7 |
• Данные взяты из [IV. 60].
Однако при давлениях, превышающих 70 ат, когда температура выше критической температуры смесит, присутствие жидкой фазы при содержании, не превышающем 10%, по-видимому, не влияет на расчет средней плотности смеси методом, основанным на применении коэффициента сжимаемости.
7. ОТРИЦАТЕЛЬНЫЙ КАЖУЩИЙСЯ ОБЪЕМ ЖИДКИХ КОМПОНЕНТОВ
Понятие об отрицательном кажущемся объеме жидкости, растворенной в газе высокого давления, становится ясным из данных, получаемых при изучении сжимаемости газа [IV. 52]. Один из авторов при подготовке опыта с природным газом в бомбе высокого давления заметил его необычайное поведение. Газ при температуре 24° С и давлении 140 ат, не содержащий жидкости, был охлажден до 0° С. После этого из бомбы было извлечено около 0,5 л жидкости. Далее температура в бомбе была вновь поднята до 24° С. При этом давление в бомбе поднялось до 144,2 ат. Отсюда следует, что если извлеченную жидкость снова закачать в бомбу, то давление в ней будет уменьшаться. Был проведен также эксперимент в бомбе с смотровым окном, в которой содержалось при температуре 37,8° С и давлении 140 ат 0,859 моль метана. Бутан из расчета 0,141 г/моль закачивался в бомбу, при этом температура в ней поддерживалась равной 37,8° С. Когда закачка бутана была закончена, давление в бомбе снизилось до 134 ат, при этом смесь метана и бутана в бомбе находилась в однофазном состоянии. В связи с этим представляет интерес диаграмма, приведенная на рис. IV. 25, построенная по данным Седжа, Хикса и Леси [IV. 62] для системы метан—бутан [IV. 52]. В пределах площади 1 бутан имеет отрицательный кажущийся объем, т. е. один метан при тех же значениях температуры и давления будет занимать объем больший, чем в смеси с бутаном. Бутан влияет на силы взаимодействия между молекулами метана так, что облегчается их сближение друг с другом. В пределах площади 2 значение кажущегося объема изменяется от нуля до значения, соответствующего чистому жидкому бутану. И, наконец, в пределах площади 3 кажущийся объем бутана в газовой фазе превышает таковой для жидксй фазы. При давлении, близком к атмосферному, объем таких компонентов в газовой фг-.зе приближается к объему идеального газа.
°/20 <ь ы
^ 80
о | 60
g ы
я;
О __
О 0,2 0,и 0,6 ОД 1,0
Весовая доля метана
Рис. IV. 25. Кажущиеся объемы бутана в насыщенной смеси метан—бутан [1П. 62, III. 63, IV. 52].
8. ВЛИЯНИЕ МОЛЕКУЛЯРНОЙ ПРИРОДЫ ВЕЩЕСТВА НА СЖИМАЕМОСТЬ
Отклонение поведения газов от теоремы соответственных состояний, а также возможность существования явления отрицательных кажущихся объемов при растворенни других углеводородов в метане показывают, что поведением молекул управляют силы меж-молекулярного взаимодействия и что потребуется накопление определенного количества знаний, прежде чем вопрос о предсказании объемного поведения компонентов будет решен окончательно.
Чтобы охарактеризовать отклонение поведения молекул реальной жидкости от поведения молекул совершенной жидкости, Питзер (Pitzer) [IV. 68] предложил ввести параметр несовершенства п. Этот параметр является функцией упругости пара Ps, соответствующего значению приведенной температуры, равному 0,7, и функцией критического давления рс\
Рс_
Р.
(IV. 22
— I.
Рг
Часто в термодинамических расчетах требуется знать функциональную зависимость коэффициента сжимаемости от давления и температуры. Значения коэффициента сжимаемости, приведенные в табл, II. 2, были рассчитаны по диаграмме рис. IV. 16, построенной в крупном масштабе.
В приложении даются следующие функции (в виде тпблиц и в графическом виде).
Таблица II. 2: коэффициенты сжимаемости природных газов.
Рг
Табл. П. 3: J zdpr.
Рг
Табл. П. 4: Г г ,
0,2 0,2 Табл. П. 5: j zdpr и j —d/7,..
Рг
На рис. IV. 26 представлена зависимость коэффициента сжимаемости от параметра несовершенства для различных значений приведенной температуры. График построен для приведенного давления, равного 1,6.
Табл.
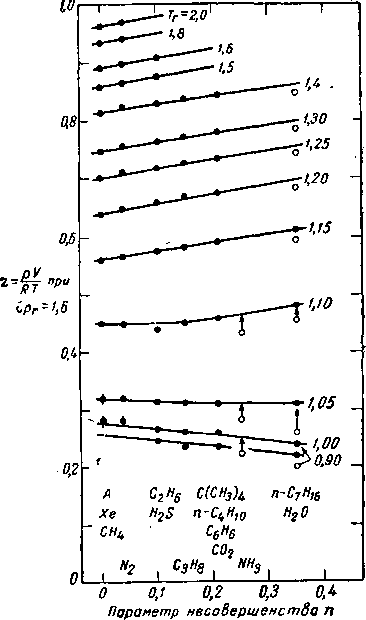
Рис. IV. 26. Зависимость коэффициента сжимаемости от параметра несовершенства ПРИ рг = 1,6 [IV. 68].
Табл. П. 7:
0,5+ Г г/Рг
Табл. П.
J.1 + B(z/prydpr
10. ДИАГРАММА СЖИМАЕМОСТИ ПРИРОДНЫХ ГАЗОВ
Иногда необходимо выразить сжимаемость природных газов по форме, обычно применяемой для выражения сжимаемости жидкостей. В этом случае сжимаемость газа определяется следующим равенством:
_
Cg = ~ Vdp'
(IV. 23)
Труб (Trube) [IV. 93] определяет псевдоприведенную сжимаемость Сг, произведением Cg-Pc, являющимся безразмерной величиной. Значения Сг он вычислял по коэффициентам сжимаемости природных газов (рис. IV, 16) на основании следующего соотношения:
Г4 Г* п ^ ^
(IV. 24)
На рис. IV. 27 и IV. 28 приведены кривые зависимости псевдоприведенной сжимаемости от приведенной температуры и приведенного давления.
Пример.
Требуется определить сжимаемость природного газа удельного веса 0,65 при давлении 101 ат и температуре 68° С.
Газ удельного веса 0,65 имеет ГС = 208°К и ре =¦> = 45,6 ат (см. рис. IV. 22):
68+ 273 „ 101
Тг='
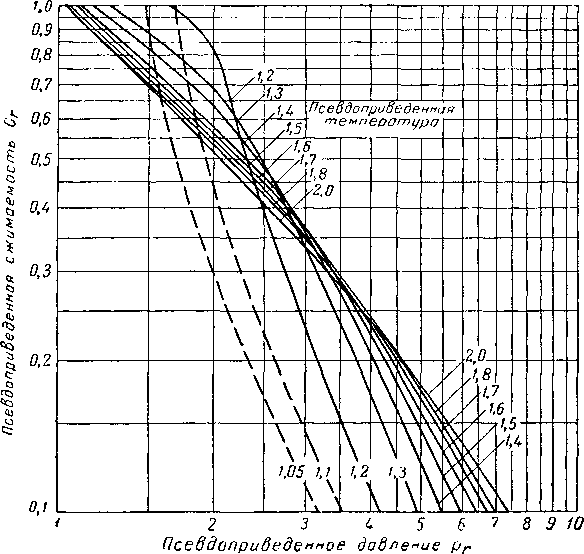
Рис. IV. 27. Сжимаемость природных газов [IV. 93].
Рис. IV. 28. Сжимаемость природных газов [IV. 93].
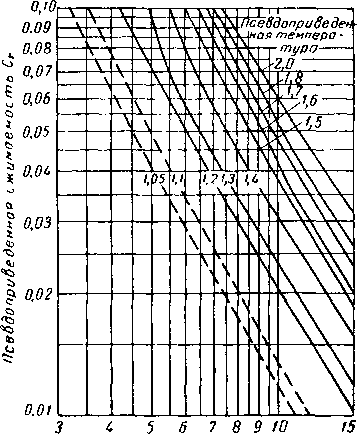
ПсвВдопоидедеппое давление р.
Из рис. IV. 27 по данным Тг и рг находим Сг = 0,51. п.К1 ед. объема
0,51
С" = 45Г6 = 0'0112,
' (ед. объема) X (ат)
II. ПЛОТНОСТЬ ЖИДКОСТЕЙ
Плотность индивидуальных соединений в жидком состоянии при увеличении температуры уменьшается, принимая при критической температуре значение плотности пара (рис. IV. 29). Аналогично этому изменяется и плотность смеси жидкостей (значения плотностей индивидуальных соединений в жидком состоянии см. в [IV. 1]). На рис. IV. 30 приведена плотность пропана в зависимости от температуры [1.2].
В лабораторных исследованиях плотности жидкостей обычно измеряются с помощью ареометра или пикнометра. Температурные поправки к плотностям жидкостей для приведения к какой-либо стандартной температуре, например 20° С, можно найти в стандартных таблицах [IV. I]. Индивидуальные углеводороды в жидком состоянии (например, пентан и гексан) при комнатных температуре и давлении имеют почта аддитивные объемы 13.
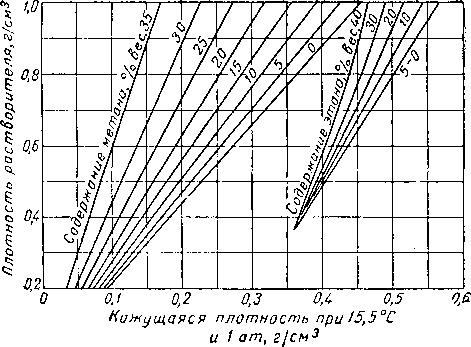
Плотность углеводородных жидкостей может быть рассчитана по их составу и плотностям входящих в них компонентов [IV. 88, I. 19, I. 2]. При этом предполагается, что объемы пропана и более тяжелых углеводородов при температуре 15,5° С аддитивные. Зная плотность смесей жидкостей, содержащих метан и более тяжелые углеводороды при температуре 15,5° С и давлении 1 ат, можно вычислить кажущуюся плотность растворенного метана. На рис. IV. 31 приведены значения кажущейся плотности метана и этана, растворенных в углеводородных жидкостях, в зависимости от их про-ценгного содержания и плотности растворителя. Пример расчета плотности жидкости по ее составу приведен в табл. IV. 15. При растворении азота в жидкости плотностью 0,68 г/см3 его кажущаяся плотность составляет 0,48 г/см3.
Таблица /V. 15
Пример расчета плотности жидкости по ее составу при давлении 112 am и температуре 49° С
| Компонент | Моляр ная доля жид кости |
Моле куляр ный вес | Моли | Плотность жидкости, г/см3 |
А О 3 |
| Углекислый газ . . . |
0,0029 | 44 |
0,13 | (0,420) |
0,31 |
| Метан....... | 0,2943 | 16 |
4,73 | (0,320) |
14,77 |
|
0,0510 | 30 |
1,53 | (0,485) |
3,16 | |
|
0,0356 | 44 |
1,57 | 0,5072 |
3,09 | |
|
Изобутан...... | 0,0167 | 58 | 0,97 |
0,5625 | 1,72 |
| 0,0275 | 58 | 1,60 | 0,5836 | 2,75 | |
|
Пентаны...... | 0,1463 |
72 | 10,55 |
0,6270 | 16,80 |
| Гексаны...... | 0,1283 | 86 | 11,05 |
0,6630 | 16,70 |
| Гептаны -{-..... |
0,2974 | 196 |
58,30 | 0,8500 |
68,50 |
| Метан +...... | 90,43 | 127,80 | |||
|
Этан +...... |
85,70 | 113,03 |
|||
| Пропан+...... | 84,17 |
109,87 |
Плотность метан С, -|- = 90,43/127,8 = 0,708 г/смs Плотность этан С2 =85,70/1 13,03 = 0,757 г/см3 Плотность пропан С3 = 84,17/109,87 = 0,768 г/см3 Плотность прн 15,5° С н 1 am = 0,708 г/см3 Поправка на давление к плотности прн давлении 112 ата (рис. IV.32) составляет -|-0*(И0> поэтому плотность вместо 0,708 будет 0,718.
По плотности 0,718 и температуре 49* С находим плотность смеси, равную 0,691 (рис. IV.2а),
Таким образом, плотность прн температуре 49е Си давлении 112 ат составляет 0,691 г/см3.
При мечание. Данные взяты из [IV.50].
г75 -50 0 50 100 150 200 250 300 350 Ш
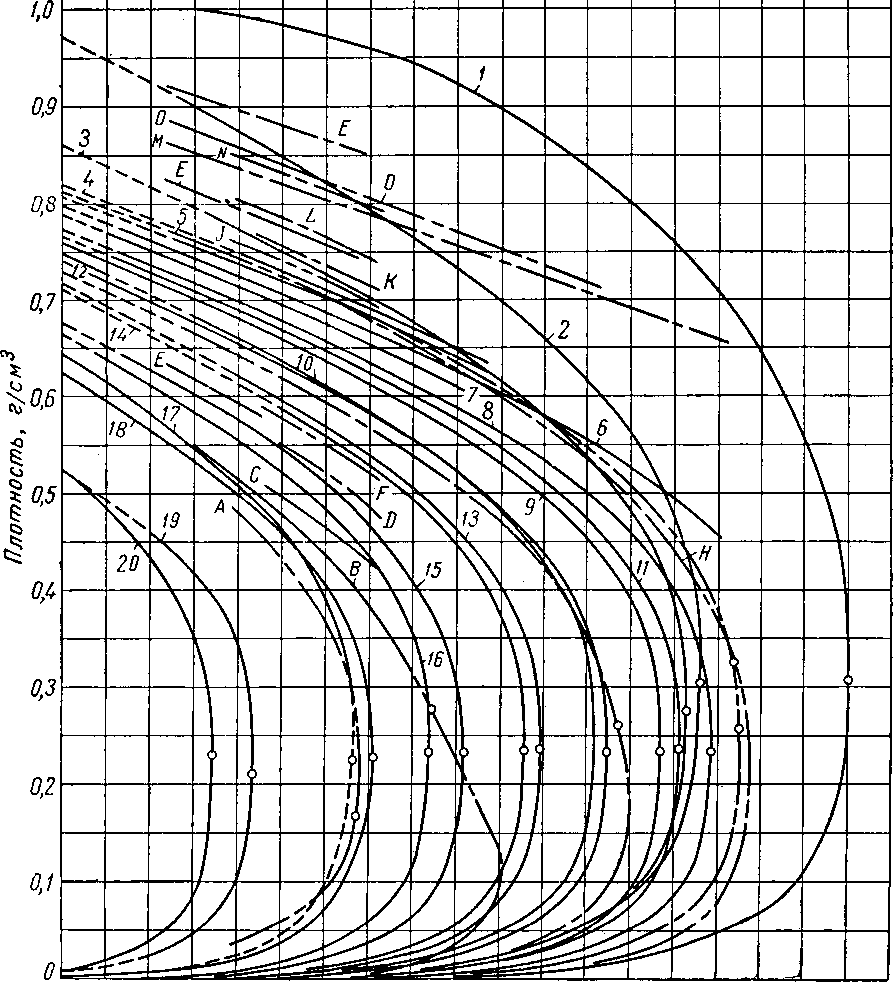
Рис. IV. 29. Ортобарическая плотность жидкостей и паров [I. 2].
А — смесь 8 % мол. СН« и 92% С3Нв при абсолютном давлении, равном 26—52 от; 5 — 50,25 по весу СгНби 49,75% rt=C7Hie; С— 19,2% по весу СН < и 80,8%СвНц при абсолютном давлении, равном 170—175 am; D — 7,15 % по весу СН 4 и 92,85 %«-CeHi2 при абсолютном давлении, равном 60—74; Е — взято из стандартных нефтяных таблиц; F — 7,15% по весу СН4 и 92,85% С8Н18 при абсолютном давлении, равном 210 am; G 9,78 % по весу С*Нв и 90.22 % п-С7Н1б; II — газолин; / — нефть; J — нефть месторождения Конрое переменного состава при 172—-216 ат\ К— 8% по весу газа в нефти месторождения при Л = 5,11%по весу газа в нефти промысла Санта фсСпрингс при абсолютном давлении, равном 148—180; М—веретенное масло из пенсильванской нефти при атмосферном давлении; jV — 4% по весу СН* в бесцветном масле прн абсолютном давлении, равном 136—170; О — оклахомское смазочное масло при атмосферном давлении; Р — кеттлманский конденсат при 38—58 ат; 1 — вода; 2 — бензол; 3 — циклогексан; 4 — додекан; 5-^ундекан; 6»— декан; 7 — нонан; 8— к-октан; 9 — к-гептан; 10 — днизопропил; 11 — днизобутил; 12 — к-гексан; /? «-пентан; 14 — изопентан; 15 — «-бутан; 16 — изобутан; 17прошилеи; 18 пропан; /$ — этан; 20 — этнл’ен.

0,002
150 200
250 300 350 Ш
Температура, °С
Рис. IV. 30. Плотность пропана [I. 2].
Характер влияния давления на плотность жидкости зависит от плотности самой жидкости. При этом, чем меньше плотность жидкости или чем ближе ее температура к критической, тем больше ее сжимаемость. На рис. IV. 32 дана поправка плотности на давление в зависимое™ от плотности жидкости при 15,5° С. Труб [IV.93a] предложил диаграмму для определения сжимаемости пластовых углеводородных жидкостей (рис.
IV. 32с). Значения псевдокритических параметров могут быть взяты из рис. IV. 32а и IV. 32в.
Рис. IV. 31. Кажущаяся плотность метана и этана [IV. 88, I. 2].
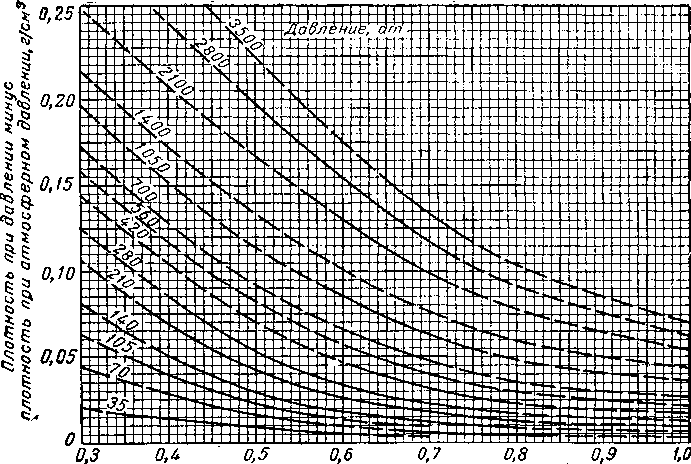
0,5 0,6 0,7 0,8
Плотность при 15,5°С и 1ат,г!см3
Рис. IV, 32. Влияние-давления на плотность жидкостей при температуре 15,5° С
[1.2; IV. 883,
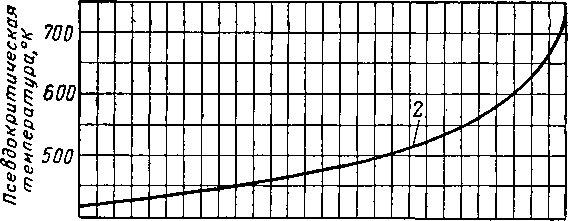
35
|
/ | |||||||||||||||||||||||||||
Ц*® 0,61 0J65 0,70 0,75 0,80 0,85 0,89
25
15
Удельный Вес недонасыщенной лластоВой жидкости при пластовом давлении•, приведенный к 15,5°С
Рис. IV. 32 а. Псевдокритические условия недонасыщенных пластовых жидкостей [IV. 93а].
1 -* псевдокритическое давление; 2 — псевдокритическая температура,,
Абсолютное давление насыщения при. 15,5 °С,
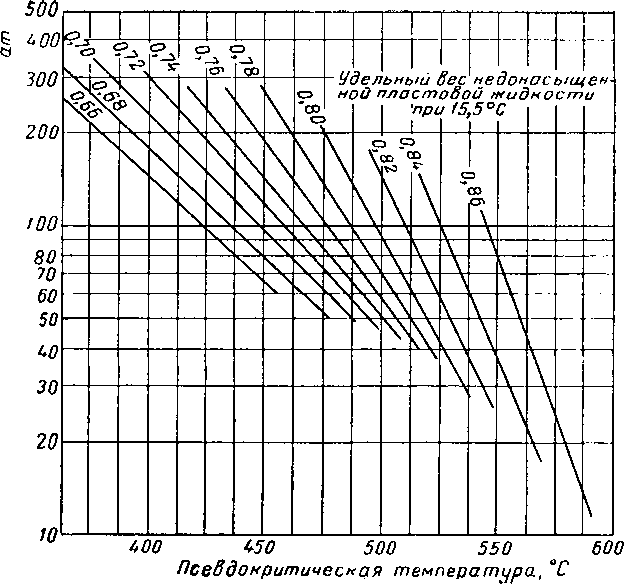
Рис. IV, 32 в. Зависимость псевдокритической температуры от удельного веса и давления насыщения жидкости [IV. 93 а].
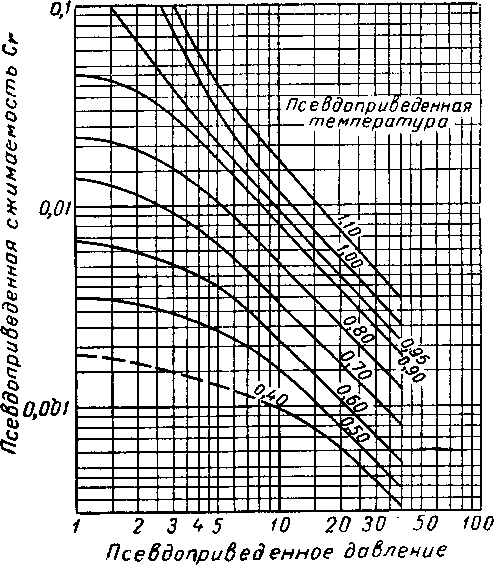
Рис. IV. 32 с. Приведенная сжимаемость для недонасы-щенных пластовых жидкостей [IV. 93 а).
Парциальным объемом компонента называется изменение объема системы при добавлении к ней единицы массы этого компонента. Парциальный объем зависит от температуры, давления и состава фазы [IV. 78], Представляет интерес сравнение парциальных объемов определенных компонентов в смесях разного состава. Олдс, Седж и Леси [IV. 65] представили данные о парциальных объемах к-бутана и н-декана при 137,5° С (рис.
IV.33 и IV. 34) в функции от давления и концентрации бутана в бинарной системе. По этим графикам можно непосредственно (рассчитывать плотность жидкой фазы при 137,5° С.
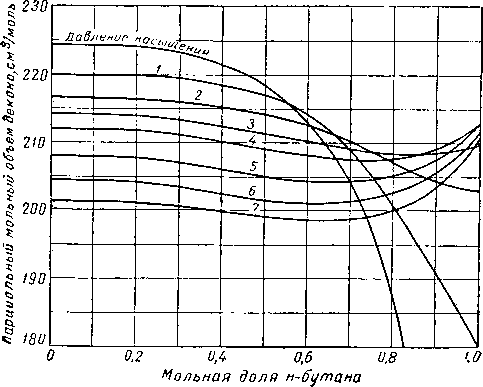
Рис. IV. 33. Парциальный объем декана при 138° С в системе н-бутан-декан [IV. 65]. Давление в ат: 1 — 70;
2 — 140; 3 — 210; 4 — 280; 5 — 420; 6 — 560; 7 — 700.
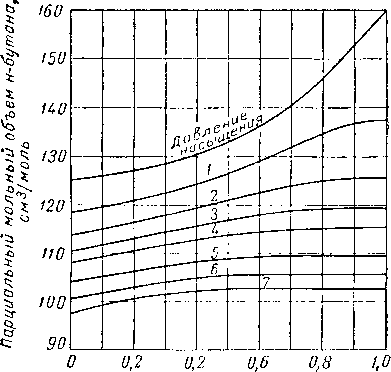
Мольная доля н-бутана
Рис. IV. 34. Парциальный объем н-бутана при 138° С в системе н-бутан — декан [IV. 65]. Давление насыщения в ат: I —70; 2— 140; 3 — 210;
4 — 280; 5 — 420; 6 — 560; 7 — 700.
Рассчитать плотность жидкости, состоящей из 0,463 мольных долей бутана и 0,537 мольных долей декана при давлении 280 ат и температуре 137,5° С (Олдс, Седж и Леси [IV. 65] определили экспериментально для этих условий объем I моль этой смеси равным 165,2 см3/моль).
Решение
Используя парциальные объемы (рис. IV. 33 и IV. 34), находим следующее.
|
Углеводо роды | Моль ная доля | Пар-циальн ый объем при 280 am и 137* С, см3/моль |
Произведение мольная доля* парциальный объем |
| «-Бутан Декан | 0,463 0,537 | 113,3 209,8 | 52,5 112,7 |
| Сумма |
165,2 |
Величина 165,2 точно соответствует экспериментальному значению. Используя кажущиеся плотности ин дивидуальных компонентов с поправками на темпера' туру и давления смеси, находим:
| У глеводо-роды | Моль ная доля | Молеку лярный вес | Моли |
Плотность при 15,5* С г/см3 |
смг/моль |
|
Бутан . | 0,463 |
58 | 26,9 |
0,5844 | 46,1 |
| 77,4 |
105,4 | ||||
|
Декан . | 0,537 |
144 | 107,3 |
0,7341 | 151,5 |
Таким образом, при 15,5° С и атмосферном давлении 104,3
плотность равняется j51-5 = 0,689 г/см3. Поправка на
давление (рис. IV. 32) равна 0,024. Плотность при 15,5° С и давлении 280 ат равна 0,713 г/см3. По этой плотности и по разности температур (рис. IV. 29) находим плотность при 137,5°, равную 0,605 г/см3. Удельный объем 165,2 см3!моль соответствует плотности, рав-104,3
ной i05~2 =г/см3.
Таким образом, плотность жидкости, вычисленная подобным методом, на 4% ниже плотности, полученной экспериментально.
13. ХАРАКТЕРИСТИЧЕСКИЙ ФАКТОР УГЛЕВОДОРОДОВ
Углеводороды, находящиеся в пласте в газообразном состоянии, кипящие до 65°, состоят из метановых углеводородов, а кипящие при более высокой температуре, также и из ароматических и нафтеновых углеводородов. При стандартном анализе таких углеводородных жидкостей определяют пределы кипения, удельные веса и иногда молекулярные веса.
Смит и Ватсон (Smith and Watson) [IV. 86] предложили характеристический фактор углеводородов в следующем виде:
3
0,81618 (-[f + 0,00826) ’ (1V> 25)
где К — характеристический фактор углеводородов; Т — средняя температура кипения в °К; 74 — удельный
вес жидкости при 20° С (берется по отношению к удельному весу воды при 4° С или в г/см3).
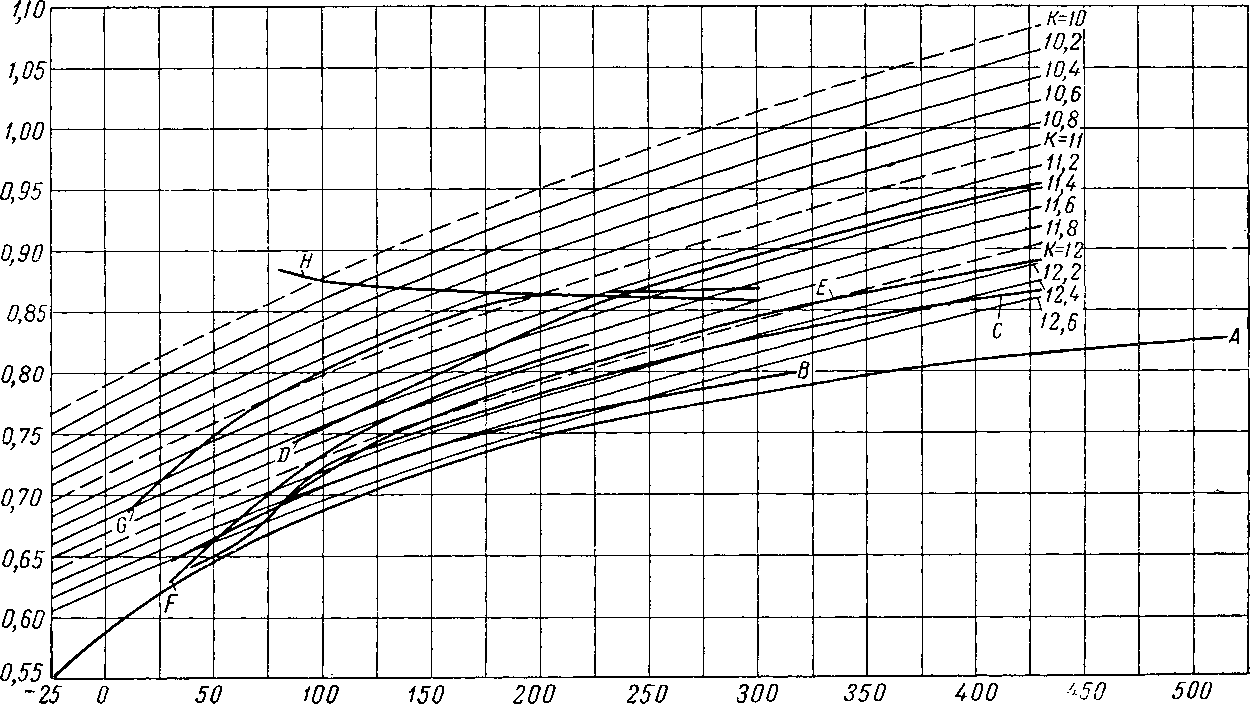
Плотность жидкости при 15,5°С, г/см
Температура кипения при атмосферном давлении, °С
Рис. IV. 35. Зависимость плотности жидкости при 15,5° С от температуры кипения при нормальном атмосферном давлении [I. 2].
А — парафины нормального ряда; В — олефины; С — пенсильванская нефть; D— калифорнийская нефть; ? — оклахомская нефть; ^ — газолин; G — нафтены; Н — ароматические углеводороды с метилышми группами нормального строения в боковом положении депн; /( — характеристический фактор.
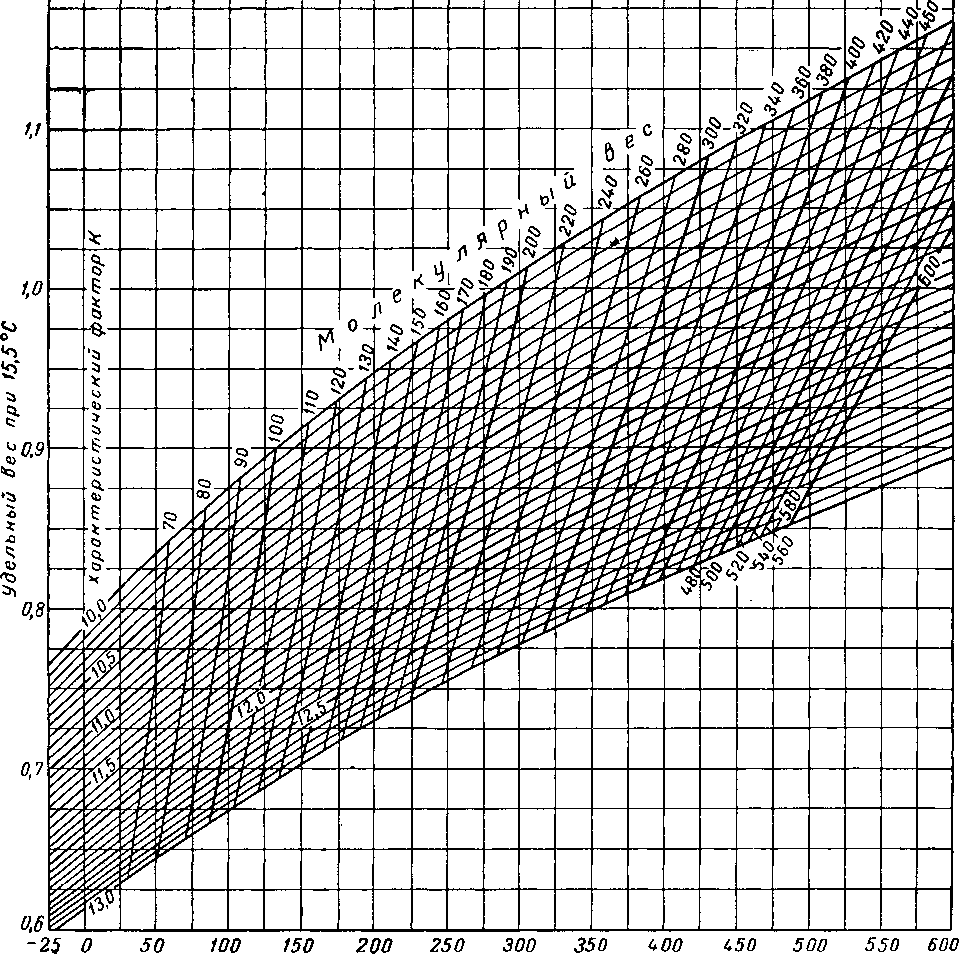
Рис. IV. 36. Соотношение между молекулярным весом, характеристическим фактором, плотностью и темпера
турой кипения [IV. 86, I. 2].
На рис. IV. 35 [1.2] дано соотношение между плотностью и температурой кипения для различных жидкостей, а также проведены линии постоянных значений характеристического фактора К. Диаграмма, представленная на рис. IV. 36, дает соотношение между температурой кипен/ия п,ри нормальном давлении молекулярным весом, удельным весом и коэффициентом К.
В -разделе о капиллярном давлении показано, что неполное вытеснение жидкости из пористой среды вызывается действием капиллярных сил. Наличием поверхностного натяжения объясняются такие явления, как
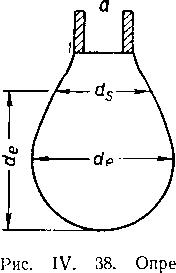
целение поверхностного натяжения методом висячей капли.
Рис. IV. 37. Определение поверхностного натяже- По АА ния методом кольца.
Рис. IV. 39. Поверхностное натяжение углеводородов [IV. 49, IV. 48].
1 — метан; 2 — этан; 3 — пропан; 4 — изобутан; 5 — «-бутан; 6 — м-пен-тан; 7 — «-гексан; 8 — «-гептан; 9 — «-октан.
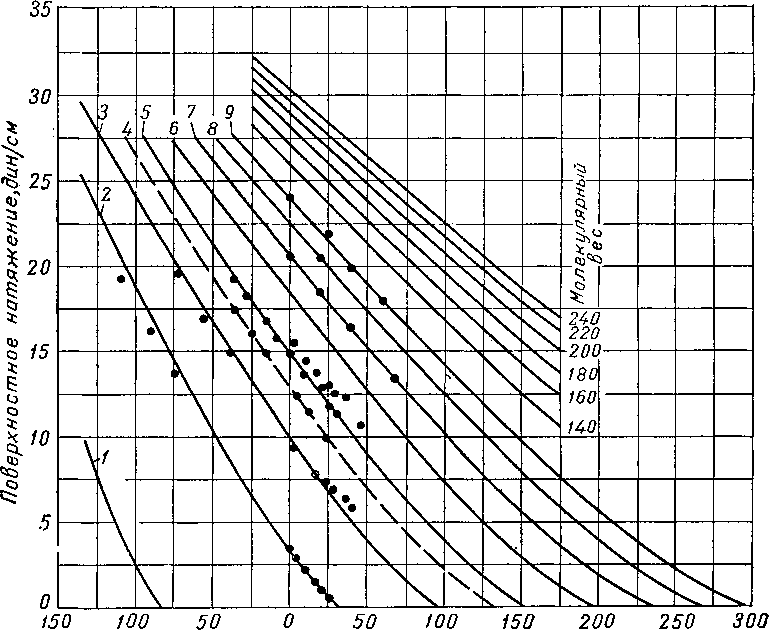
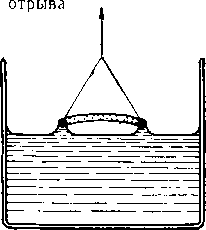
процесс образования пены и характер процесса кипения, когда пар и жидкость находятся в тесном контакте.
Поверхностное натяжение, возникающее на поверхности раздела жидкости и пара, вызывается различием молекулярных сил в паре и в жидкости и отсутствием равновесия этих сил на поверхности раздела.
Из ранних работ по определению поверхностного натяжения пластовых нефтей, содержащих растворенный газ, следует отметить работу Бичера и Паркхарста (Весег and Parkhurst) [IV. 8].
Одним из методов определения поверхностного натяжения является метод отрыва кольца (рис. IV. 37). Сущность этого метода состоит в том, что для отрыва кольца от поверхности раздела двух фаз необходимо приложить силу, п. р опер ц ион а льну ю уд воен ио й длине окружности кольца. Таким образом, поверхностное натяжение выражается как сила, действующая и а единице длины (в дин/см).
Капиллярный метод определения поверхностного натяжения [ом. рис.'II. 38 и формулу (II. 22)] основан на измерении высоты подъема жидкости в капиллярной трубке. Недостатком этого метода является зависимость высоты подъема жидкости от характера смачивания стенок капилляра исследуемой жидкостью. В случае полного смачивания жидкостью поверхности капилляра cos0= 1 и измерения становятся надежными.
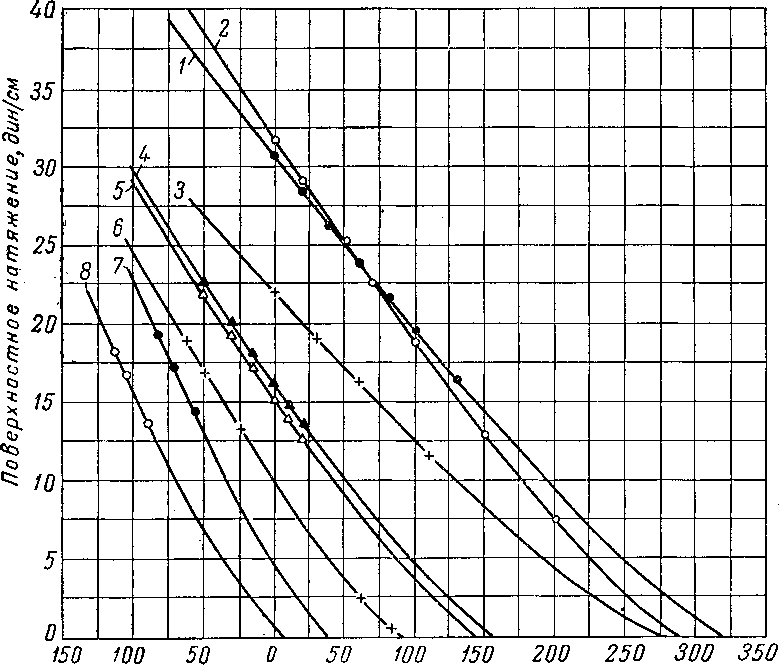
Рис. IV. 40. Поверхностное натяжение углеводородов.
•толуол; 2 — бензол; 3 — диизобутил; 4 — бутен-2; 5 — бутен-1; 6 — нропилен; 7 — ацетилен; 8-
Наиболее предпочтительным методом измерения поверхностного натяжения является метод висячей капли, так как он зависит только от плотности жидкости и размеров капли и не зависит от угла смачивания жидкость!» твердой поверхности (рис. IV. 38). Вся применяемая для этого метода аппаратура может быть помещена в сосуде высокого давления [IV. 36, IV. 44]. Формула для подсчета поверхностного натяжения при измерении по этому методу может быть написана в виде
° = ~Н (Рж-Рг). (IV. 26)
где 0—поверхностное натяжение; de — максимальный диаметр капли (рис. IV. 38); g — ускорение силы тяжести; Н — постоянная величина, являющаяся функцией отношения ds/de, где ds определяется способом, показанным на рис. IV. 38.
— У 2 х
*2
Значения Н, в зависимости от d3/de приведены в работе Фордхена (Fordhan) [IV. 33],
Поверхностное натяжение индивидуальных жидкостей на границе с паром с ростом температуры уменьшается, достигая значения, равного нулю при критической температуре (рис. IV. 39, IV. 40) [IV. 49]. Каждая группа углеводородов имеет свою кривую зависимости (рис. IV. 41) поверхностного натяжения от приведенной температуры [IV. 49].
Вейнауг и Катц (Weinaug and Katz) [IV. 94] исследовали поверхностное натяжение смеси метан—пропан при разных температурах в зависимости от давления (рис. IV. 42). На рис. IV. 43 представлен график, ни котором совмещены диаграмма давление—температура и значения поверхностного натяжения, начиная с по верхностного натяжения, равного нулю на огибающей кривой критических точек.
При давлениях, меньших критических на 14 ат, поверхностное натяжение метан-пропановых смесей составляет менее 0,5 дин/см. Вейнауг и Катц рассчитывали также поверхностное натяжение метан-пропановых смесей, используя значения парахор индивидуальных компонентов по формуле
I
•ч
<b
5:
CD
*
Cj
<ъ
Ci
3:
?
to
СЭ
a:
1
«О
0,2 0,3 OA 0,5 0,6 0,7 0,8
0,9 1,0
Приведенная температура
Рис. IV. 41. Зависимость поверхностного натяжения углеводородов от приведенной температуры [IV. 49].
/•—изопарафины; 2 — нормальные парафины; 3—смеси углеводородов; 4 — бензол; 5 — толуол.
где Рь Р2 —парахоры отдельных -веществ или компонентов в смеси; x\t *2— мольные доли компонентов в жидкой фазе; dm — плотвость жидкой фазы в г/см3\ Мж — молекулярный вес жидкой фазы; у 1, f/2 — мольные доли компонентов в паровой фазе; dn — плотность паровой фазы в г/см3\ Ма — молекулярный вес паровой фазы;
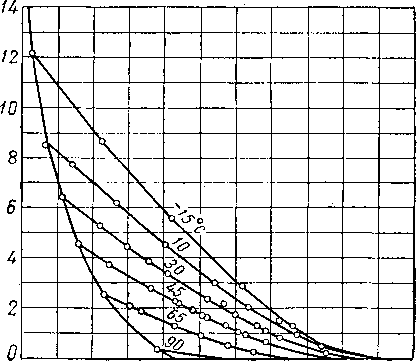
§
*
сь
*
I
3:
о
*
ч
3-
<ъ
<§
о — поверхностное натяжение в дин/см.
Индексы 1, 2, ... обозначают индивидуальные компоненты в смеси.
Значения парахор компонентов или смесей могут быть или определены по структуре молекул 'компонентов, или рассчитаны по значениям поверхностных натяжений индивидуальных веществ при атмосферных условиях.
Значения иaipaхор индивидуальных веществ приведены в табл. IV. 16.
Рис. JV. 42. Поверхностное натяжение в системе метан—пропан [IV. 94].
10 20 30 40 50 60 70 80 90 100 110 Абсолютное да8ление1 ат
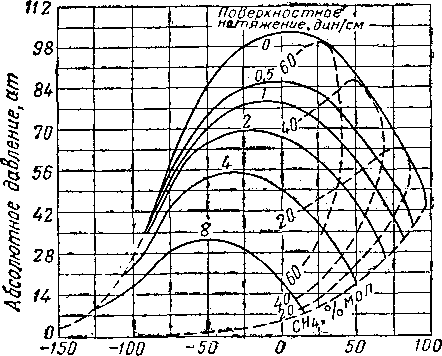
Рис. IV. 43. Поверхностные натяжения системы метан—пропан [IV. 94].
Таблица IV.16 Значения парахор индивидуальных компонентов*
| Компонент |
Парахор | Компонент |
Парахор |
| Метан .... | 77,0 |
«-Гептан . . . | 312,5 |
| Этан..... |
108,0 | «-Октан . . . |
351,5 |
| Пропан .... | 150,3 |
Этилен .... | 100,1 |
| Изобутан . . . |
181,5 | Ацетилен . . . | 88,6 |
| «-Бутан . . . | 189,9 |
Пропилен . . . | 139,9 |
| Изопентан . . |
225,0 | Водород ... |
34(приблизительно) |
| w-Пентан . . . | 231,5 | Азот..... | 41 (прибли |
| зительно) | |||
|
w-Гексан . . . | 271,0 |
* Данные взяты из [IV.94].
Были определены парахоры гептановой и более тяжелых фракций нефти. Эти данные совместно с данными для индивидуальных компонентов приведены на рис. IV. 44.
Метод расчета поверхностного натяжения использовали для равновесных систем нефть—природный газ. Результаты этих расчетов [IV. 48] совместно с данными Шварца (Schwartz) [IV. 81] и Джонеса (Jones) [IV. 47] приведены на рис. IV. 45. Сравнение рассчитанных и экспериментально измеренных значений поверхностного натяжения сырой нефти показывает, что при температуре 48,3° С и давлении 189 ат измеренное значение составляет 1,1 дин/см, а рассчитанное 0,85 дин/см [IV. 50]. В настоящее время можно быть твердо уверенным в том, что углеводородная жидкость, конденсат или нефть, насыщенные природным газом при пластовом
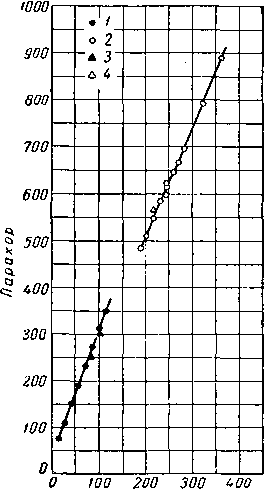
Молекулярный вес
Рис. IV. 44. Парахоры углеводородов [IV. 48].
/ —нормальные парафины: 2 ^ гептаны + L III. 68]; 3 ^ газолины; 4 -* нефть.
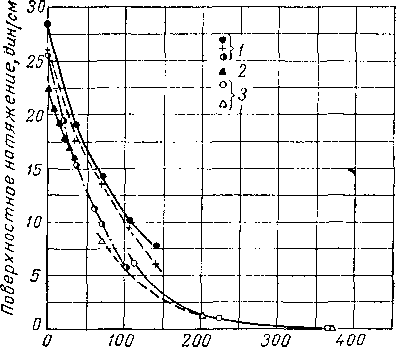
Абсолютное давление насыщ^ния^т
Рис. IV. 45. Поверхностное натяжение нефтей [IV. 48].
/—экспериментальные данные Шварца при 31° С;
2 — экспериментальные данные Джонса при 35° С;
3 — расчетные данные Стендинга и Катца при 49° С.
давлении более 210 ат, будут иметь поверхностное натяжение 2 дин/см или менее. В табл. IV. 17 дается пример расчета поверхностного натяжения по значениям парахор.
Таблица IV.17
Расчет поверхностного натяжения по парахорам
При температуре 30° С и давлении 56,5 am смесь метан — пропан имеет следующие свойства в паровой и жидкой фазах.
I ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ НА ГРАНИЦЕ РАЗДЕЛА ЖИДКОСТЬ — ЖИДКОСТЬ
На границе раздела двух жидких фаз, например вода и нефть или вода и конденсат, наблюдается поверхностное натяжение.
Хаосан, Нильсон и Калхаун (Hassan, Nielsen and Calhoun) [IV. 37] последовали поверхностное натяжение индивидуальных углеводородов на границе с водой в зависимости от температуры и давления. На рис. IV. 47
|
Свойства | Жидкая фаза |
Паровая фаза |
|
Мольная доля метана . . . |
0,255 | 0,672 |
|
Мольная доля пропана . . |
0,745 | 0,328 |
|
Молекулярный вес .... |
36,9 | 25,2 |
|
Плотность, г/см3..... |
0,4200 | 0,0807 |
Значение парахора для метана равно 77, а для пропана 150,3.
„ /0,42 0,0807 \ /0,42
0 U ~ 77 (зб,9 0,255 ~ 25,2 0,672 ) + 150,3 (зад х
0,0807 \
X
0,745_25 2 °>32® ) = Ы76, о = 1,91
дин/см.
Экспериментально (измеренное поверхностное натяжение для этих условий равно 2,14 дин/см [IV. 94].
Поверхностные натяжения для индивидуальных веществ приводятся в таблицах Американского нефтяного института [I. 15]. Поверхностное натяжение смесей веществ было установлено с помощью приведенных поверхностных натяжений [IV. 13].
Поверхностные натяжения воды на границе с природным газом в равновесных условиях получены Хокоттом (Hocott) [IV. 42] и Хугом, Рзаза и Вудом (Hough, Rzasa and Wood) [II. 36]. Данные их экспериментов иллюстрируются рис. IV. 46.
Рис. IV. 46. Зависимость поверхностного натяжения воды на границе с метаном и природным газом от давления [11.36, IV. 42].
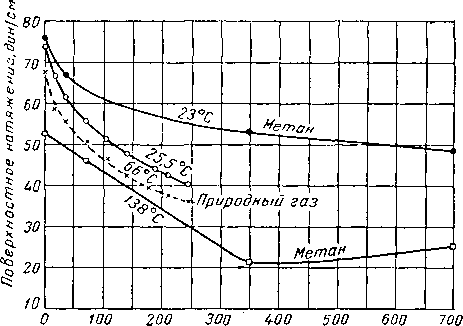
Абсолютное давление , ат
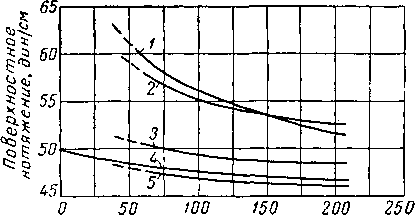
Абсолютное да8ление,ат
Рис. IV. 47. Поверхностное натяжение воды на границе с индивидуальными углеводородами при 49° С [IV. 37].
1 — пропан; 2 — «-бутан; 3 — «-пентан*, 4 — «-гексан; 5 — «-октан.
представлены результаты их опытов, проведенных при температуре 48,8° С. Увеличение давления приводит к уменьшению поверхностного натяжения. Хокотт [IV. 42] исследовал поверхностное натяжение между водой и различными нефтями, насыщенными природным газом (рис. IV. 48). Возрастание поверхностного натяжения с ростом давления в этом случае объясняется увеличением концентрации растворенного газа, т. е. добавлением в систему углеводородов низкого молекулярного веса. После того как давление достигнет давления насыщения, при дальнейшем увеличении уменьшится поверхностное натяжение.
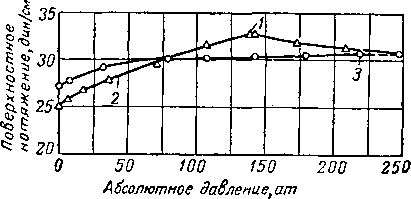
Рис. IV. 48. Поверхностное натяжение воды на границе с нефтями, насыщенными природным газом [IV. 42].
/ — давление насыщения; 2 — нефть Коирое прн 77° С; 3 — нефть Анахуак прн 81° С.
Законы термодинамики широко применяют при определении свойств углеводородов. Например, влияние давления на энтальпию газа может быть рассчитано по данным pVT. Скрытая теплота парообразования может быть определена по наклону кривой упругости пара. Наиболее важными являются следующие свойства: удельная теплота газов и жидкостей, теплота парообразования, влияние давления на энтальпию сжимаемых компонентов. С помощью диаграмм энтальпия — энтропия для природных газов можно определять изменение температуры при расширении газов или обратимую работу при их сжатии.
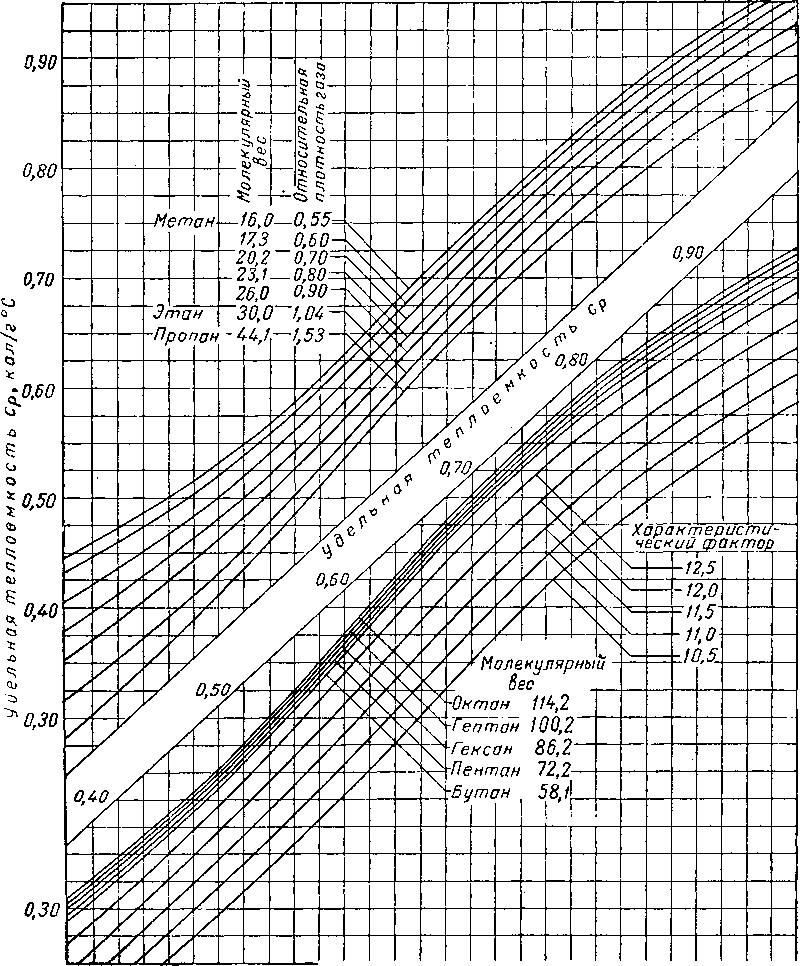
150 200 250 300 350 Ш 450 500 550 600 • Те м п ер а тур а,°С
-100 -50
Рис. IV. 49. Удельная теплоемкость углеводородных газов при атмосферном давлении [IV, 16].
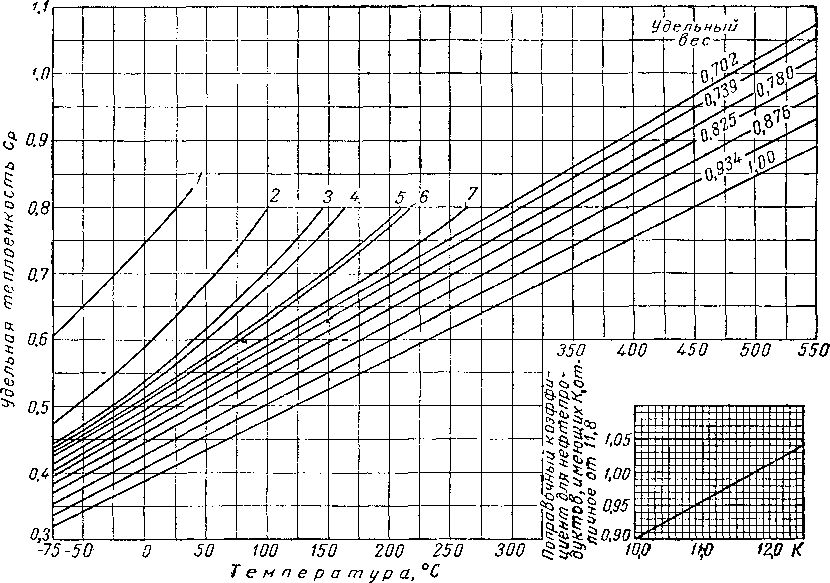
Рис. IV. 50. Удельные теплоемкости углеводородных жидкостей [111.25].
/ — этан; 2 — пропан; 3 — нзобутан; 4—н-бутан; 5 — изопентан; б — н-пентан; 7 — н-гексан.
1. ТЕПЛОЕМКОСТЬ
Свойство вещества, которое позволяет судить о количестве тепла, требующегося для повышения или понижения его температуры, называется его энтальпией-1. Для однофазного состояния вещества изменение энтальпии в зависимости от изменения температуры Т и даз-ления р определяется уравнением
(IV. 28
dp.
i
Влияние на энтальпию только температуры выражается уделыной теплоемкостью при постоянном давлении ср:
[д1\
1 — 1 (IV. 29)
р~\дТ)р Влияние только давления выражается
уравнением
а--
(IV. 30)
¦ объем.
где
( dH \
Для идеальных газов т = 0.
Для реальных га-
' dp I т'
зов изменение энтальпии при изменении давления выражается через коэффициент сжимаемости г:
1дН \ — RT14 [dz \
Удельные теплоемкости газов и жидкостей определяются экспериментально калориметрическим методом, как правило, при атмосферном давлении. Удельные теплоемкости газов и жидкостей, состоящих из несложных молекул, могут быть определены по спектроскопическим данным.
Удельная теплоемкость для природных газов при атмосферном давлении зависит от температуры и от удельного или молекулярного веса газа. На рис. IV. 49 и IV. 50 приведены удельные теплоемкости газов и жидкостей по данным исследований Брауна и Холкомба (Brown and Holcomb) [III. 25, IV. 14, IV. 16]. Удельный вес природного газа используется для определения течения линий удельной теплоемкости паров. При определении удельной теплоемкости паров высококипящих жидкостей требуется знать только характеристический фактор углеводородов [I. 8]. Удельная теплоемкость жидких углеводородов может быть определена по диаграмме, приведенной на рис. IV. 50, для чего необходимо знать его наименование нли удельный Bee-
г. ВЛИЯНИЕ ДАВЛЕНИЯ НА ЭНТАЛЬПИЮ И УДЕЛЬНУЮ ТЕПЛОЕМКОСТЬ
Влияние давления на энтальпию можно найти из закона соответственных состояний. Так как влияние давления определяется при постоянной температуре, то для
—Д/
этой цели удобно пользоваться выражением ft ~Y~•
рис. IV. 51 по данным Брауна [IV. 16] дается зависи--Д/
мость величины - jr от приведенного давления при
различных температурах. Эта диаграмма, применимая для природных газов, построена на основании коэффициентов сжимаемости, взятых из диаграммы рис. IV. 16, Если (^jf^ положительно (что бывает при значении
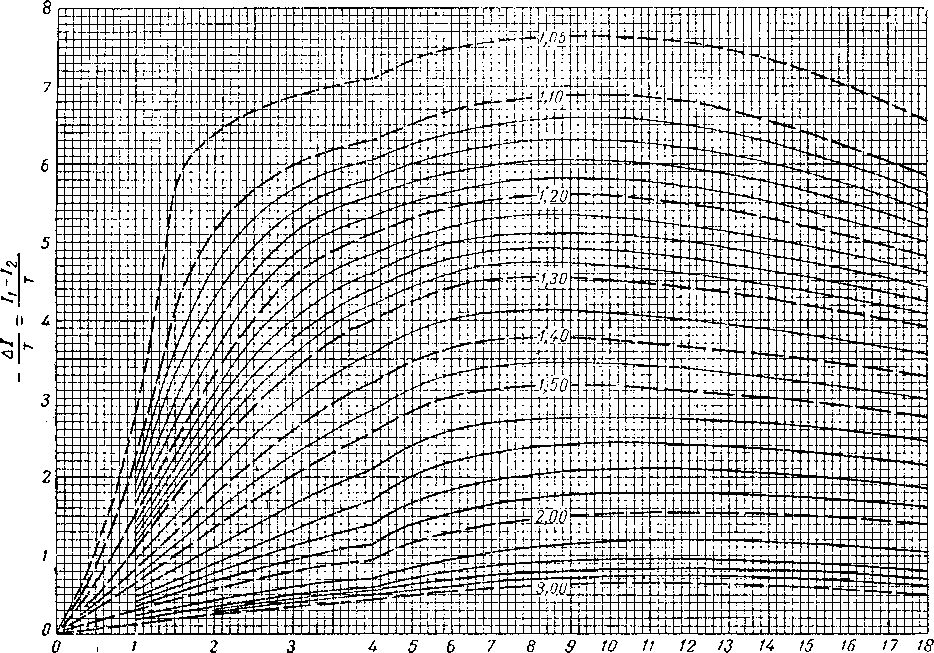
Лсевдоприведе-нное давление рг Рис. IV. 51. Влияние давления на энтальпию природных газов [IV. 16].
приведенного давления от 8 до 10 ат или при абсолютных давлениях до 350 ат), то энтальпия газа уменьшается при сжатии газа и, наоборот, увеличивается при его расширении. Следовательно, положительные значе-
ния величины jr являются энтальпиеи, поглощаемой
при расширении газа, так как 4/ = /2 — h-
Для смесей газов при переходе к приведенным условиям пользуются псевдокритическими давлениями и dz
температурами. Если ^ отрицательно для газов при
высоких давлениях (рис. IV. 16), то при расширении газа температура увеличивается.
Эдмистер (Edmister) [IV. 29] определяет влияние дав-
Д/
ления, используя несколько отличное выражение уг,
в котором вместо действительной температуры берется псевдокритическая (см. диаграмму на рис. IV. 52).
Коэффициент Джоуля—Томсона u. [IV. 91] выражается в виде
Изменение температуры при расширении газа, происходящее при отсутствии передачи тепла или работы, учитывает влияние давления на энтальпию и удельную теплоемкость:
1-) -V \дТ\0
(IV. 32)
Для определения коэффициента Джоуля — Томсона Эдмистером была предложена обобщенная диаграмма [IV. 29]. Седж и Леси определили значение этого коэффициента для 'Некоторых углеводородов. Для метан-пропановых смесей этот коэффициент был определен 6а-денхольцером, Боткином, Седжем, Леси (Badenholzer, Botkin, Sage and Lacey) [IV. 17]. На рис. IV. 53 представлены данные этих авторов для смеси, содержащей 75,52% вес. метана.
Удельная теплоемкость при постоянном давлении для реальных газов зависит от давления *, На рис. IV. 54 приведены кривые зависимости теплоемкости ср от температуры при рааличных значениях давления для смеси, состоящей из 85,4% мол. метана и 14,6% мол. пропана [IV. 17].
0,01 0,02 0,03 0,04 0,06 0,08 0,10 0,2 0,3 0,4 0,6 0,8 1,0 2 3 i 6 8 <0,0
Приведенное давление [Jr
Рис. IV. 52. Влияние давления и температуры на энтальпию природных газов [IV. 29].
Чтобы не составлять многих графиков, подобных этому, отличающихся от газов различной плотности, Эдми-стер [IV. 29] 'представил графики в несколько ином виде, а именно в виде зависимости Д ср от приведенных давления и температуры (рис. IV. 55). Этот график позволяет определять ср при данных давлении и температуре для газов различного удельного веса.
Удельная теплоемкость при постоянном объеме с у связывается с удельной теплоемкостью при постоянном давлении для идеальных газов следующим выражением:
ср = cv -)- R = су + 1,99 [кал/моль • °С].
Отношение удельных теплоемкостей К = — исполь-
зуется при расчетах адиабатического сжатия газов. Для идеальных газов адиабатический процесс записывается в виде
pVK = const.
Значения отношения теплоемкостей К для паров углеводородов приведены на рис. IV. 56, а для индивидуальных углеводородов при атмосферном давлении в табл.
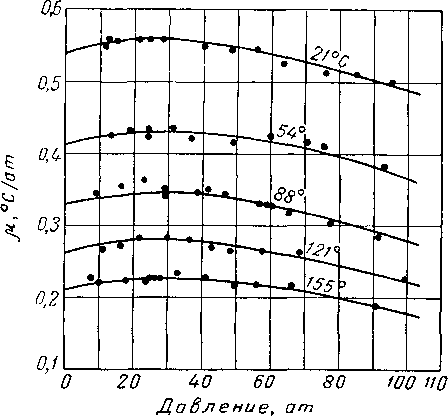
Рис. IV. 53. Значения коэффициентов Джоуля—Томсона для метан-пропановой смеси, содержащей 0,7552 долей по весу (85,4%мол.) метана [IV. 17].
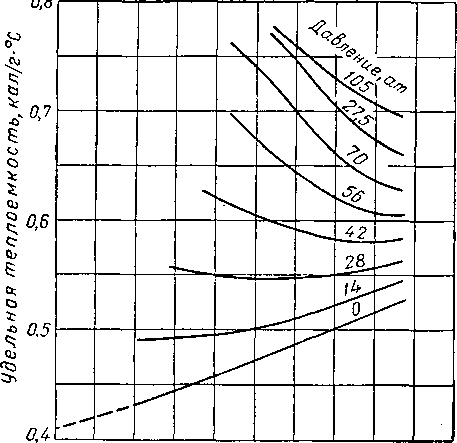
Рис. IV. 54. Теплоемкость при постоянном давлении
для смеси, содержащей
85,4% мол. метана и 14,6% мол. пропана [IV. 17].
20 0 20 40 60 80 100 120 14-0 160 180 Т емпеоатиоа.°С
Н для углеводородов 2,2 2,1 2,0 1,9 1,8 1,7 1,6 1,5 1Л 1,3 1,2 1,1 1,0

О ' 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0 1,1 1,2
Рис. IV. 56. Значения отношения теплоемкостей К для паров углеводородов [IV. 29] (путь определения К показан на диаграмме стрелкой).
1 — метан; 2—-этилен; Зш—этан: 4 — пропилен; 5 — пропан: 6 — изобутилен; 7 — изобутан;
fi — 2-бутен; 9 — к-бутан; 10 — изопентан: // —к-пентан, /2 —бензол; 13 ~~ днизопроггил; 14 — к-гексан; 15 — н-гептан; 16 — диизобутнл и к-октан.
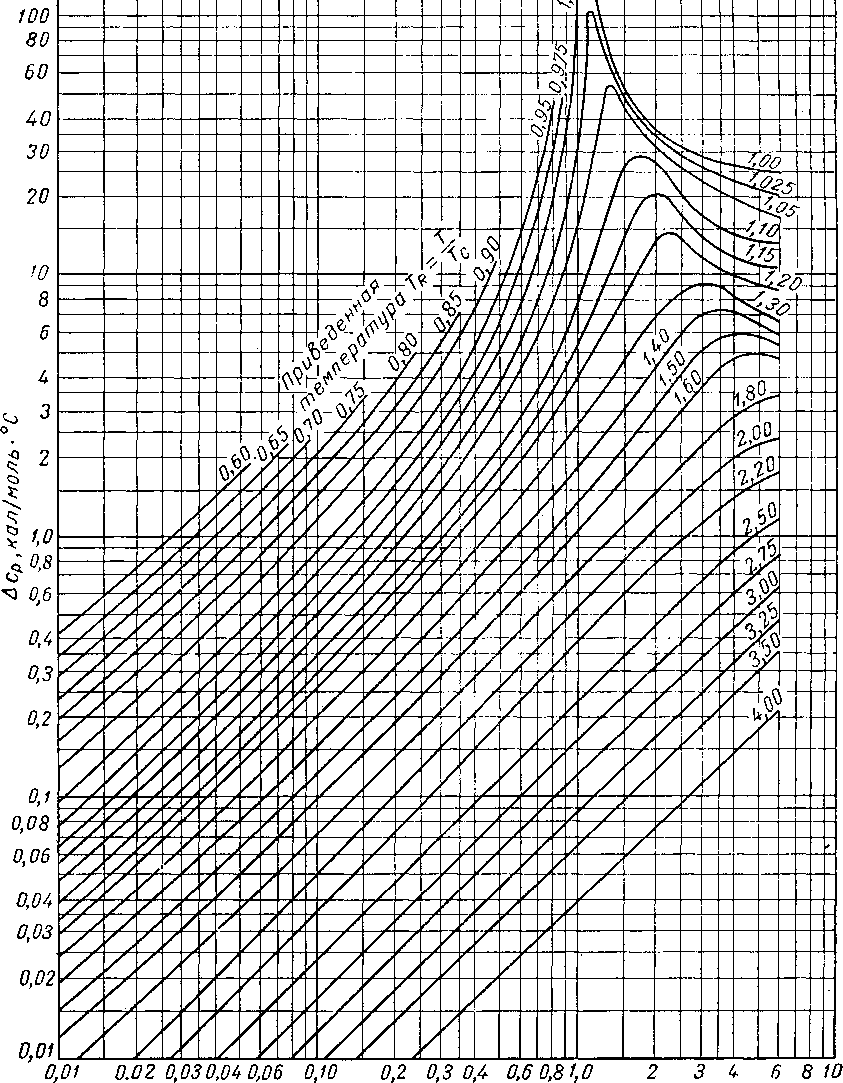
200
Рис. IV. 55. Изотермы зависимостиАсР для паров от приведенного давления (\ср=ср при данном давлении минус сг при атмосферном давлении) [IV. 29].
Скрытая теплота или энтальпия парообразования для чистых веществ — это энерлия, необходимая для испарения единицы вещества при постоянных давлении и температуре. Она связана с кривой упругости пара уравнением Клаузиуса — Клапейрона
dp Д/ AS
df = TAV = ДУ > (]V- 33)
где ^ — наклон кривой упругости пара; Д/ —скрытая теплота парообразования, приращение энтальпии при изменении фазового состояния; Т — абсолютная температура; ДК — приращение объема при парообразовании; AS — приращение энтропии при парообразовании.
Юнг (Young) [IV. 97] вычислил значения скрытой теплоты парообразования для тридцати чистых веществ, для которых им были получены значения упругости пара и плотности фаз.
1
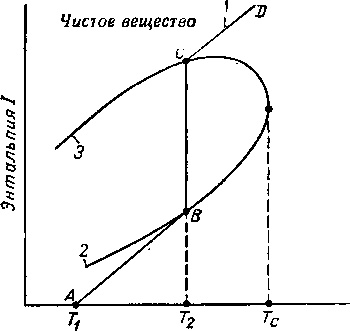
Температура
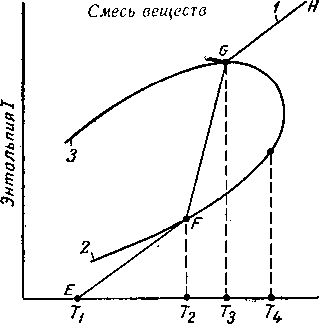
Рис. IV. 57. Увеличение энтальпии в процессе парообразования.
1 — постоянное давление: 2 —
насыщенная жидкость: 3— на
сыщенный пар.
Температура
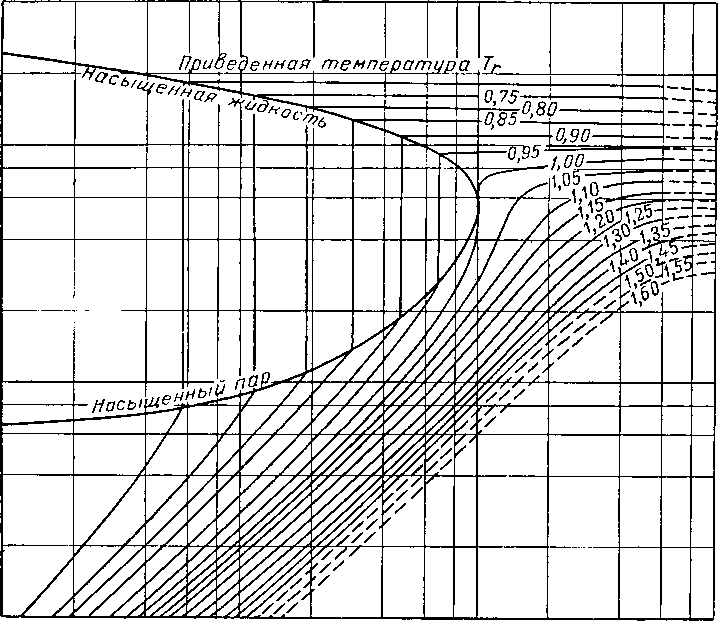
20
10
6
4
0,01 0,02 ОМ 0,06 0,1 0,2 0,4- 0,6 1 2 4 6 10
Рис. IV. 58. Зависимость энтальпии пентана от температуры и давления [IV. 56].
Температура,°С 150 100 50 О
Рис. IV. 59. Скрытая теплота испарения индивидуальных веществ [III. 25J.
1 — н-додекан: 2 — «-ундекан; 3 — к-декан; 4 — м-нонан; 5 —«-октан: б —«-гептан;
^ — «-гексан: 8 — «-пентан; 9 — изопентан; 10 — «-бутан; 11 — изобутан; 12 — пропан; 13 — пропилен; 14 — циклогексан; 15 — 1,3-бутадиен; /6 —бензол; 17 — метан; 18 — этилен; 19 — этан..
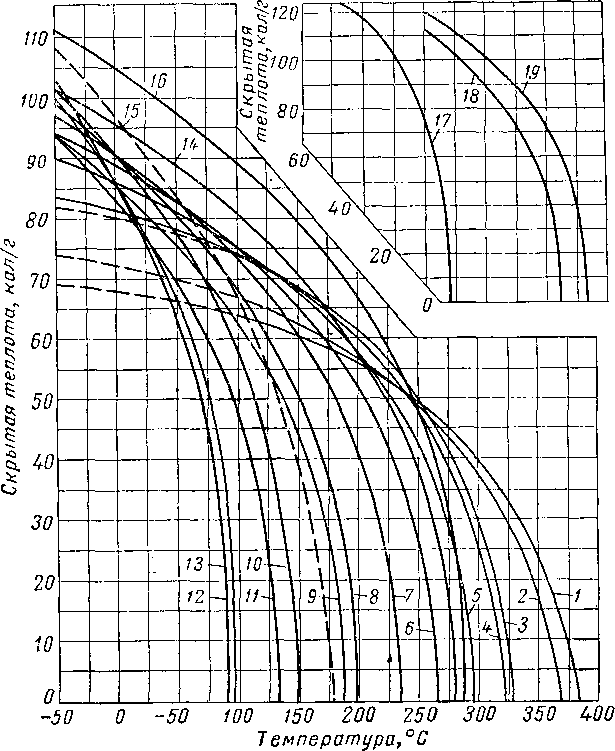
Графики на рис. IV. 57 иллюстрируют увеличение энтальпии вещества при его нагревании. Для чистого вещества это увеличение энтальпии происходит по линии ABCD. Отрезок АВ соответствует затратам тепла на нагревание жидкости, отрезок ВС — затратам подводимого тепла на перевод жидкости в пар (скрытая теплота) и отрезок CD —на нагревание пара. Количество тепла, необходимое для нагревания жидкости или газа, определяется по отдельным теплоемкостям соответствующих фаз. Скрытая теплота относится к той температуре Т>, при которой рассматриваемое давление равно давлению насыщенного пара.
В критической точке скрытая теплота обращается в нуль, так как при более высоких температурах уже не происходит изменения фазового состояния вещества. На рис. IV. 58 приведены данные Конца и Брауна [IV. 56],
Д/
показывающие зависимость величины ¦уг- от давления
и температуры для пентана. Из этого графика видно, что уменьшение скрытой теплоты парообразования и обращение ее в нуль сопровождаются резким изменением Д/
величины для вещества, находящегося в однофазном состоянии, что по существу возмещает отсутствие
Д/
скрытой теплоты. Величина ~jr Для скрытой теплоты
эквивалентна приращению энтропии при парообразовании AS.
Для смесей процесс парообразования не происходит при постоянных температуре и давлении (рис. IV. 57). Интервал температур от Гг до Г3 соответствует пределам температуры кипения смеси. При переходе из точки F в точку G тепло затрачивается не только на парообразование, но также и на повышение температуры смеси. В этих условиях очень трудно определить точное значение скрытой теплоты парообразования. Необходимо также указать, что в этом случае возможно существование жидкой фазы и при температуре, превышающей критическую температуру Т4-
На рис. IV. 59 представлены кривые зависимости скрытой теплоты парообразования от температуры для индивидуальных углеводородов [III. 25], а на рис. IV. 60 дана зависимость молярной энтропии парообразования индивидуальных углеводородов от приведенной температуры [IV, 29].
Рис. IV. 60. Мольная энтропия парообразования углеводородов [111.29].
/ —«-октан; 2 -«-гептан и диизобутил; 3 — «-гексан; 4 — изопентан и «-пентан и диизопропил; 5 — бензол, циклогексан и бутены; 6 — изобутан и «-бутан; 7 — пропилен; 8 — пропан; 9 — этилен; 10 — этан; 11 — метан.
Весьма распространенными являются диаграммы, выражающие зависимость энтальпии от энтропии, давления или температуры. Большое применение для решения задач течения пара получила диаграмма Молье энтальпия— энтропия. Свободное расширение пара, например, при истечении через дроссель происходит при постоянной энтальпии, Д/ = 0. Адиабатическое обратимое расширение и сжатие происходят при постоянной энтропии 45 = 0.
Браун (Brown) [IV. 16] построил диаграммы энтальпия— энтропия природных газов, используя значения удельных теплоемкостей (по графику рис. IV. 49), зна-Д/
чения отношения -jr (из рис. IV. 51) и значения отношения f/p (из рис. VIII. 29). pVT—соотношения были взяты из диаграммы рис. IV. 16.
На рис. IV. 61 даны изотермы приращения энтропии природных газов. Диаграммы энтальпия — энтропия для природных газов удельного веса 0,6, 0,7 и 0,8 (по воздуху) приведены соответственно на рис. IV. 62, IV. 63 и IV. 64. Значения псевдокритической температуры и давления, приведенные на этих диаграммах, соответствуют в основном углеводородным газам. Удельные веса газов приняты при 0° С и атмосферном давлении. На рис. IV. 65 приведена диаграмма для газон удельного Reca 0,7 содержащего 10% мол. азота. Псевдокритические условия
Д/
взяты для указанной смеси, но для у и Д5 были
использованы диаграммы для углеводородных газов. Приведенные диаграммы можно использовать для определения изменения температуры газов при их расширении и сжатии, а также для определения обратимой работы расширения или сжатия.
Пример.
Ежесуточно через дроссель происходит истечение 1,026 млн/м3 (приведенных к температуре 15,5° С и давлению I атм) природного газа при температуре 60° С; удельный вес газа 0,6. При этом давление падает с 56 до 28 ат.

1 2 3 4 5 6
ПсеВдоприВеденное давление рг
-As = (sf-s2) -as=Csf-sz)
dS, кал/моль • °С-
| . | |||||||||
|
- | ~ |
-4 | -- | ||||||
| * |
|||||||||
|
:г: | ; | ||||||||
| -У | |||||||||
| -Jf- | |||||||||
| 7 |
0,02 0,03 0,0 U
Атмосферное давление Псевдокритическое давление
LO
ЬООО
1500
3000
2500
2000
1500
1000
500
-500
- <000
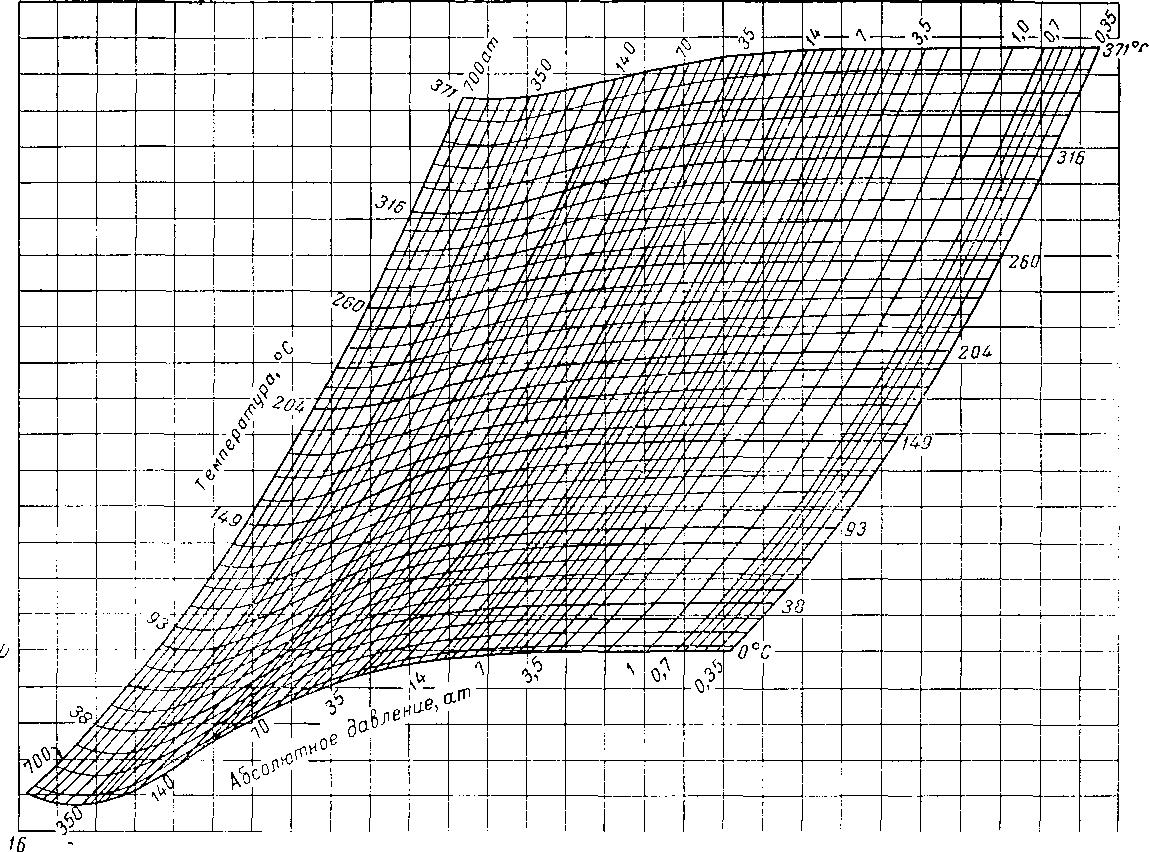
¦14 -12 -10
-8 ~6 -4 -2 0 2 4 6 8 Ю
Энтропия, нал/моль ¦ °С
Рис, IV. 62. Диаграмма энтальпия—энтропия для природного газа удельного веса 0,6 [IV. 16]. (Псевдокритическое давление 48
псевдокритическая температура 200° К)
Энтальпия, кал/моль
ат,
-16 -14 42 -10 -8 -6 -4 ~2 0 2

Энтальпия, кал/моль
4500
Рис, IV. 63, Диаграмма энтальпия—энтропия для природного газа удельного веса 0,7 [IV. 16]. (Абсолютное псевдокритическое давление
4,6,7 ат, псевдокритическая температура 218°К).
SSODr
5000
<*300
ШО
3500
3000
•о
*2500
§
*2000
i
? 1500 «
500
О
-500 -iOOO
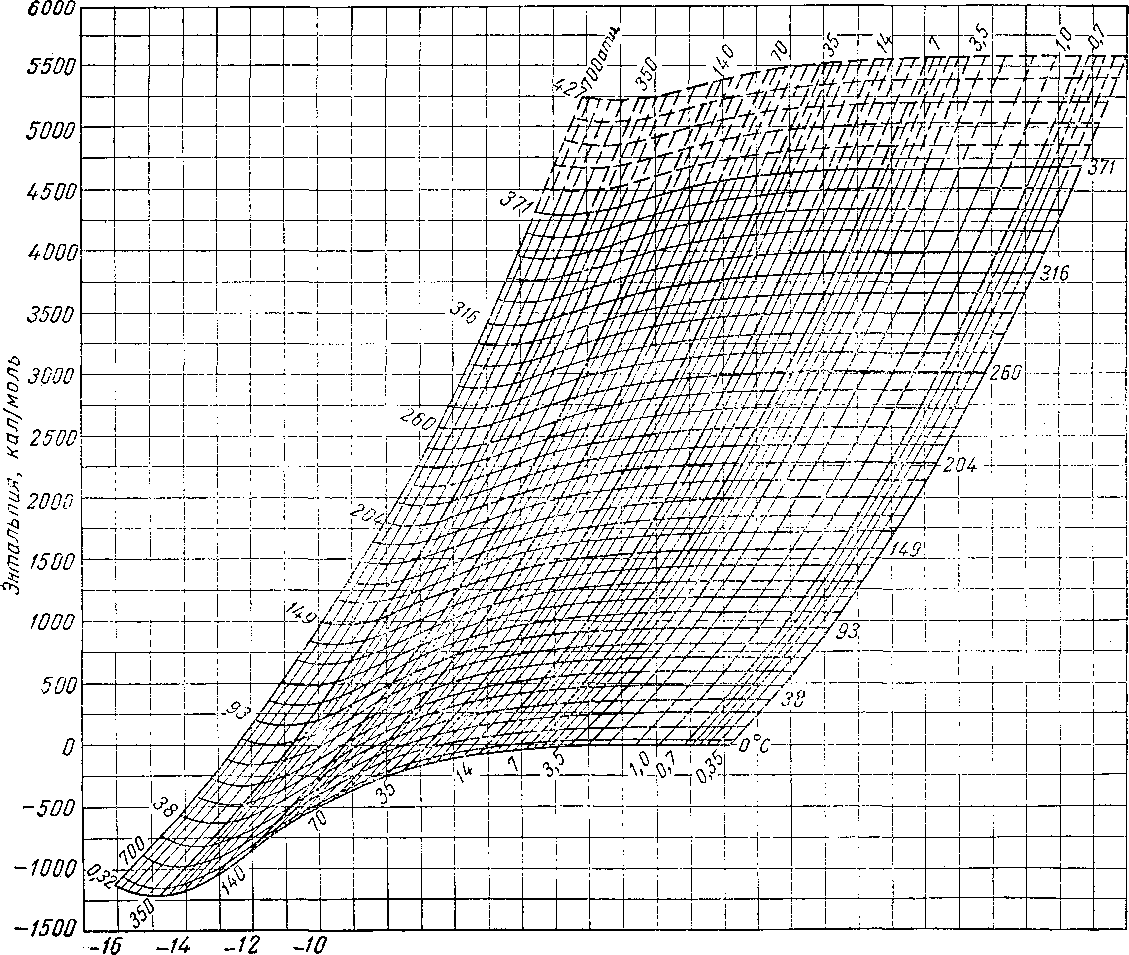
8 -6 -4 ~2 0 2 4- 6 8 10 12 14-
65. Диаграмма энтальиия—энтропия для газа удельного веса 0,7, содержащего 10% азота [IV, 16]. (Пеевдокритиче-ское давление 45,9 ат, исевдокритическая температура 280°К).
ютное дайление ,
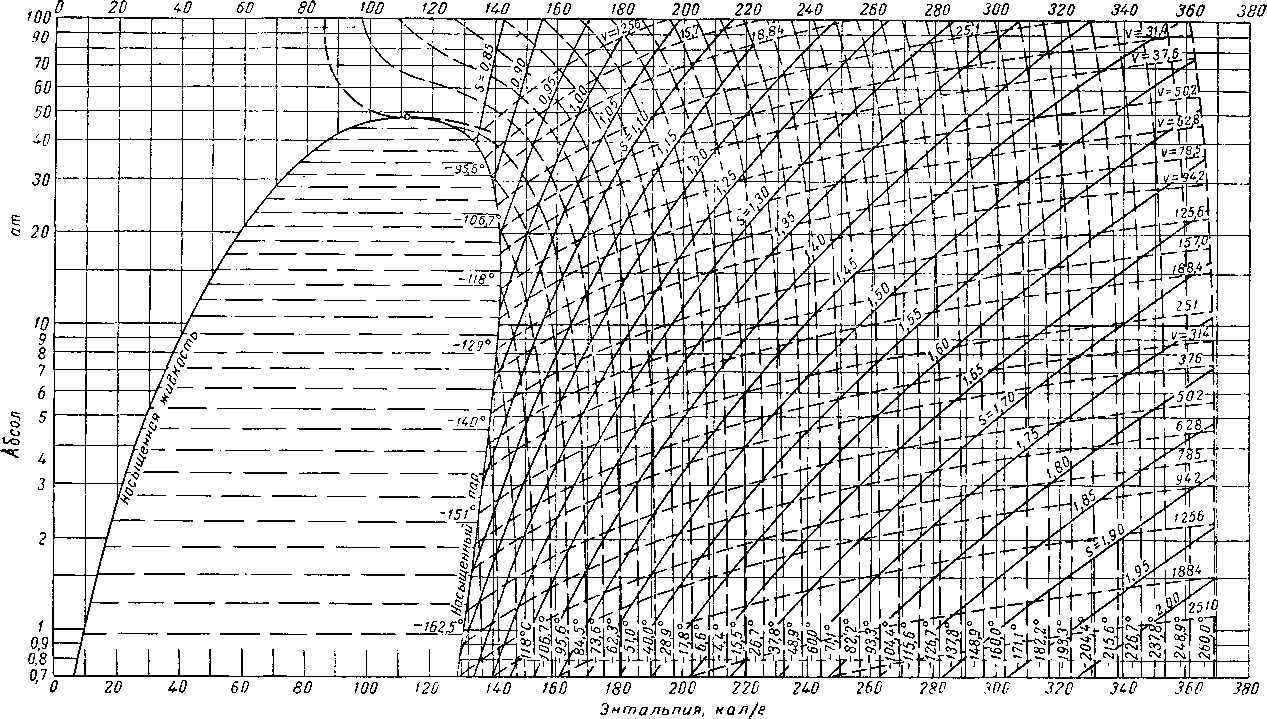
Рис. IV. 66. Диаграмма давление — энтальпия для метана [111. 42J. (Для насыщенной жидкости при —173,5° С энтальпия и энтропия равны
нулю).
V — удельный объем и см*/г, S — энтропия в кал/г • °К
Абсолютное да&лени.е,ат

Абсолютное да&ление, ат
200 220 2ЬО
Энтальпия, кал/г
Рис. IV. 67. Диаграмма давление — энтальпия для этана [IV. 6].
смъ1г\ S *=- энтропия в кал/s»9 К; Г— температура в °С; / «О, ?«0 для твердого тела при 0° К.
V —¦ удельный объем
СП
ЙЗсолютное давление t am
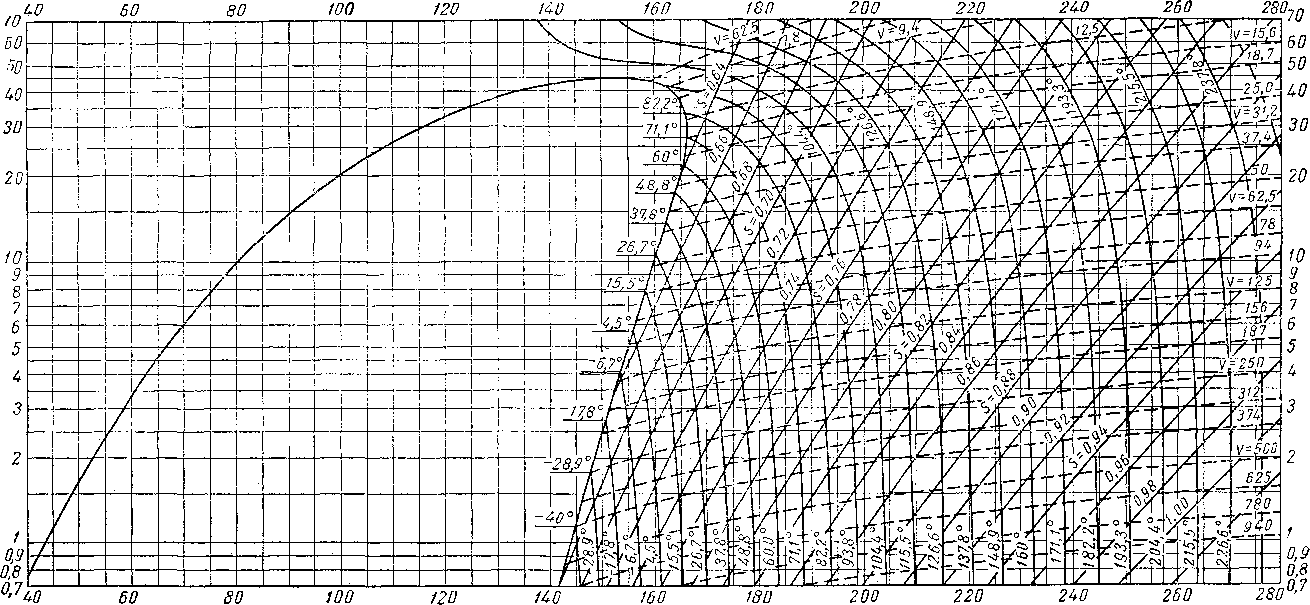
Абсолютное давление
Энтальпия, кал/г
Рис. IV. 68. Диаграмма давление — энтальпия для пропана. (Для насыщенной жидкости при — 129° С энтальпия и энтропия’равны нулю).
V — удельный объем в см>1г\ S — энтропия в кал/г-°К', Т — температура в °С.
Абсолютное давление,
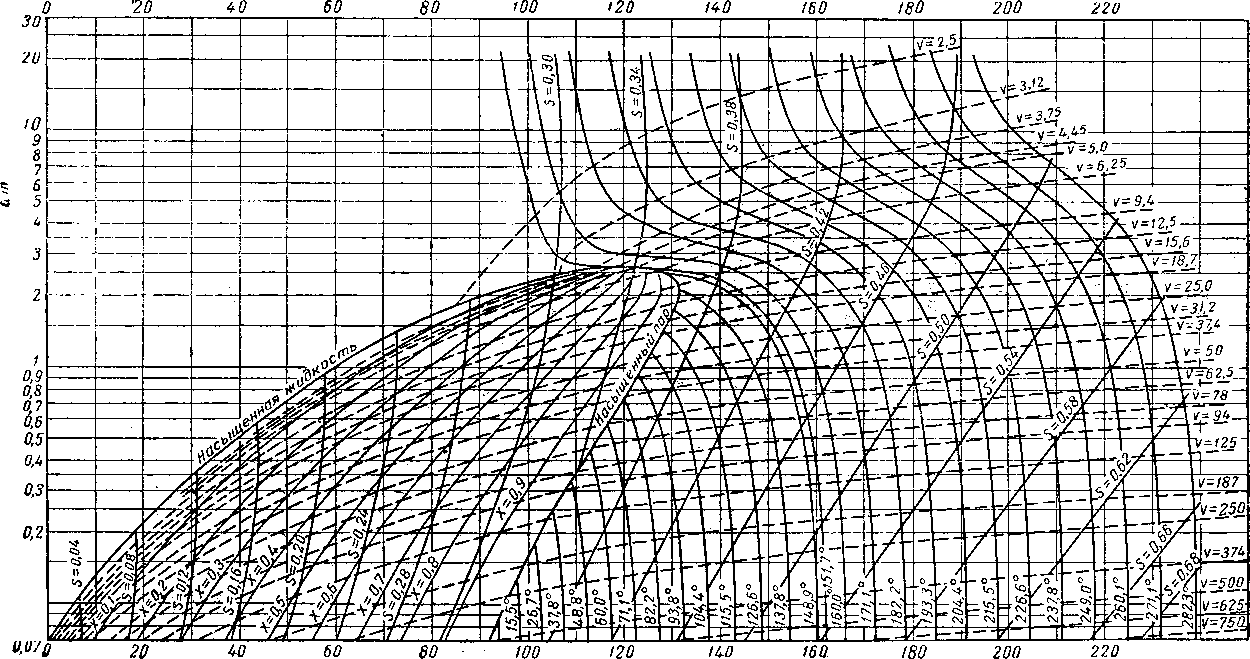
80 ЮО 120 li-0 160 180
Энтальпия, кал]г
Рис. IV. 69. Диаграмма давление — энтальпия для «-бутана [IV. 71].
Г — температура в °С; If— 0 hS^M) при атмосферном давлении и сухости 0° С.
24-0 250
D.I
0,69
О,OS
со
-~4
‘s
энтальпия
(VI. 34)
I в этой энтальпия
вещества
dT
Определить.
1. Изменение температуры газа при истечении.
2. Макаимальную работу, которая будет получена при расширении газа без использования тепла.
3. Изменение температуры газа при его обратимом адиабатическом расширении.
Решение
Из рис. IV. 62 находим:
1) при давлении 56 ат и 60° С / = 342 кал/г ¦ моль;
при давлении 28 ат и / = 342 температура равна
49° С;
2) при 56 ат и 60° С 5 = —6,55 кал/г-°С, при 28 аТ и 5 = —6,55 температура 10° С, а / = —44 кал)г -моль. Тогда —А/ =/]—/2 = 342 — (—44) = 386 кал/моль.
Таким образом, работа равна—Д/ = 386 кал/моль;
1 л. с. — 637 ккал/ч.
1026000x386
Мощность = 23J5X 24x637" = 1089 л• с" где 23,76 — объем 1 моль газа при атмосферном давлении и 15,5° С (см. табл. IV. I).
Изменение температуры пара при его расширении, кроме того, представлено диаграммами (рис. V. 48, V. 49 и V. 50) в связи с определением условий гидратообразован и я.
Диаграмма давление — энтальпия для метана была получена Меттьюзом и Хардом (Matthews and Hurd) [111.42], для этана — Барклью, Валентином и Хардом (Barkellw, Valentine and Hurd) [IV. 6], для пропана — исследователями компании Шелл дивелопмент и для бутана Принглом, Гринхаузом и Йорком (Prengle, Greenhaus and York) [IV. 71] (рис. IV. 66—IV. 69). Из этих рисунков видно, что эти диаграммы являются различными для разных газов. На этих диаграммах нанесены линии постоянной энтропии 5, объема V и температуры. С помощью этих диаграмм может быть быстро решена задача о течении газа при постоянном значении / или при постоянном значении 5.
Диаграммы энтальпия — температура для индивидуальных веществ были получены Эдмистером (Edmis-ter) [IV. 29], Максвеллом (Maxwell) [I. 10] и другими. Эта диаграмма дает соотношение энтальпия — температура — давление для чистых веществ, а также может быть использована для смесей этих веществ.
Пример
Определить, сколько выделится тепла. При переводе 28 500 нм?/ч метана при давлении 70 ат и температуре 38° С в насыщенную жидкость при давлении 1,75 ат.
Решение
Из рис. IV. 66 при 70 ат и 38° С / = 218 кал/г. При давлении 1,75 ат температура равна 155° С, а / = = 14 кал/г. Удельный расход тепла равен — 4/ = — q = = 218 — 14 = 204 кал/г. Отсюда общее количество вы-28300
делившегося тепла 23
75 16 X 204 = 3,9 X 106
ккал/ч, где 16—-молекулярный вес
метана.
5. ЭНТАЛЬПИЯ СМЕСЕЙ
Рис. IV. 57 иллюстрирует более сложную задачу определения скрытой теплоты парообразования смеси, так как температура в процессе испарения изменяется. На рис. IV. 70 приведены данные Фикала и Брауна (Fekula and Brown) для смеси лигроина с газолином удельного веса 0,72. Сложность определения теплоты парообразования смеси заключается также и в том, что жидкости часто содержат растворенные газы при температурах выше нх критических температур. Энтальпия одного компонента зависит от других компонентов смеси и от его концентрации. Поэтому для оценки энтальпии смеси существуют только приближенные методы [IV. 51].
системе; ni системы.
Для иллюстрации зависимости парциальной энтальпии вещества от состава смеси и от его концентрации на рис. IV. 70а приведена парциальная энтальпия метана в трех бинарных смесях по данным Седжа, Олдса и Леси [IV. 79].
Миллер (Miller) измерил теплоту растворения бутана в растворителе при температуре выше и ниже критической температуры бутана (рис. IV. 71), Теплота растворения зависит от концентрации бутана. Кривая зависимости теплоты растворения от температуры, соответствующая постоянной концентрации, представляет собой плавную кривую, проходящую через критическую температуру для бутана.
Пытались рассчитать парциальные энтальпии [IV. 19, IV. 70] легких углеводородов, но законченной системы расчета значений энтальпий не удалось создать. Поэтому данные по соотношению энергий при переходе вещества из одного фазового состояния в другое могут быть очень ценными.
Существуют два метода определения энтальпии смесей. По первому методу (методу Холкомба и Брауна [III. 25] предполагается, что влияние концентрации не учитывается. Второй метод основан на использовании диаграмм Петерса (Peters) [IV. 67] и Максвелла (Maxwell) [I. 10] для энтальпий индивидуальных компонентов, из которых составлена смесь. Энтальпия смеси рассчитывается по энтальпиям составляющих ее компонентов.
Холкомб и Браун за исходную выбрали точку, в которой давление и температура °С равны нулю. Энтальпии жидкостей, находящихся при температуре выше нуля (при давлении, равном нулю), представлены на рис. IV. 72. Диаграмма построена на основании удельных тепл от (см. рис. IV. 50) и сопоставления зависимости значений энтальпий от температур кипения при атмосферном давлении [III. 25]. Энтальпия смеои определяется путем суммирования энтальпий компонентов, пропорционально их концентрациям. Поправка энтальпии на давление определяется по диаграмме рис. IV. 73 на основании данных удельного веса жидкости, температуры и давления.
Для газов основным соотношением являете^ превышение энтальпии его при 0° С и атмосферном давлении над энтальпией жидкости при температуре (°С) и давлении, равных нулю (рис. IV. 74). Эта диаграмма построена с учетом величины 4/, затрачиваемой на испарение, рассчитываемой по константам равновесия с помощью уравнения Ван-Гоффа
d(ln/^ (IV. 35)
Влияние температуры определяется по удельной теплоемкости пара (рис. IV. 49), а влияние давления
определяется по значениям —- ~ (рис. IV. 51).
Пример
100 моль смеси, состоящей из 63,7% мол. метана и 36,3% мол. я-бутана, находятся в однофазном состоянии при температуре 121° С и давлении 141 ат. Смесь пропускается через теплообменник и попадает в сепаратор с температурой 21° С и давлением 28 ат, где из нее отбирается 67 мол. пара (88,3% мол. метана) и 33 моль жидкости (13,8% мол. метана).
-концентрация вещества /; h
где /1—-парциальная
RJ2 •
Парциальная энтальпия вещества 1\ определяется как изменение энтальпии системы при добавлении единицы вещества /:
д!
h
240

260
'220
200
/80
6
а
- /60 <У
з
| /40 a
"=> /20 Qi
а
1 100 S
1 80 <c
60
40
20
Рис. IV. 70. Энтальпия смеси газолина и керосина удельного Беса 0,72, отнесенная к 0° С и атмосферному
давлению.
Вычислить теплоту, выделяемую в теплообменнике.
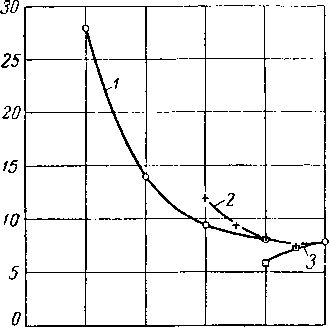
Решение
Пользуясь диаграммой Холкомба и Брауна, находим энтальпию системы при 121° С и 141 аг, а также энтальпию паровой и жидкой фаз в сепараторе при температуре 21° С и абсолютном давлении 28 ат. Разность этих величин дает тепло, выделяющееся в теплообменнике.
Расчет псевдокритических свойств для системы до теплообменника и для паровой фазы в сепараторе, а также плотности углеводородной жидкости в сепараторе следующий.
|
Углеводо роды |
Критическая температура Тс% *к | Критическое абсолютное давление Рс, am |
Система до теплообменника | Пар в сепараторе |
||||
| молярная доля р |
псевдо-крнтн-ческая температура Рт с | Я щ Ю ^ ago, М О. О 4> Йо«1 m “ а> о х и а> и с s* ч |
молярная до*1 ля р |
псевдо- крити ческая темпе ратура Ртс | псевдо- крнти- ческое давле ние рРс |
|||
| Метан . н-Бутан |
190 425 |
47,3 38,7 |
0,637 0,363 | 121 154 | 30,2 14,0 | 0,883 0,117 |
168 49,7 |
41,7 4,5 |
|
275 | 44,2 |
217,7 | 46,2 |
|||||
!
'О
§
53
#
весовое содержание иетана
Рис. IV. 70а. Парциальная энтальпия метана в газовых смесях [IV. 79].
1 — система метан—этан; 2 — система метан— бутан; 3 — система метан—пентан.
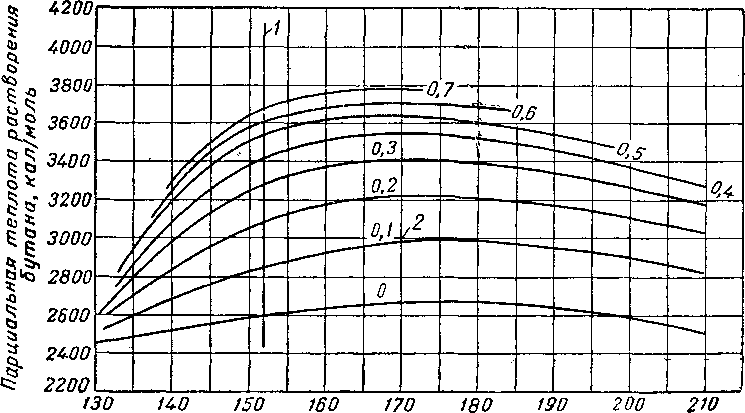
Рис. IV. 71. Парциальная теплота растворения н-бутана при 28 ат в растворителе с молекулярным весом 145 [IV. 51].
I_критическая температура чистого бутана; 2 — число молей бутана в жидкости на моль рас
творителя.
Температура, °С
Приведенные температура и давление: для оистемы до теплообменника
45700 кал 120300 кал
394 141
Тг = Ш> = I’43’ Рг = 4^2 = 3,18;
для пара в сепараторе
Жидкость в сепараторе:
294 28
ТГ = 2177? = ь35, Рг = 46^ = 0,607'
|
Углеводороды | Плотность, г/см• | % мол. |
Плотность, г/моль |
см‘/моль |
| Метан .... | 0,25* |
13,8 | 2,21 |
8,84 |
| Бутан .... | 0,584 | 86,2 |
50,1 | 86,0 |
| 52,31 |
94,84 |
* Из рис. IV.31 52,31/94,84 = 0,552 г/см'.
Газ до теплообменника
Превышение энтальпии пара над энтальпией жидкости ггри температуре 0° С и давлении, равном нулю (рис. IV. 74):
63,7 X 2150 =
137 000 кал 309 000 кал
36,3 X 8500 =
446 000 кал
Влияние давления (из рис. IV. 51) —
— Д/ = 2,5 X 394 = 985 кал/моль.
446 000 кал при давлении, ранном нулю, и температуре 121°С минус 98500 кал при 121° С и абсолютном давлении от нуля до 141 на 100 молей равно 347 500 кал.
Газ из сепаратора при давлении, равном нулю (рис. IV. 74):
0,883 X 67 X 1260 = 74600 кал
0,117 X 67 X 5830 = Д/
Влияние давления: ¦— — = 0,58
— Д/ = 0,58 X 294 = 171 кал; —171 X 67 = —
— 11420 кал/моль 120 300— 11 420 = 108 880 кал.
Жидкость из сепаратора: 21° С при давлении, равном нулю (рис. IV. 72):
метан 0,138 X 33 X 297 = 1350 кал............73 г
n ™ 18750 кал 1650 г
бутан 0,862 X 33 X 660 = 20Ю0 кал...... 1723 г
Влияние давления (рис. IV. 73):
/210 9 — ^ = 3,24 к&л/з1!
/р — Iq = 0,32 кал/г,
/ — /0 = 0,32 х 1723 = 550 кал.
Энтальпия жидкости равна 20100 + 550 = 20650 кал.
Теплота, выделяемая в теплообменнике, составит 347500 — 108880 — 20650 = 217970 кал.
Максвелл построил диаграммы, в которых энтальпия индивидуальных компонентов дана в зависимости от температуры и давления (рис. IV. 75). Для жидких смесей индивидуальных компонентов справедливо правило аддитивности. Для паров же это правило более справедливо в интервале давлений от нуля до 1 ат. чем при давлении, большем атмосферного. Изменение энтальпии чистого пара в зависимости от давления может быть найдено путем интерполяции диаграмм по среднему молекулярному весу смеси. Если компонент находится в жидкой фазе, хотя температура и давление соответствуют двухфазному состоянию, энтальпия жидкости определяется по линии «насыщенная жидкость» при данной температура
Г ейпер а т ур а,°С -17,5 -10 0 10 20 30
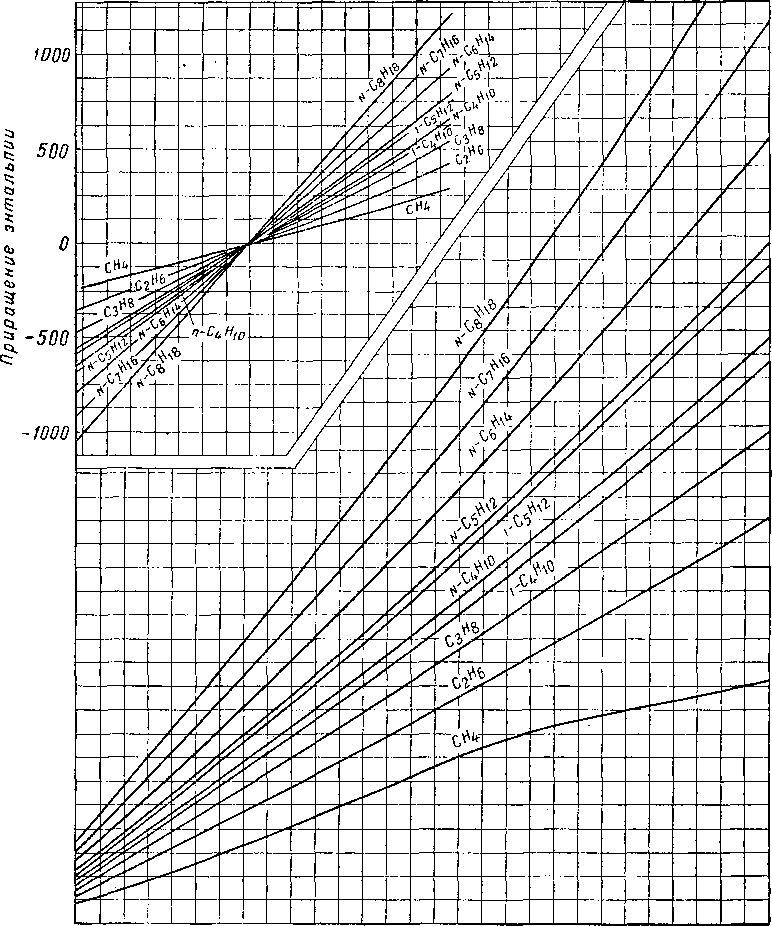
Сз
53
*
CD
3000
о
Рис. IV. 72. Приращение энтальпии углеводородных жидкостей при данной температуре и нулевом давлении по сравнению с эптальпией жидкостей при давлении и температуре (в °С), равных
нулю [III. 25].
Плотность при !5°С,г/см3 /$0,50 0,55 0,60 0,65 0,70 0,75 0,80 0,85 0,90
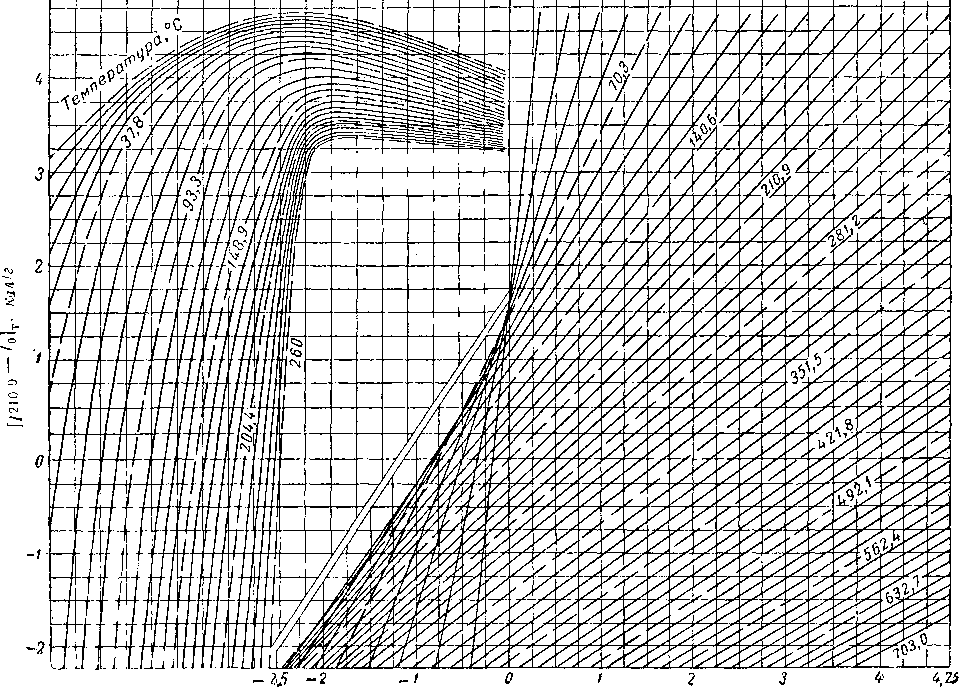
1р~10, «ал/?
Рис. IV. 73. Изотермическое изменение энтальпии ления по сравнению с их энтальпией
U2b 5 6 7 S 9 10 11 12 13 14-
9 r~"
—————————i——r——————r—r—i———r————i———r—i——
——
2t ь Ux
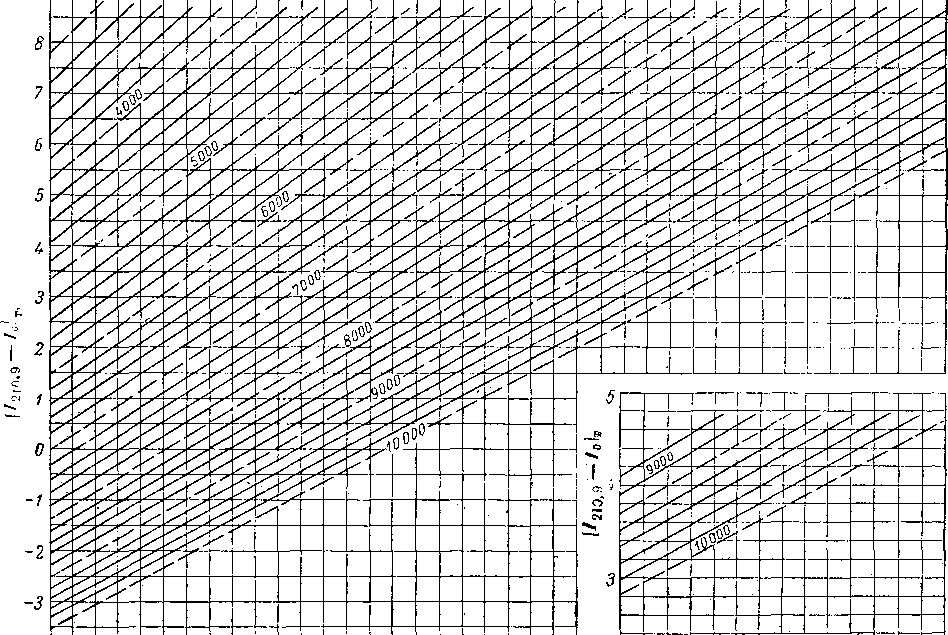
28 '
'13,25 14- 15 Id 16,75
[lp~Io]j
жидких углеводородов в зависимости от дав-при давлении, равном нулю [III. 25].
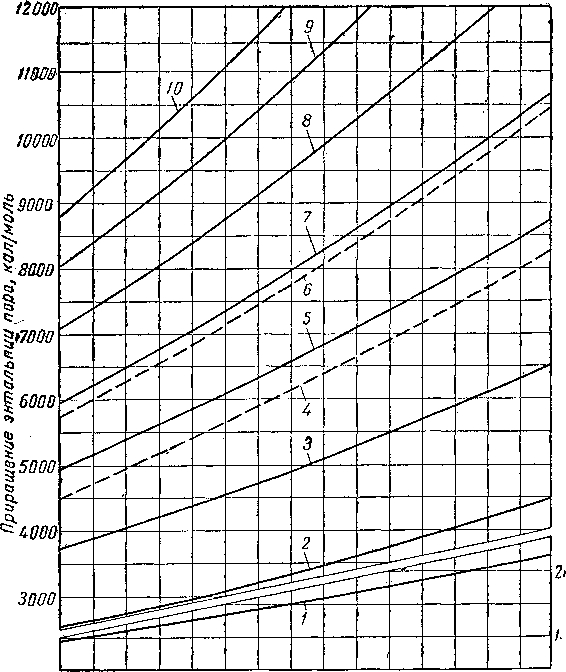
-20 О 20 4-0 60 80 /00 /2д
Температ-ура, °С а
Рис, IV. 74. Приращение энтальпии паров углеводородов при с энтальпией жидкости при давлении
/ S— метан; 2 — этан; 3 — пропан; 4 — изобутан; 5 — бутан;
Пример (см. начало стр. 69)
Средний молекулярный вес смеси до теплообменника — 31,3, газа в сепараторе — 20,9.
Смесь до теплообменника.
Интерполяция влияния давления между этапом и пропаном.
|
Давление, ат | 1, кал/гр | |
| этан | пропан |
|
| 0 | 225 |
214 |
| 141 |
182 | 146 |
| 43 | 68 |
|
Щ (68 - 43) + 43 = 45,3,
3130 х 45,3 = 142000 кал,
705000— 142,000 = 563000 кал при 121°С и 141 ат. Пример
Решить предыдущий пример с помощью диаграммы Максвелла. Исходная точка жидкости при температуре —94° С.
Газ из сепаратора.
Приращение энтальпии пара, нал/моль
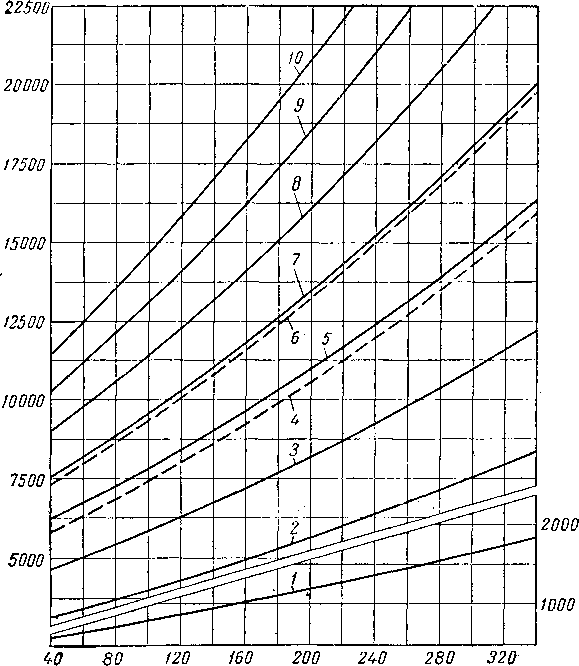
Температура, °С
5
данной температуре и атмосферном давлении по сравнению и температуре (°С), равных нулю [III. 25].
6 — изопентан; 7 — пентан; 8 — гексан; 9 — гептан; 10 — октан.
| Углеводороды | Поток до теплообменника прн 121° С и 14 1 ат | Газ из сепаратора при 21° С и 28 ат | Жидкость из сепаратора при 21° С | |||||||||
| число молей |
г | кал/г |
кал | число молей | г | кал/г |
кал | число молей | г |
кал/г | кал | |
| Метан .... Бутан .... |
63,7 36,3 | 1020 2110 | 245 217 | 250 000 455 000 | 59,2 7,8 | 946 455 | 189 165 |
179 000 75 000 | 4,5 28,5 | 74 1655 | 141 78 |
10 400 129 100 |
| 100,0 |
3,130 | 705 000 |
67,0 | 1 401 |
254 000 | 33,0 |
1 729 | 139 500 |
||||
Интерполяция влияния давления между метаном и этаном.
| Давление, ат | кал | |
|
метан | этан | |
|
0 | 188 | 179 |
| 28 | 180 | 163 |
|
8 | 16 |
254000— 15000 = 239000 кал при 21° С и 28 ат.
563000 — 239000— 139500 = 184500 кал.
Таким образом, в теплообменнике выделено 184 500/сал тепла.
На рис. IV. 76 — IV. 80 представлены составленные Петерсом диаграммы парциальных энтальпий компонентов от метана до пропана, если они находятся в смеси [IV. 67]. Энтальпия смеси равна сумме парциальных энтальпий компонентов. Чтобы найти разницу между эптальпией смеси и энтальпией исходной точки жидкости при —94° С, необходимо суммировать произведения энтальпий компонентов на их весовое содержание в смеси. При этом значения энтальпий находятся на диаграммах по значениям молекулярных весов или по средней молярной точке кипения.
Рис. IV. 75. Энтальпия углеводородов [I. 10]. Энтальпия жидкости в состоя* нни насыщения при —129° С принята равной нулю.
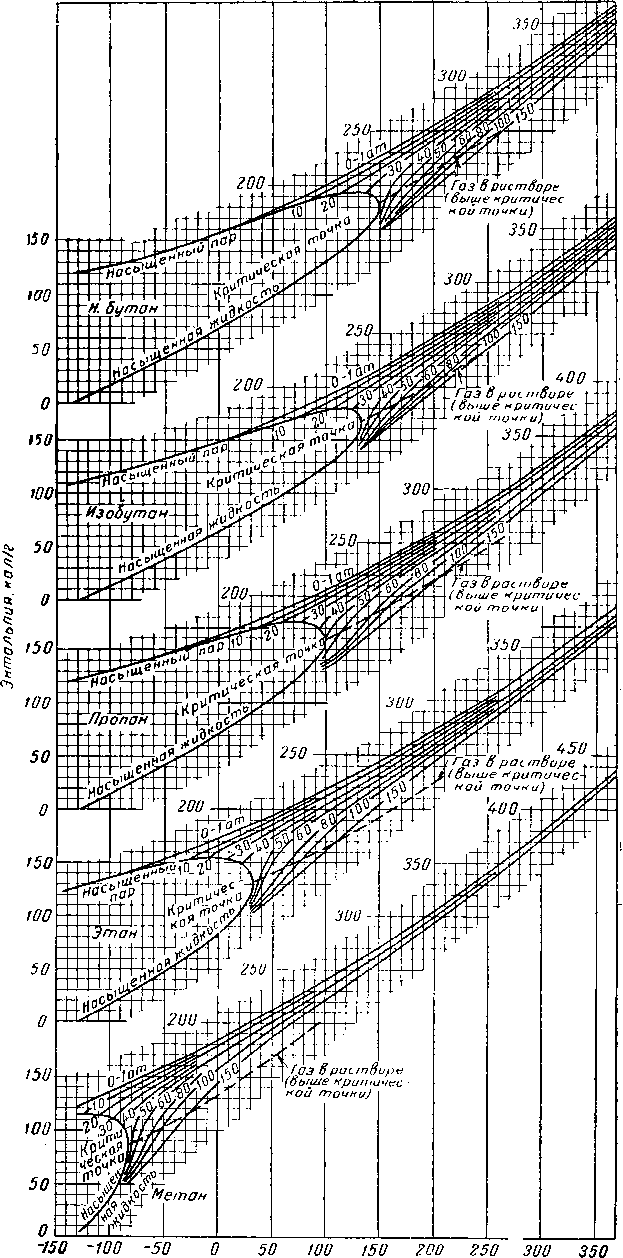
Темпвратура, °С а
Энтальпия, нал/s
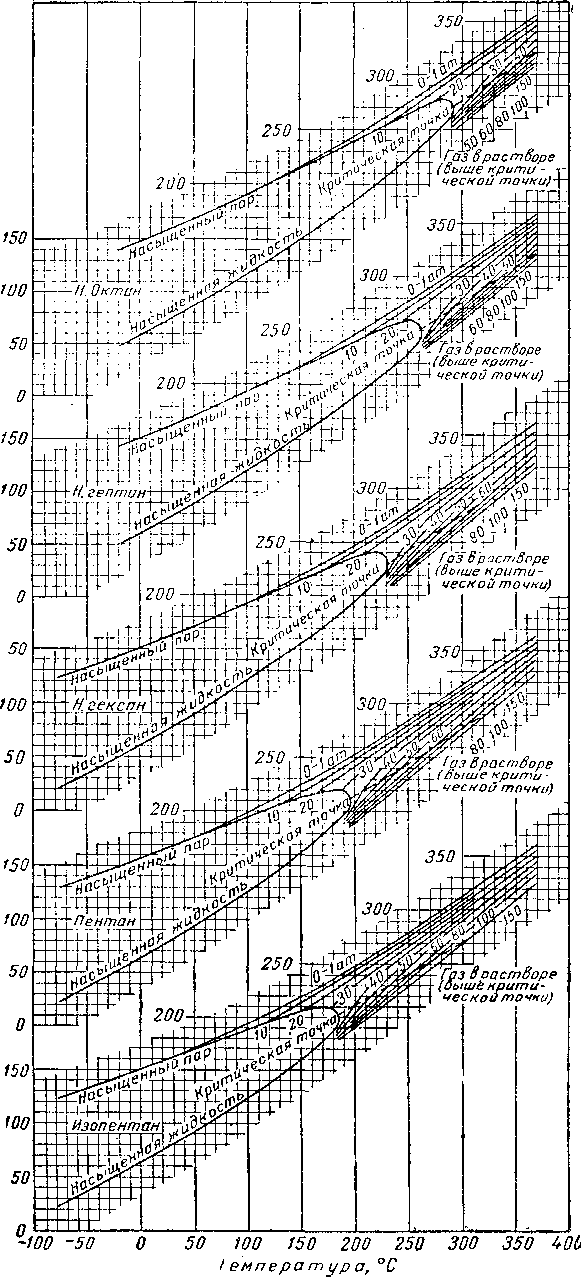
Температура, °С Рис. IV. 76. Энтальпия этилена [IV. 67].
Пунктирные линии давления относятся к чистому компоненту. Пунктирные линии энтальпии относятся к неточной области. В? —среднемольная точка кипения жидкой фазы; MW —
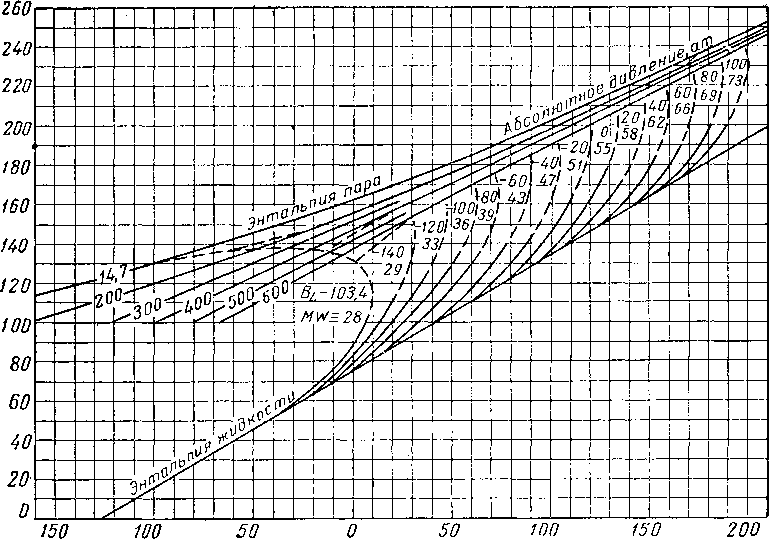
Энтальпия, нал/г Энтальпия, кал/г
молекулярный вес.
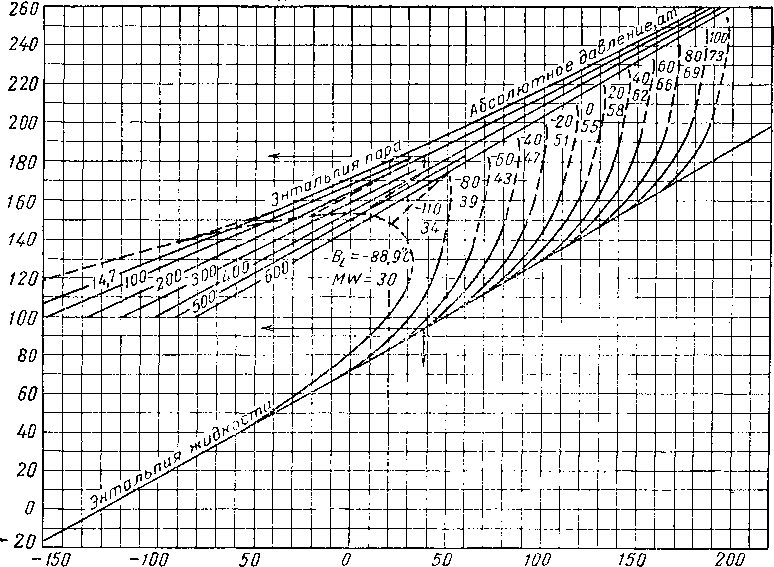
Температура, °С Рис. IV. 77. Энтальпия метана [IV. 67].
Пунктирные линии давления относятся к чистому компоненту. Пунктирные линии энтальпии жидкости относятся к неточной области. В^ —среднемольная точка кипения жидкой фазы; MW —молекулярный вес.
Рис. IV. 78. Энтальпия этана [IV. 67].
нктнрные линии давления относятся к чистому компоненту. Пунктирные линии энтальпии жидкости юсятся к неточной области. — среднемольная точка кипения жидкой фазы; MW — молекулярный вес.
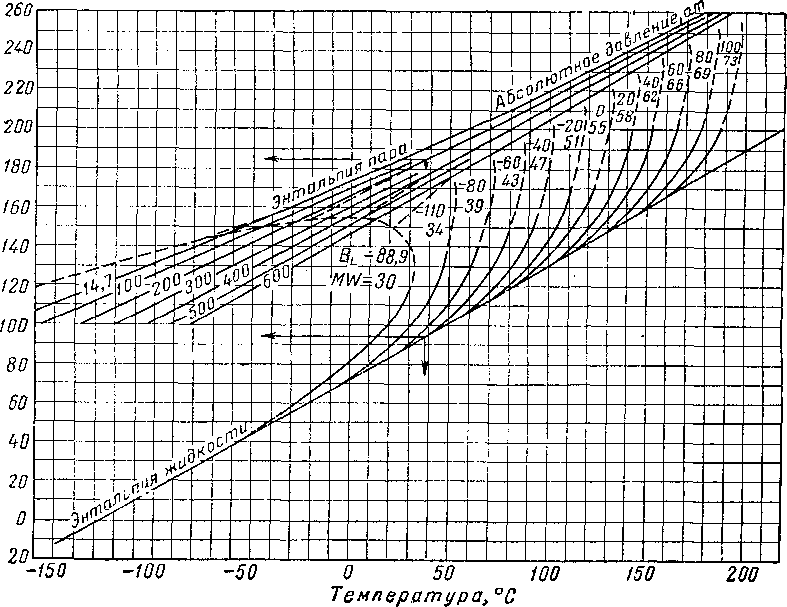
Энтальпир, кал/г “а Энтальпия, нал/s
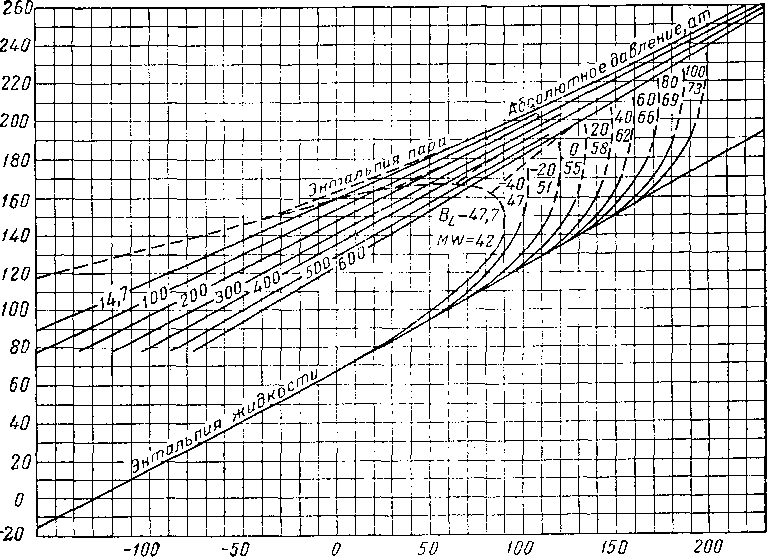
-150
Температура, °С
Рис. IV 79. Энтальпия пропилена [IV. 67].
Пунктирные линии давления относятся к чистому компоненту. Пунктирные линии энтальпии жидкости относятся к неточной области. Вг— среднемольная точка^кипения жидкой фазы; MW молекулярный вес.
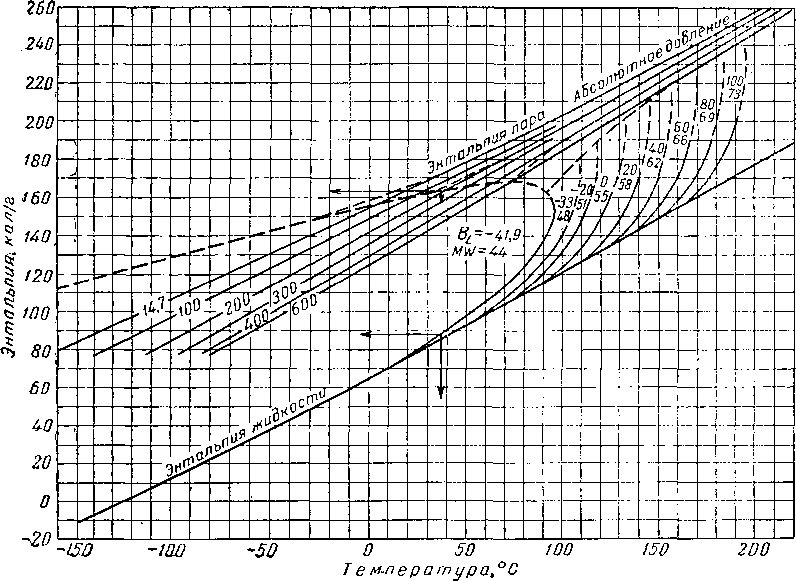
Рис. IV. 80. Энтальпия пропапа [IV. 67].
Пунктирные линии давления относятся к чистому компоненту. Пунктирные линии энтальпии жидкости относятся к неточной области. — среднемольная точка кипения жидкой фазы; MW— молекулярный вес.
§ 5. ТЕПЛОТВОРНАЯ СПОСОБНОСТЬ15
Теплотворной способностью природного газа называется тепло, выделенное при сгорании единицы объема газа в определенных условиях. Метан при 15,5° С и атмосферном давлении имеет теплотворную способность 8890 ккал/л.3 в случае, если горение метана происходит в воздухе. Эта величина теплотворной способ-нссти определяется количеством тепла, выделившегося при охлаждении продуктов сгорания до 15,5° С и при конденсации образовавшейся влаги, и известна как общая или полная теплотворная способность. Значения теплотворной способности и индивидуальных углеводородов приведены в табл. П. 1.
Сгорание 1 моль метана происходит по следующей химической реакции:
СН4 (г) + 20а (г) -> СОа (г) + 2Н20 (ж) + 211 ккал.
(IV. 36)
Так как скрытая теплота парообразования для воды при 15,5° С и атмосферном давлении равна 0,585 ккал, то для 2 моль воды 18X2x 0,585 = 21,0 ккал-.
2Н20 (ж) -> 2Н20 (г) — 21,0 ккал. (IV. 37)
Складывая выражения (IV. 36) и (IV. 37), получим количество тепла, выделившегося при сгорании метана, без учета выделения тепла за счет конденсации паров воды:
СН* (г) + 20а (г) ->СОа (г) + 2НаО (г) + 189,4 ккал.
Величина теплотворной способности 1 м3 метана при 15,5° С и атмосферном давлении определена в предположении применимости к нему законов идеальных газоз путем деления 211 ккал на 0,02375 м3/моль, что даег 8S73 ккал на 1 м3 идеального газа. Метан при 15,5° С и атмосферном давлении имеет коэффициент сжимаемости 0,998 (рис. IV. 18), поэтому общая теплотворная способность 1 м3 метана равна
8873
Q-ggg = 8890 ккал/м2.
Методика измерения теплотворной способности природного газа и применяемая при этом аппаратура описаны в [IV. 2]. На рис. IV. 81 схематически изображен водяной калориметр. Принцип действия этого калориметра состоит в том, что газ с определенной скоростью сжигается в камере сгорания, выделяя тепло, которое идет на повышение температуры проходящей через калориметр воды. Скорость циркуляции воды определяется взвешиванием воды, прошедшей через калориметр за определенный промежуток времени. Сконденсированная вода собирается в мернике. Воздух для поддержания горения подается на 40% больше требуемого теоретически. В расчет общей теплотворной способности следует вводить поправку, учитывающую влажности воздуха и испытуемого газа.
Для измерения теплотворной способности газов в газопроводах применяются регистрирующие калориметры непрерывного действия. Однако калибруются эти приборы с помощью описанного выше водяного калориметра.
Теплотворная способность природного газа может быть подсчитана по теплотворным способностям входящих в него компонентов и состава газа (табл. П. 1) в предположении, что природный газ подчиняется законам идеального газа или по правилу аддитивности объемов. В табл. IV. 18 приведен такой расчет в предположении аддитивности объемов компонентов.
Таблица IV.18
Расчет теплотворной способности природного газа известного состава
|
Компонент | Молярные или объемные доли | Теплотворная способность компонентов при 1,033 am и 15,5е С, ккал/м.3 |
Общая теплотворная способность газа, ккал/мг |
|
Азот..... | 0,023 |
0 | 0 |
|
Метан .... | 0,887 |
8890 | 7890,0 |
| Этан..... | 0,056 | 15650 | 877,0 |
| Пропан .... |
0,021 | 22600 |
475,0 |
| Изобутан . . | 0,003 |
29440 | 88,3 |
| «-Бутан . . . | 0,006 | 29590 | 177,6 |
| Пентаны . . . |
0,004 | 35100 |
140,4 |
| 1,000 | 9648,3 |
Таким образом, теплотворная способность газа при абсолютном давлении 1,033 и температуре 15,5° С равна 9648 ккал/м3. Например, при абсолютном давлении 1,029 и температуре 15,5° С теплотворная способность того же 1,029
газа будет равна j-ggg 9648,3 = 9633,7 ккал/м3.
Если природный газ насыщен парами воды при температуре 15,5° С и давлении 762 мм рт. ст., то величина теплотворной способности будет
„„„„ „ 762 762 — 13
9648,3 —^02— = 9500 ккал/м3.
Если в каждых 10 м3 газа содержится 1,8 г (0,1 моль) воды, то общая теплотворная способность такого газа при абсолютном давлении 1,033 и температуре 15,5° С будет
9648,3 10+ (0,1 х 0,0238) = 9648'° ккал/м3.
Цапфф (Zapffe) [IV. 98] построил диаграмму зависимости теплотворной способности природных газов от их удельного веса (рис. IV. 82). На этом рисунке разные линии соответствуют различному содержанию инертного газа.
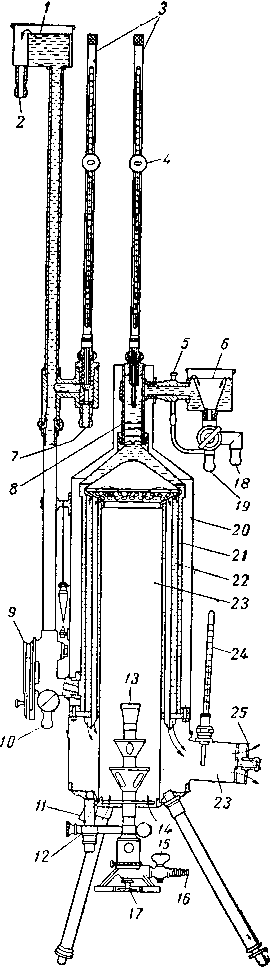
Рис. IV. 81. Схема американского водяного калориметра [IV. 2].
/ — водослив; 2 — сток воды; 3 — термо
метры для измерения температуры воды поступающей, отходящей; 4 — смотровое стекло; 5 — отводиая трубка: 6 — выходной водослив; 7 — вход воды; 8 — пластины для перемешивания; 9 — устройство для регулировки расхода воды; 10 — дренажный кран; // — выпуск сконденсировавшейся воды: 12 — держатель горелки;
13 — распылитель пламени: 14 — воздух;
15 — горелка: 16 — газ; 17 — игольчатый
вентиль: 18 — обводная линия: 19 — к мерному сосуду; 20 — воздушная рубашка;
21 — водяная рубашка; 22 — конденсатор;
23 — камера сгорания: 24 — термометр на
выходе; 25 — регулятор тягн; 26 — сборник продуктов сгорания.
Hi
N1
2,5*
~ 2,37 = 1'
*’ х — 21,26 = 4,7%-
(IV. 39) (IV. 40) (IV. 41) (IV. 42) (IV. 43) (IV. 44)
СНз ОН 4 СНО-
сно-
сно„
о2 + м ¦ -HCHO н
м,
65001_______________
ДО 0,57 0,59 0,61 0,63 0,65 0,67 0,69 0,71 0,73 0,75 Удельный Вес
Рис. IV. 82. Связь между теплотворной способностью, удельным веоом и содержанием инертных газов [IV. 98].
Водонасыщенность отнесена к 762 мм вод. ст. и 15.5° С.
Льюис и фон Елбе (Lewis and von Elbe) [IV. 58, IV. 35] дали следующий возможный порядок химической реакции:
НСНО+ 02 -> свободные радикалы -*¦ ОН,
ОН + СН4 Н20 + СН3,
+- 02 ОН + нсно,
¦ нсно-> н2о + сно, f 02-*С0 + но2,
Чтобы процесс горения начался, источник воспламенения переводит некоторое количество метана (СН4) в свободные радикалы, которые в свою очередь окисляются до формальдегида (HCHO) и ОН. Радикал ОН реагирует с метаном по уравнению (IV. 40) и восстанавливается по уравнению (IV. 45) но цепной реакции. Подобные же реакции объясняют процесс горения других углеводородов. Одним из условий, при которых не будет горения, является разрушение радикалов ОН до того, как они сумеют прореагировать с СН4. Часто причиной разрушения радикалов ОН является твердая поверхность.
Скорость химической реакции может быть рассмотрена в свете скоростей движения и числа столкновения молекул. Вообще говоря, при определенных условиях скорость реакции может быть измерена, но шкала времени должна выражаться в микросекундах (1 : 1 ООО ООО сек). Скорость реакции резко возрастает при увеличении температуры. Примерно можно считать,
2С.0-|-Н20+ ОН. (IV. 45)
• сно„
H5D0
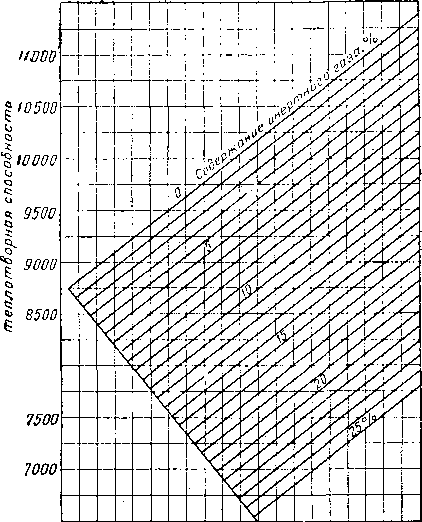
Таким образом, нижний предел воспламеняемости данной смеси газов равняется 4,7% об. газа в смеси с воздухом.
Зависимость пределов воспламеняемости от давления дана на рис. IV. 83 и IV. 84. Из рис. IV. 83 видно, что при давлениях ни^се 50 мм рт. ст. смеси природного газа с воздухом не “боспламеняются. При давлениях выше атмосферного (рис. IV. 84) увеличение его приводит к резкому увеличению верхнего предела воспламеняемости. Характерно, что смесь 40% мол. пропана и 60% мол. воздуха, образующаяся в результате смешения с пропаном горячего воздуха, поступающего из компрессора под давлением 42 ат, горит без взрыва, раскаляя трубы до вишнево-красного цвета. Добавление к смеси горючего газа с воздухом инертных компонентов. например азота или углекислого газа, как это видно из рис. IV. 85 и IV. 86, приводит к изменению пределов воспламеняемости. При этом как нижний, так и верхний пределы воспламеняемости повышаются, что объясняется частичным уменьшением концентрации кислорода в смеси при добавлении к ней инертного газа.
Процесс горения может протекать при сравнительно медленном распространении волны горения и при быстром распространении детонационной волны [IV. 58]. Волна горения распространяется за счет теплопередачи и диффузии между горящей смесью и невоспламенив-шнмся топливом. Детонационные волны — это ударные волны, которые образуются за счет реализации энергии химической реакции. При. атмосферном давлении скорость распространения фронта волны горения составляет порядка 0,3—2,4 м/сек. Нижнее значение этих скоростей присуще углеводородам природных газов, а верх-
что скорость реакции возрастает вдвое при увеличении температуры на каждые 15° С.
Существуют для каждых данных условий два предела воспламеняемости смесей воздуха и газообразных горючих веществ. Нижний предел соответствует минимальной концентрации горючего газа, при которой горение еще возможно. Верхний предел соответствует максимуму этой концентрации. В табл. П. 1 приведены значения нижних и верхних пределов воспламеняемости индивидуальных углеводородов в воздухе. Для метана в воздухе эти пределы соответствуют концентрациям 5 и 15% мол. или об., для пропана-—концентрациям 2,4 и 9,5%.
Для газовых смесей нижний предел воспламеняемости может быть легко подсчитан по нижним пределам воспламеняемости компонентов [IV. 27] при помощи следующей формулы:
где индексы 1, 2, 3 относятся к компонентам 1, 2, 3; п — содержание каждого компонента в смеси при нижнем пределе воспламеняемости в молярных или объемных процентах; Л'—нижний предел воспламеняемости каждого компонента в чистом виде в молярных или объемных процентах.
Пример
Вычислить нижний предел воспламеняемости природного газа, состоящего из 92% об. СН4, 5,5% С2На и 2,5% об. С3Н8.
Решение
Обозначив через х процентное содержание газа в смеси газ — воздух, имеем
92,0 х 5,5 х ~5ДГ + 2"
18,5 *+ 1,71 х + 1,05 л =
(IV. 46)
п2
| Атмосферное давление | ||||||||||||||
| Ч |
4 | 4 |
4 | 4 | 4 | |||||||||
| * | ч | 4 | 4 | 4 | ч | |||||||||
| Ч | 4 |
4 | 4 | 4 |
ч | |||||||||
| Ч | ч |
14 | \V | N4 | 4 | к |
||||||||
| Ч\ cnj W4! | ' 05у7астЪ\\ | \\ пи- ч\Ч | 4 | к | ||||||||||
| S | 41 |
к\Ч | \\ | Ч\1 |
к | |||||||||
| к |
ч\Ч | 4 |
Ч | 4 |
хч | |||||||||
| Ч |
Ч’ | 4 | 4 |
41 | ч | 4 | О | |||||||
| * |
Ч | Ч | 4 | 4 | \Ч |
чЧ1 | ||||||||
| Ч |
Ч | Ч | 4 |
кх | Ч |
4 | V V | |||||||
| ч |
Ч: | \ч V\ |
[4 | и |
ч^ | |||||||||
| -- 1 | ч |
ч | \Ч | кч | к4 | 4 | 4 | ч | ч |
N | ||||
| ч | ч |
Ч; | Ч' |
4 | ч^ |
Г | ||||||||
| 4N |
4 | 4 |
(4 | > | ||||||||||
| J—t | ||||||||||||||
2 4 6 8 W 12 14-
Содержание" природного газа, % о5.
|
'/ |
7а | Я |
1 | |||||||||||||
| ?/ |
ъ | у/, | К | // ч | Z | |||||||||||
|
А | уа |
УЛ | УЛ | й | N | 'А |
Ул | |||||||||
| \А | у, |
Ъ | V- |
У | V |
Y' | 2 | V | ||||||||
| ъ |
Ъ | "Л |
ул | у<\ | ул | % |
? | А | /> // | И | ||||||
| k |
Об | Лй |
сг | / / пь | ОС! | 7У7 |
у/ ам | ен | к/ яе | 1/ / 40 | У А// сти |
|||||
| к |
V |
у/. |
Й | // | Ч | |||||||||||
| V' |
УА | УА | к | V |
V |
ул | W | |||||||||
| А | У/ |
'Л |
ул | УА | '// |
V | ||||||||||
| ъ |
V | УА |
% | V, |
V |
у/, | УА | % | А |
|||||||
| % | V/, | У), | 'А |
г |
% | % |
У/\ | У/ |
я | |||||||
| ~ |
||||||||||||||||
50 W0 150
Абсолютное давление^апг
800 700 . 600 $ о
'S 500
* ш
<b'
5j
? 300
«5
^ 200
WO
О
ВО ¦§' 55 S? 50 а" 45 «> а
S 40
сз
8 35 I 30
§ 25 О.
* 20 <ь
5 /5 сз
5 to
о.
5
сз
«о Q
гол
Ри-c. IV. 83. Влияние снижения давления ниже атмосферного на пределы воспламеняемости смесей природный газ — воздух [IV. 58].
Рис. IV. 84. Влияние увеличения давления выше атмосферного на пределы воспламеняемости смесей природный газ — воздух [IV, 84].
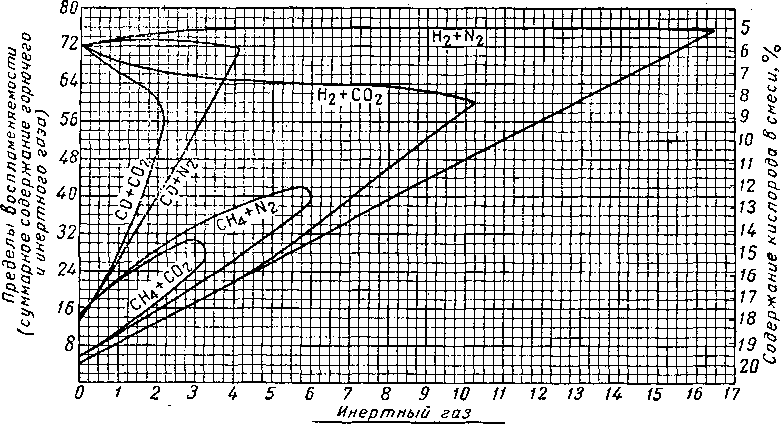
В оспламеняемыи газ
Рис. IV. 85. Пределы воспламеняемости смесей горючий газ — воздух, содержащих разные количества азота и углекислого газа [IV. 58].
45
40
35
-30
10
5
|
тг^ | |||||||||||||||||||||||||||||
| _ | |||||||||||||||||||||||||||||
| • , |
& | ||||||||||||||||||||||||||||
| У | _ | ||||||||||||||||||||||||||||
| / | " |
||||||||||||||||||||||||||||
|
/ | - | ||||||||||||||||||||||||||||
| 1 |
У | И |
/ | ||||||||||||||||||||||||||
| г |
\ | ? | - | ||||||||||||||||||||||||||
| / | |||||||||||||||||||||||||||||
| / |
г | /- | е> |
эа | СП | рс | С/ |
ЛО | CL |
- | |||||||||||||||||||
|
/ | |||||||||||||||||||||||||||||
| - | |||||||||||||||||||||||||||||
| > | |||||||||||||||||||||||||||||
| — | |||||||||||||||||||||||||||||
0 1 2 3 4-5
6 7 8 9 10 11 12 13 14 15
Инертный газ Пропан
a
тэ
о
§¦
О
*?
oj Рис. IV. 86. Пределы воспламе-§ няемости смесей пропан — воздух,
2 содержащих разные количества
о. азота и углекислого газа [IV. 58].
/ — углекислый газ: 2 — азот.
о
О
<o
12
13
H
15
16
17
18 19 2C,
ga gS ^ Q
<Ь^
5: ^ Cj
^5 25 <s 20
0*5 CS U 4>«5 15
«4 G) 6
^ S «
^ Л ^
rS?S-^ ^5>
которых возможно детонационное горение, приведены в табл. IV. 19.
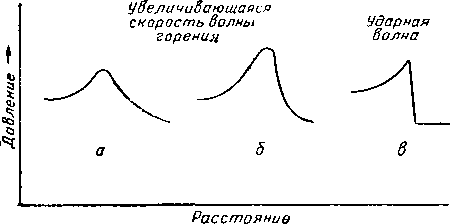
Рис. IV. 87. Упрощенное представление о развитии ударной волны [IV. 40].
нее — водороду. Эти скорости достаточно малы и допускают визуальное наблюдение за распространением волны горения.
В некоторых процессах горения скорость распространения волны горения, образованной источником воспламенения, резко увеличивается, достигая значения, характерного для детонационной волны. Начиная с этого момента, скорость остается сравнительно постоянной. Скорость распространения детонационной волны горения (900—3000 м/сек), в несколько раз превышает скорость звука в воздухе при комнатной температуре. На рис. IV. 87 схематически изображены развитие волны горения и переход ее в детонационную ударную волну. Невоспламенившаяся смесь горючего газа с воздухом сжимается непосредственно впереди зоны горения, как показано на рис. IV. 87, а. Увеличение давления приводит к увеличению температуры, что в свою очередь увеличивает скорость реакции. Увеличение скорости реакции по мере продвижения франта горения происходит до тех пор, пока не достигаются условия, известные под названием фронта удара (рис. IV. 87, в). Этот фронт удара или детонационная волна распространяется с высокой, но постоянной скоростью до тех пор, пока он поддерживается энергией, выделяющейся в результате химической реакции. Для многих смесей природных газов с воздухом скорость распространения волны горения не достигает значений, достаточно высоких для создания детонационной волны. Пределы концентраций, при
Таблица IV. 19
| Смесь |
Содержание топлива, % об. |
|
| иижний предел |
верхний предел | |
|
Ы2 — воздух |
18,3 | 59 |
|
Н2 - О, | 15,0 | 90 |
|
С3Нд - 02 |
3,2 | 37 |
|
г-С4Н10 — Оа | 2,8 |
31 |
|
с2н2-о2 |
3,5 | 92 |
|
С2Но — воздух |
4,2 | 50 |
|
NH3 — 02 |
25,4 | 75 |
Примечание. Данные взяты из [IV. 58].
Горение смеси газ — воздух в комнатных условиях, даже когда не достигается детонационная скорость, может привести к повышению давления, вызывающего значительные разрушения. Более серьезные последствия вызываются при перерастании волны горения в детонационную волну и образовании фронта удара.
2. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКОГО ДАВЛЕНИЯ И ТЕМПЕРАТУРЫ
При изучении фазового состояния смеси могут потребоваться значения истинных критической температуры и критического давления. Смит и Ватсон (Smith and Watson) [IV. 86], Карета и Катц (Kurata and Katz) [1. 2, IV. 52а] и Органик (Organik) [IV. 66] предложили методы определения этих критических свойств. Ниже описывается метод определения критического давления и критической температуры, предложенный Органиком. Этот метод заключается в вычислении среднемольной точки кипения В и оредневесового молекулярного веса Wm смеси с последующим нахождением критических условий по диаграмме рис. IV. 88. Может потребоваться использование рис. IV. 89 для нахождения поправки к среднеобъемным точкам кипения, а также применение рис. IV. 36.
Пример [IV. 66]
Рассчитать критическую температуру и критическое давление продукции скважины, если известен ее состав.
Состав продукции скважины
со2
сн4
CHoHg
С3Н8
;-с4н10
л-С4Н10
(-С5Н12
/z-CsH^
С0н14
QHjs + высшие (газ из сепаратора)
С7Н16 + высшие (жидкость из сепаратора)
Компоненты
| Газ из сепаратора, доли вес. |
Жидкость из сепаратора, доли вес. | Продукция скважины, доли вес. |
| 0,0229 |
0,0145 | |
| 0,6383 |
0,0173 | 0,4106 |
| 0,1187 | 0,0136 | 0,0802 |
|
0,0972 | 0,0338 |
0,0739 |
| 0,0199 |
0,0210 | 0,0203 |
| 0,0398 | 0,0460 |
0,0421 |
| 0,0136 | 0,0336 | 0,0209 |
| 0,0136 |
0,0382 | 0,0226 |
| 0,0116 | 0,1026 |
0,0450 |
| 0,0244 | — | 0,0155 |
| — | 0,6939 | 0,2544 |
Разгонка компонента C7Hie + из сепараторной жидкости дала следующие результаты (удельный вес этого компонента при 15,5° С равен 0,7805 г/смг).
| Разгонка |
Фракции | Плотность, г/см9 | |
|
Начальная точка кипения 80° С Выкипание, %: | 1 | 0,7425 | |
| 10 | 91°С | 2 | 0,7436 |
| 20 | 100“ С |
3 | 0,7503 |
| 30 | 110°С |
4 | 0,7572 |
| 40 | 12ГС |
5 | 0,7678 |
| 50 | 137“ С |
6 | 0,7796 |
|
60 | 154“ С |
7 | 0,7910 |
| 70 | 178° С |
3 | 0,8054 |
|
80 | 204° С |
Остаток | 0,8423 |
Примечание. Наклон кривой разгонки 10—90% Роняется 1,83° С/%. Среднеобъемная температура кипения 150° С.
Решение
1. Расчет среднемольных и средневесовых свойств тяжелого остатка.
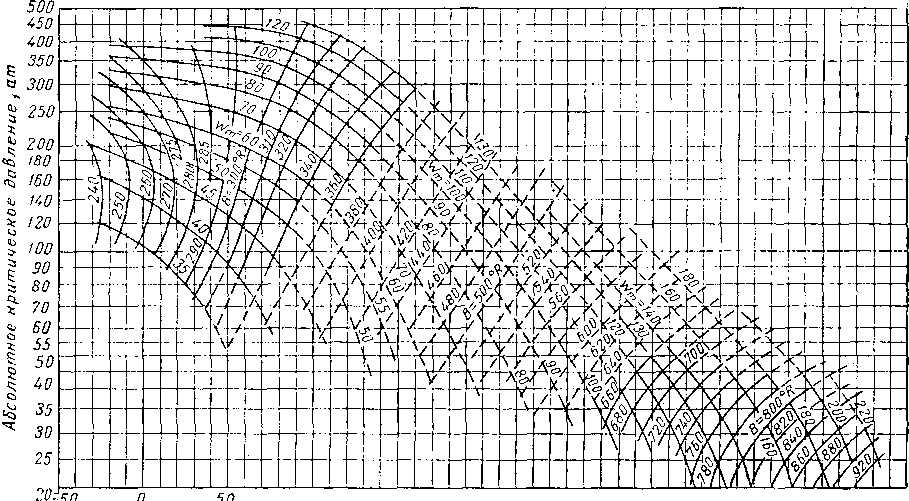
100
150 200 250 300
Критическая температура,°С
350
400
450
Рис. IV. 88. График для определения критических температур и критических давлений
сложных смесей [IV. 66].
В — среднемольная температура кипення в 3R (T°R - 1,8 7° К); ^ т~ средневесовой молекулярный eecj
Наклон кривой, разгонки ASTM 10-90% ,°С/’/0
¦Q
а;
5
О)
гО
^сь
С)
О)
t
О)
ta
*
«о
СЦ
cr
о . Cz
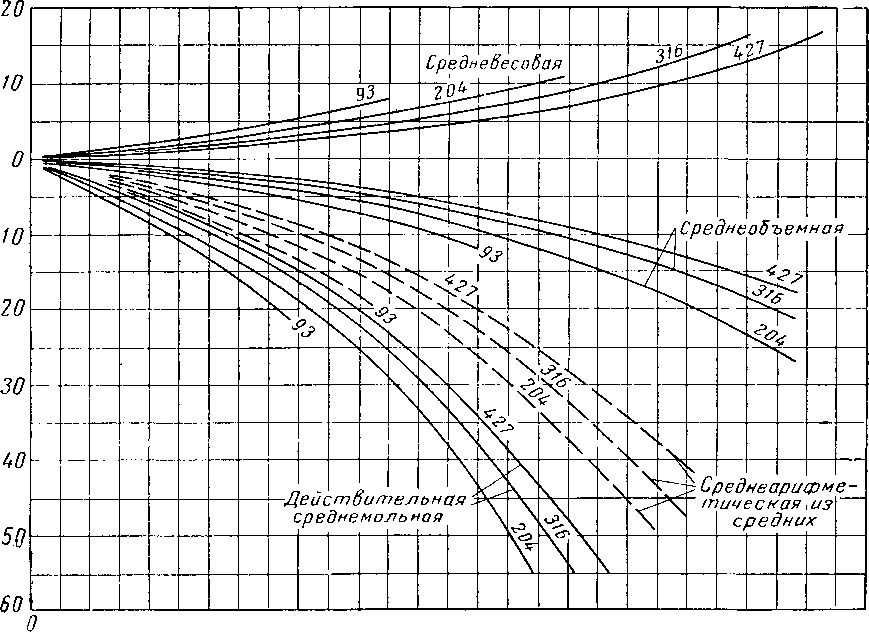
Сс
3
J:
си
с:
з
t
г:
в
1=
CJ
Cl.
Q)
С
?
Рис. IV. 89. Поправки к среднеобъемным температурам кипения [IV. 86; 1. 2].
Цифры на кривых обозначают среднеобъемиые температуры кипения в ° С.
Для расчета В и Wm продукции скважины известного состава в первую очередь желательно определить эти величины для фракции C7Hi6 + в газе и жидкости из сепаратора. Можно принять, что фракция C7Hi6 + для сепараторного газа имеет свойства нормального октана: В = 399° К и №т = 114. Для определения В и Wm этой же фракции из сепараторной жидкости рекомендуются два метода. Первый метод служит для грубой, но быстрой оценки этих свойств. Для более точных расчетов рекомендуется второй, несколько более сложный и трудоемкий метод. Согласно первому методу предполагается, что В приблизительно равно средней арифметической из средних температур кипения и что Wm для фракции С7Н!6 + существующих в природе смесей может быть определено непосредственно по наклону кривой разгонки и на основании среднего значения характеристического фактора.
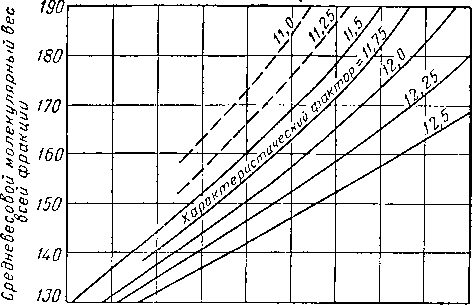
/ 1,5 2 г,5 3 3,25
Наклон кривой разгонки ASTM 10-30 °/o°Cj°/i
Средняя арифметическая из средних температур кипения определяется из диаграммы рис. IV. 89: наклон кривой разгонки 10н-90°/о = 1,83°С/%, среднеобъемная температура кипения равна 150° С, поправка к среднеобъемной температуре кипения равна —12° С. Средняя арифметическая из средних температур кипения 138° С.
Рис. IV. 90. Средневесовой молекулярный вес нефтяных фракций (С7+) [IV. 66].
среднекубическая температура кипения определяется следующим образом.
Средняя объемная температура кипения равна 150° С; поправка к среднеобъемной температуре кипения равна —5° С.
Среднекубическая температура кипения 145° С.
Следовательно, В равняется 138 + 273 = 411° К.
Значение Wm, как указано выше, определяется по наклону кривой разгонки и по среднему значению характеристического фактора. Последний может быть найден из рис. IV. 36 по известной плотности (0,7805 г/см3) и среднекубической температуре кипения. По рис. IV. 89
Расчет среднемольных и средневесовых свойств компонента гептаны + сепараторной жидкости
| Произведение колонок 4 и 14 1 | 1Л | '-DinwNtNNOUlCJO СТ-СОСО!-—t-— C4C4C4<NC4C4<NC4<N<N | СО '6 Сч |
| Частное от деления значений колонки 7 на значения колонки 13 | тг |
0,00825 0,00774 0,00750 0,00709 0,00673 0,00639 0,00594 0,00534 0,00525 0,00485 | СО СО 1Л иэ о о |
|
Действи* тельный молеку лярный вес | со | 1Л 0U30N’T<Nn — a)M 0)0)00—> <N СО 1Л 1Л t-» | |
| Произведение колонок 7 и 11 | С4 |
in(OWinONCOncOM ОтГСчЮСОООтГО^СО t-—t-—coao<7)0—‘co^in |
СО г— 1Л о |
|
Эквива лентный молеку лярный вес | - | woonmnwtNoo 0)0""tNOOTT,-Ot-'-0) | |
|
Средняя суммарная весовая доля фракции в сепараторной жидкости | О |
О О СО <N СО тг —« o<o <n 0)Ю"С0ЮтГтГЮ0)тГ nONMON’T'^OOiO ООтГтГЮ'-О'-ОС-'-СОаОО) оооооооооо |
|
| Суммарная весовая доля фракции в сепараторной жидкости |
О) | *~OOU3COO)OCN Ncoo ЦЭС4СОтГ—'Qoioioino О Nco О f«cOO NIO<MO nn ТГ ЮЮЧ) NNCO 0)0 ОООООООООО—" | |
|
Весовая доля фракции в сепараторной жид» кости 0,6939 г 78,05 | СО |
0)0^0сч<->—iwintoto in !?)tD N00 0)0 —^ ТГ t-—t-—t-— оооооооооо ОООООООООО | |
| Весовое содержание, г |
С-- | Ю(ОпМООФО’т2о INnONNOl-ifl^’T ТГ ТГ Ю Ю со С-'- О) о ОО t-—f—t-—t-—t-—t-—t-—аоаосо | 1Л о со" О) |
| Характе ристиче ский фактор | иэ | > ЮтГОЮМСС0)ООО ЦЭ f-t-» t-» t-» «О «О Г-N ^ О 0. | |
| Экспериментально измеренная плотность при температуре 15,5® С, г/см® | 1Л | « юфпсчсо'оо’тоо о C-inONNC) -in -<N CO 1ЛТГ1Л1Л<ОГ-0)0 — <N *5 t-- t-- f— t-— t-— CO CO CO Q. оооооооооо ^ >23 <y | |
| Средняя температура кипения, еК |
ТГ | # * к cooiNO’Tcocomgl, 0 in<ONO)0-rt'JD22 д «cococo,,T',r',T',T 2» 2» eg 0. H и | |
|
Средняя температура кипения, *С |
СО | <r> a Ю СО тг --ЧЛ 1Л C4 JO a- cooio — w’t^w^c^ ^ — — — —^ * 0 | |
|
Состав, % мол. | С4 |
000000001 j | | 100 эатуры г |
| Фракция | - | 1 8 3 4 5 6 7 H 9 (остаток) 10 (остаток) Всего * Темпер | |
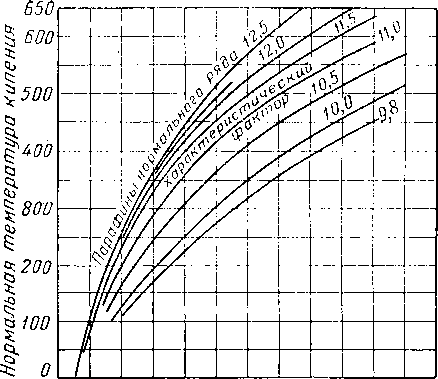
Эквивалентный молекулярный Вес
Рис. IV. 91. Эквивалентные молекулярные веса нефтяных фракций и компонентов газа [IV. 66].
Из рис. IV. 36 среднее значение характеристического фактора равно 11,7. На основании этих данных величина Wm может быть определена по диаграмме, представленной на рис. IV. 90. На этой диаграмме даны значения Wm в зависимости от наклона кривой разгонки для различных значений характеристического фактора. (Эту диаграмму можно применять только для фракции C7Hi6+ природного конденсатного газа и легкой сырой нефти и нельзя применять для фракций С3-Ь С9+ и т. д.). Из рис. IV. 90 находим Мт = 151.
2. Второй метод расчета является более точным, так как в этом случае тяжелые остатки разбиваются на ряд произвольно выбранных фракций. Свойства каждой фракции определяются и суммируются, что дает в итоге свойства всего остатка в целом. Подобный расчет приводится в табл. IV. 20, В этой таблице в колонках
3 и 4 даны значения средних температур кипения, взятых из кривой разгонки для десяти произвольно выбранных фракций.
Значения характеристического фактора для каждой фракции (колонка 6) взяты из рис. IV. 36 по экспериментально определенным значениям плотности и средним температурам кипения фракций. Вследствие того, что характеристические факторы почти постоянны и близки к 11,7, это же значение было принято и для
девятой и десятой остаточных фракций. Весовое содер
жание каждой фракции (колонка 7) можно выразить в весовых долях сепараторной жидкости в целом (колонка 8) умножением веса каждой фракции на отношение 0,6939/78,05, т. е. на отношение весовой доли фракции С7Н16 + К общему весу этой фракции. В колонке 9 эти весовые доли выряжены в виде суммарных весовых долей всей сепараторной жидкости.
Далее строится график зависимости логарифма абсолютной средней температуры кипения (колонка 4) от среднего содержания каждой фракции, выраженного в
весовых процентах (колонка 10) (рис. IV. 92). Полу
ченная на рис. IV. 92 вполне прямая линия проходит через все точки и экстраполируется до значения, соответствующего 100%, и средняя температура кипения оставшихся девятой и десятой фракций определяется по этой экстраполированной прямой. Из графика следует, что их значения равны соответственно 475 и 494° К. По
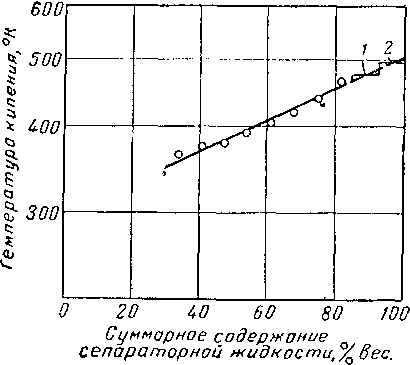
Рис. IV. 92. Кривая разгонки фракций С7+ сепараторной жидкости (полулогарифмический график) [IV. 66].
1 — остаток Хв 9; 2 — остаток Хв 10,
этим значениям определяем плотности, молекулярные веса и эквивалентные молекулярные веса этих фракций.
Эквивалентный молекулярный вес каждой фракции (колонка 11) можно найти из диаграммы рис. IV. 91 по средней температуре кипения и характеристическому фактору данной фракции. Затем вычисляется средневесовой эквивалентный молекулярный вес всего компонента С7Н16 + (Ат) путем деления суммы колонки 12 на общий вес компонента (см. колонку 7), Wm = 135,5. Среднемолярная температура кипения компонента С7Н16 + определяется путем деления суммы колонки 15 на сумму колонки 14, В = 411° К- II. Опреде-
Лейие величин В и Wm для продукции скважины Данного состава.
Подобно тому, как были определены свойства компонента С7Н16 + , могут быть вычислены и значения В и Wm для всей продукции скважины. Этот расчет приведен в табл. IV. 21.
В колонках 1 и 5 даны значения весовых и молярных долей компонентов продукции скважины. Последние получены из первых с использованием молекулярных весов, приведенных в колонке 4. В колонке 2 представлены значения эквивалентных молекулярных весов углеводородов, включая и значение для компонента С7Н16 +, вычисленное в табл. IV. 20. Значение Wт для продукции скважины определяется как сумма значений, приведенных в колонке 3, и равно 60,1. Значение 5 определяется как сумма значений колонки 7 и равно 155° К.
3, Определение критического давления и критической температуры из диаграммы рис, IV. 88.
Используя полученные выше значения Wm = 60,1 и 5=155° К по диаграмме рис. IV. 88, определяем критические параметры данной смеси.
Абсолютное критическое давление рс=235; критическая температура Тс = 26,6° С.
Абсолютное критическое давление, определенное по неполным экспериментальным данным для приведенной выше смеси, находятся в пределах 210—224, а критическая температура в пределах 10—24° С.
При применении упрощенной методики соответствие между расчетными и экспериментальными значениями неудовлетворительно для критического давления и вполне удовлетворительно для критической температуры. По упрощенной методике Wm = 64, а В <= 155° К. Этим значениям параметров смеси соответствуют следующие критические условия; абсолютное давление рс = 258, Тс - 21° С.
Для смесей, состоящих из таких компонентов, как метан, этан и т, д., но не содержащих компонента С7Н16 + , методика расчета значительно упрощается.
Таблица IV. 21
Расчет В и Wm для продукции скважины известного состава
| Компонент | Весо вые доли | Эквивалентный молекулярный вес | Произ ведение колонок 1 и 2 |
Действительный МО-леку-лярный вес |
Моль ные доли |
Темпе ратура кипе ния, •К | Произведение колонок 5 и 6 |
| 1 |
2 | 3 | 4 |
5 | 6 | 7 | |
| С02........... |
0,0145 | 44 |
0,64 | 44 |
0,0095 | 194 |
1,8 |
| Q........... |
0,4106 | 16,04 |
6,60 | 16,04 |
0,7371 | 112 |
82,7 |
|
С2........... | 0,0802 | 30,1 | 2,42 |
30,1 | 0,0766 |
184 | 14,1 |
| С3........... |
0,0739 | 44,1 |
3,26 | 44,1 |
0,0482 | 231 |
11,1 |
|
1-С4........... | 0,0203 | 54,5 | 1,11 2,45 | 58,1 |
0,0101 | 262 |
2,6 |
|
п-С4........... | 0,0421 | 58,1 | 58,1 |
0,0209 | 272 |
5,7 | |
|
/-С5........... | 0,0209 | 69 | 1,44 |
72,2 | 0,0084 |
301 | 2,5 |
|
п-С5........... |
0,0226 | 72,2 |
1,63 | 72,2 |
0,0090 | 309 |
2,8 |
| 0,0450 | 85 | 3,82 |
86,2 | 0,0150 |
366 | 5,4 | |
|
С7 и выше (из сепараторного газа) , | 0,0155 |
114 | 2,23 |
114 | 0,0039 |
398 | 1,6 |
|
С7 и выше (из сепараторной жидкости) ............... | 0,2544 | 135,5* | 34,5 |
119,5 | 0,0613 |
411* | 25,2 |
| Всего. . . |
1,0000 | * # О CD II ? | 1,0000 |
В = 155,5° К* |
* Взяты из расчета, приведенного в табл. IV.20. _
*• При подсчете по упрощенной методике получено Wm — 64, В = 155,5* К-
При изучении течения углеводородных жидкостей и газов по трубам и в пористых средах или в общем случае при изучении переноса количества движения, наблюдаемого при течении жидкостей и газов, необходимо знать их вязкость. Влияние вязкости на течение жидкостей и газов особенно важно при изучении фильтрации в нефтяных пластах, так как в этом случае течение преимущественно является ламинарным и перепад давления пропорционален вязкости. При ламинарном течении вязкость определяется из соотношения
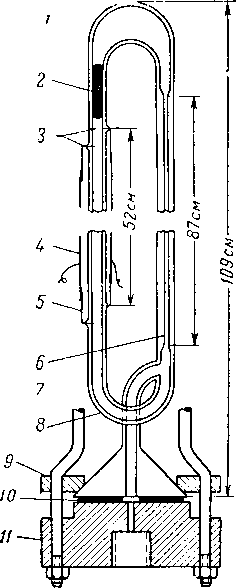
г] dU
(IV. 47)
dy
где 1)— коэффициент вязкости или абсолютная вязкость в г/см-сек',1—напряжение сдвига на единицу площади в плоскости, параллельной направлению движения, dU
в Г/см2; -jy — градиент скорости в плоскости, перпен-
• пе-
дикулярной к плоскости сдвига, в см/сек ¦ см\ g0 -ресчетный коэффициент (см2/Г) X (см/сек2).
Впервые понятие вязкости было постулировано Ньютоном, а позднее проверено экспериментально Пуа-зейлем для течения жидкостей по капиллярам [IV. 123].
За единицу абсолютной вязкости принят пуаз (пз), имеющий размерность г/см ¦ сек. Единица, в сто раз меньшая пуаза, — сантипуаз, в тысячу раз меньшая—¦ миллипуаз, в миллион раз меньшая — микропуаз. Вода при температуре 20° С имеет вязкость 1,0 спз.
Кинематическая вязкость численно равна отношению абсолютной вязкости жидкости к ее плотности:
спз ' г/см*
(IV. 48)
По вязкости жидкостей, текущих по капиллярным каналам под действием гидростатического давления, можно определить кинематическую вязкость [IV. 2].
Рис. IV. 94. Вискозиметр Ревкина [IV. 108],
/ — верхняя точка Л; 2 — ртуть;
3 — вольфрамовые контакты;
4 — медные проводники; 5 — никелевая проволока; 6 — капилляр; 7 — нижняя точка В; 8 — стекло; Э — алюминиевое кольцо; 10 — прокладка из сырой резины; 11 — стальная станина.
Для определения вязкости часто применяют вискозиметр с катящимся шариком (шариковый вискозиметр), принцип действия которого состоит в том, что скорость перемещения шарика в наклонной трубке определяется скоростью перетекания жидкости через зазор между шариком и внутренней стенкой трубки (рис. IV. 93). Как показано Комингсом, Майлендом и Эйгли (Comings, Mayland and Egly) [IV. 108], вязкость веществ, имеющих малую плотность, измеренная шариковыми вискозиметрами, вследствие турбулизации патока в зазоре между шариком и стенкой трубки получается неточной. Для определения вязкости газов предпочтительнее применять вискозиметр Ренкина (рис. IV. 94), в котором течение газа через капилляр происходит при малом перепаде давления. Стеклянный вискозиметр помещают в сосуд высокого давления, что позволяет измерять вяз-

Рис. IV, 95, Общий вид витаоз'имегра с катящимся шариком.
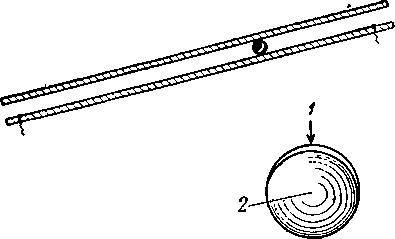
Рис. IV. 93. Принцип действия вискозиметра с катящимся ша'ришм,
/ — стснка трубки; 2 — шарик.
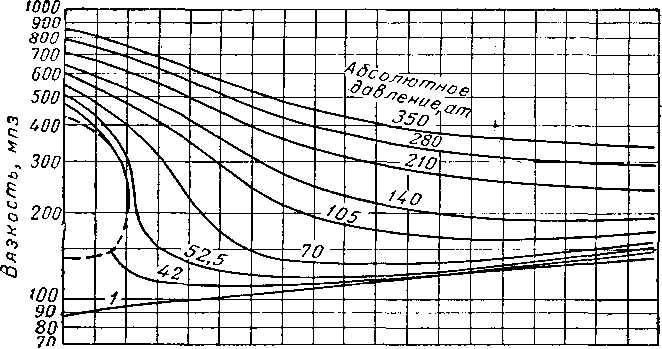
кость газов при давлениях, отличных от атмосферного. Шариковый вискозиметр (рис. IV. 95) широко применяют для измерения вязкости жидкостей при высоких давлениях, например вязкости жидкостей глубинных проб [IV. 112].
На рис. IV. 96 показано изменение вязкости этана в зависимости от изменения давления и температуры. При атмосферном давлении вязкость газообразного этана при увеличении температуры увеличивается. С другой стороны, вязкость этана в жидкой фазе при увеличении температуры уменьшается. При критической температуре свойства жидкой и паровой фаз становятся идентичными. При высоких давлениях увеличение температуры приводит к уменьшению вязкости газов, в том числе и при температурах, значительно превышающих критическую, В отличие от жидкостей, чем больше молекулярный вес пара, тем меньше его вязкость при атмосферном давлении. Увеличение размеров молекул газа приводит к уменьшению напряжения сдвига между слоями газа при его движении.
В табл. IV.22 приведена литература по исследованию вязкости некоторых индивидуальных газов при атмосферном давлении. Данные этих исследований и значения вязкостей, рассчитанные по методу Хиршфельде-ра, Бирда и Спотца (Hirschfelder, Bird and Spotz) [IV. 39], легли в основу построения графика, изображенного на рис. IV. 97.
Следует отметить, что кривая для вязкости изобутана расположена несколько выше кривой для н-бутана во всем диапазоне исследованных температур, хотя экспериментальные данные Тайтенца (Titani) [IV. 132] показывают, что при температуре, превышающей 100° С, их вязкости должны быть одинаковыми. Более поздние исследования показали, что пязкость углеводородов нормального парафинового ряда при температурах от 10 до 200° С несколько ниже (до 5%) вязкости их изомеров [IV. 136] в пределе температур, приведенных на рис. IV. 97. Малое отличие значений вязкости «-парафинов и их изомеров подтверждает положение о том, что «молекулы углеводородов нормального парафинового ряда, по-видимому, в среднем сильно скручены в газовой фазе» [IV. 136].
Рис. IV. 97. Вязкость газов при атмосферном давлении [IV. 106].
/ — гелий; 2 — воздух; 3— азот; 4 углекислый газ;
5 — сероводород; б —метан; 7 — этилен; 5 —этаи: 9 пропан; 10 ^ изобутан; 11 — н-бутаи; /2— н-пентан;
13 — «-гексан: 14 — лигептан, 15 — «-октан; 16 — «*нонан;
17 — «-декан.
Рис, IV. 96, Вязкость [IV. 130].
этана
Таблица IV. 22 Экспериментальные исследования вязкости индивидуальных газов при атмосферном давлении
| Газ | Литература | Г аз | Литература |
|
Гелий .... | IV.121 |
! Пропан .... | IV. 132 |
| Воздух .... |
IV. 114 | I Изобутан . . | IV. 132 |
|
Азот..... | IV.114 |
н-Бутан . . . | IV. 132 |
| Углекислый газ |
IV. 114 | н-Пентан . . . | IV. 132 |
|
Сероводород . | IV. 124 | н-Гексан . . | IV. 132 |
| Метан .... |
IV. 133 | н-Гептан . . | IV.116а |
|
Этилен .... | IV. 135 |
н-Октан . , , |
IV.116а |
| IV, 133 | н-Нонан . . , |
IV. 116а | |
| Пропан .... | IV. 134 | 1 |
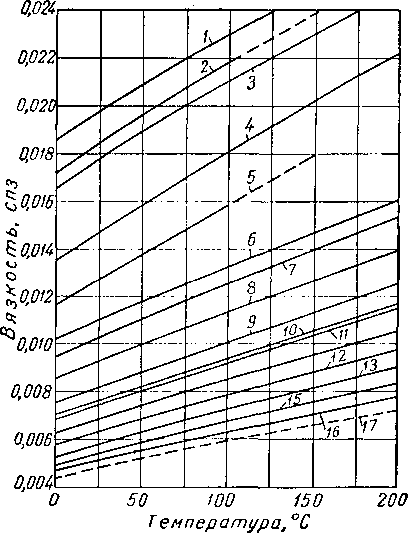
1. ВЯЗКОСТЬ ГАЗОВ ПРИ АТМОСФЕРНОМ ДАВЛЕНИИ
В свое время Бичер и Катц (Bicher and Katz) [IV. 101] представили данные вязкости газообразных углеводородов парафинового ряда при атмосферном давлении в зависимости от их молекулярного веса. Эти данные, несколько уточненные Карром, Кобаяси и Барроусом (Corr, Kobayashi and Burrows), изображены на рис. IV. 98.
Методы определения вязкости газовых смесей при атмосферном давлении, применимые и для смесей газообразных углеводородов, были даны Бичером и Катцем (Bicher and Katz) [IV. 101], Хернингом и Циппере-ром (Herning and Zipperer) [IV. Ill] и Хиршфельдером (Hirschfelder) с соавторами [IV. 39]. Последний метод основан на теоретической работе Чепмена и Коулинга (Chapman and Cowling) [IV. 24]. Расчеты по этой методике сложны и мало пригодны для практических расчетов вязкости смесей. Бромли и Уилк (Bromley and Wilke) [IV. 103] упростили методику расчета, предложенную Хиршфельдером (Hirschfelder) и соавторами, и дали графики и номограммы для определения вязкости смесей газов.
Хернинг и Ципперер (Herning and Zipperer) [IV. Ill] предложили следующее выражение для вычисления вязкости смеси газообразных компонентов:
2 ^ Ч УЩ Чс = -—-, (IV. 49)
s xiYm7
(=i
где 1см — вязкость смеси; — вязкость компонента »; Xi — молярная доля компонента i; М{—молярный вес компонента I.
Формула [IV. 49] позволяет просто и достаточно точно рассчитывать вязкость смеси природных газов, если известен состав этой смеси. Применимость формулы [IV. 49] для расчета вязкости бинарных и сложных смесей газов была подтверждена работами Карра (Сагг) [IV. 104, IV. 105] и Карра, Барроуса и Кобаяси (Carr, Barrows and Kabayashi) [IV. 106].
На рис. IV. 98 приведен график для определения вязкости смеси, состоящей преимущественно из углеводородных газов. Этот график дает возможность быстро получить достаточно точное значение вязкости газов при атмосферных условиях и данной температуре по их удельному весу.
На рис. IV. 98 даны также поправочные коэффициенты для уточнения значений вязкости углеводородных газов, содержащих небольшое количество сероводорода, aiiOTa и углекислого газа. Присутствие каждого из этих неуглеводородных компонентов приводит к увеличению вязкости смесей газообразных углеводородов.
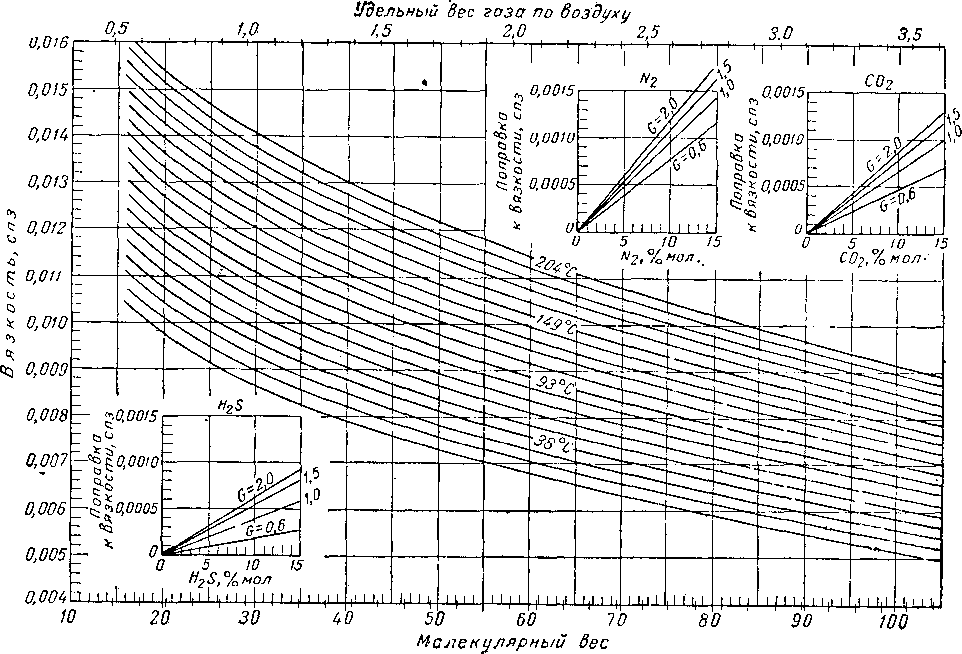
2. ВЯЗКОСТЬ ГАЗОВ ПРИ ПОВЫШЕННЫХ ДАВЛЕНИЯХ
В табл. IV. 23 приведена литература по исследованию вязкости газов при высоких давлениях.
Таблица IV. 23 Экспериментальные исследования вязкости газов при высоких давлениях
Метод исследования
Газ
IV. 102 IV. 117*
IV. 122* IV. 131* IV. 129 IV. 118 IV. 108*
IV. 127 IV. 100 IV. 108* IV. 105*
IV.116 IV.108*
Азот
Углекислый газ
Метан
Этилен
Капиллярный
»
Свободное падение То же ... . Вращение диска Капиллярный .
Шариковый . .
» . .
Капиллярный .
Вращение диска Капиллярный .
>,итера-
тура
| Продолжение таб. VI. 23 | ||
|
Метод исследования | Литера | |
| Г аз | тура | |
| Этан |
Шариковый ...... | IV. 130 |
| Пропан |
» ...... | IV. 128 |
| » ...... | IV. 130 | |
| IV. 100 | ||
| Капиллярный ..... | IV. 108* | |
| Изобутан |
Шариковый...... | IV. 126 |
| н-бутан |
» ...... | IV. 126 |
| Метан — пропан |
» ...... | IV. 100 |
| Природный газ | » ...... | IV. 127 |
| Природный газ с |
Капиллярный ..... |
IV.105* |
| большим содержанием С02 | IV.105* | |
|
Природный газ с | » ..... | |
| низким содержанием этана | ||
| Природный газ с |
» ..... | IV. 105* |
| высоким содержанием этана | ||
• Данные использованы для построения обобщенных диаграмм на рис. IV. 102, IV. 103.
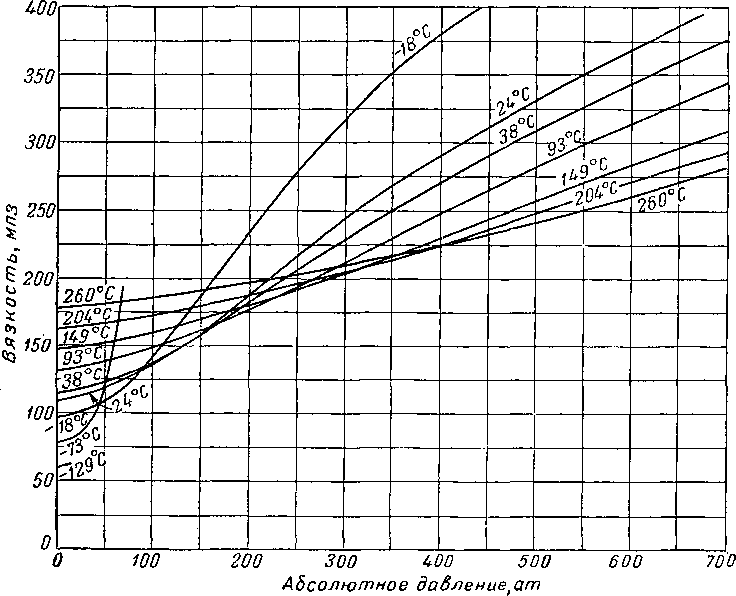
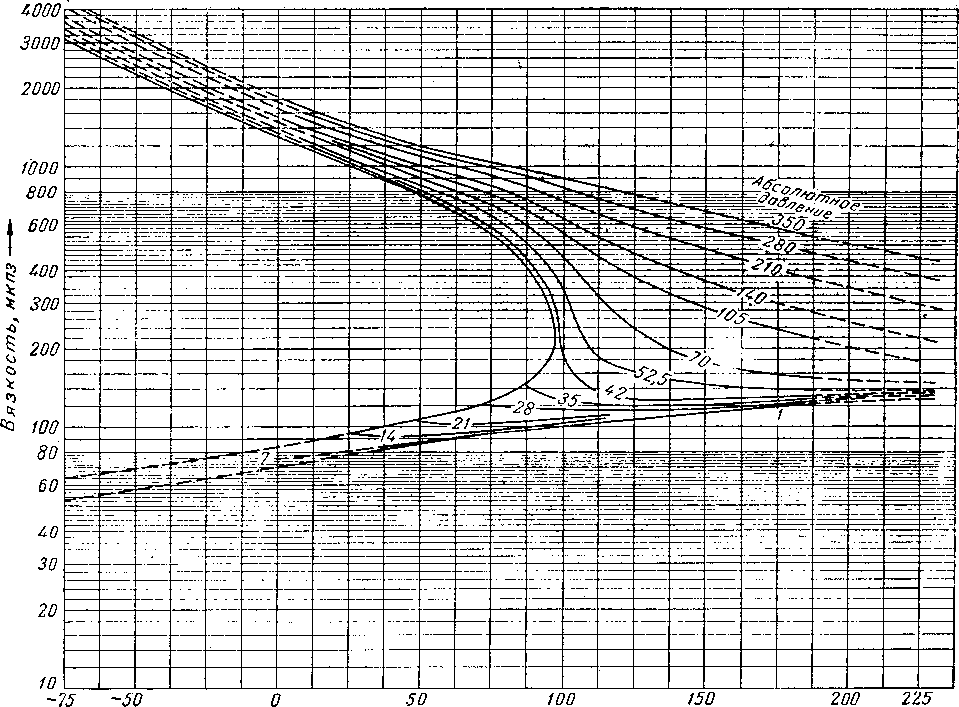
Т емпература,°С —
Абсолютное давление в am Рис. IV. 100. Вязкость пропана.
В работах Комингса, Мейланда, Эйгли (Commings, Mayland and Egly) [IV. 107, IV. 108] и Kappa (Carr) [IV. 104, IV. 105a] показано, что шариковый вискозиметр дает завышение вязкости примерно на 30%. По всем имеющимся данным с предпочтением тех, которые были получены на вискозиметре Ренкина, была дана зависимость вязкости метана (рис. IV. 99) и пропана (рис. IV. 100) от давления и температуры. На рис. IV. 101 представлены такие же данные Комингса, Мейланда и Эйгли (Egly) для этилена [IV. 108].
Еще в 1894 г. Оннес и Хаас (Onnes and de Haas) [IV. 120, IV. 121] указывали, что при соответствующих состояниях между вязкостями гомологов одного и того же ряда может быть установлено определенное соотношение. Впоследствии была сформулирована теорема соответственных состояний, примененная рядом авторов при обобщении данных о вяекости неполярных газов [IV. 130, IV. 108, IV. 106, IV. 100, IV. 107, IV. 137]. Ниже рассматривается только одно из таких обобщений.
На рис. IV. 102 и IV. 103 приводится диаграмма Карра [IV. 104, IV. 105], построенная на основании данных Комингса, Мейланда и Эйгли [IV. 108] для индивидуальных неполярных газов. Карр с соавторами распространил корреляцию Комингса с соавторами для условий более высокого давления и для сложных смесей неполярных газов [IV. 104, IV. 105, IV. 105а]. Отношение вязкости при высоком давлении к вязкости при атмосферном давлении выражается как функция приведенного давления рг и приведенной температуры Т.
Здесь
температура, °К г ~ критическая температура, °К ’ абсолютное давление Рг ~ абсолютное критическое давление ’
т] — вязкость газа при приведенной температуре Тг и приведенном давлении рг ;
и атмосферном
- вязкость газа при температуре Тг давлении.
Для смесей газов необходимо пользоваться псевдо-критическими давлениями и температурами, которые находятся из диаграммы на рис. IV. 22 по удельному весу смеси.
Уйехара и Ватсон [IV. 137] определяют приведенную вязкость 'Пг=гГ|(/1]С графически, причем в качестве переменных величин взяты приведенное давление и приведенная температура. Предлагается метод для определения критической вязкости т)с индивидуальных компонентов, а также рекомендуется способ определения ^ для смеси газов.
t>o|SN
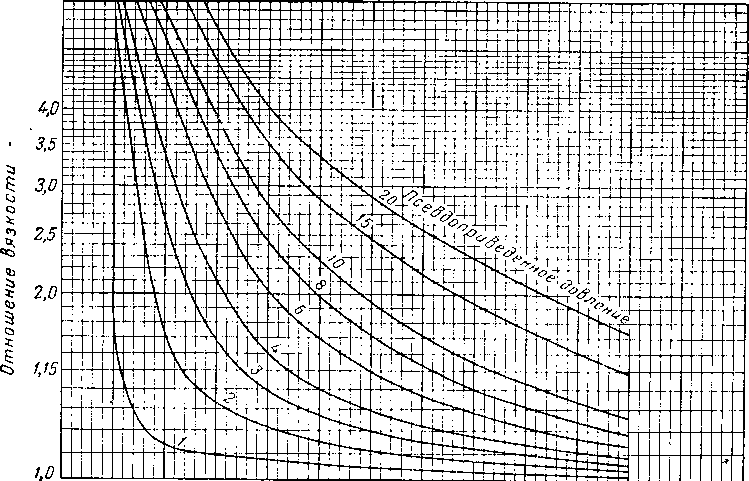
0,8 1,0 1,2 1,4 1,6 1,8 2,0 2,2 2А 2,6 2,8 3,0 3,2 ЗА
ЛсеВдоприВеденная температура Тг
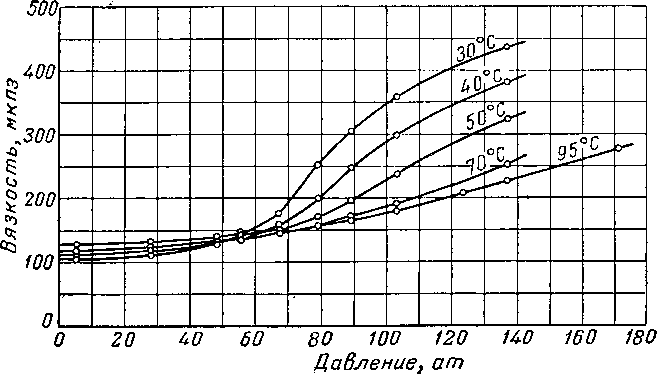
Рис. IV. 101. Вязкость этилена [IV. 108]. 6,0 5,0
Рис. IV. 102. Зависимость отношения вязкостей от приведенных температур [IV. 106].
Гранберг и Ниссам [IV. 110] предложили аналогичный метод специально для определения вязкостей чистых веществ в критической области. Смит и Браун [IV. 130], а также Бичер и Катц [IV. 100] представили абсолютную вязкость в виде функции приведенного давления, приведенной температуры и молекулярного веса.
Отношение вязкостей Vli успешно рассчитывается применением уравнения состояния Битти — Бриджмена [IV. 7] и уравнения состояния Бенедикта—Вебба—Ра-бина [IV. 10] к аналогии «кинетического давления» [IV. 102, IV. 104]. Эта аналогия утверждает, что
где ри — кинетическое давление или скорость переноса количества движения через единицу площади воображаемой поверхности внутри газа; pt — давление идеального газа, соответствующее объему идеального газа.
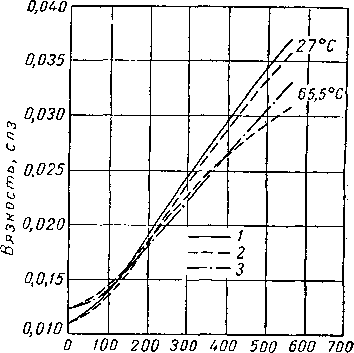
Абсолютное давление ,ат
Рис. IV. 104. Сравнение экспериментальных значений вязкости метана оо значениями, рассчитанными на основании кинетической теории.
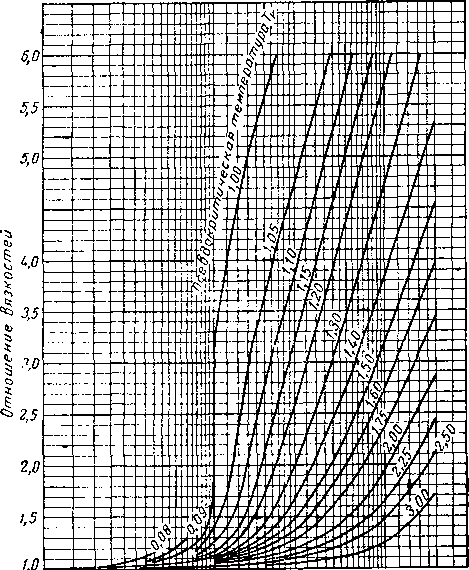
0,1 0,2 0,3 0,1* 0,6 0,8 1,0 2 3 4 56 8 10,0 20
ПсеВдоприВеденное давление рг
I — экспериментальные; 2 — по аналогии с кинетическим давлением; S — из рис. IV. 102 н IV. 103.
Рис. IV. 103. Зависимость отношения вязкостей от приведенных давлений Г1V. 106J.
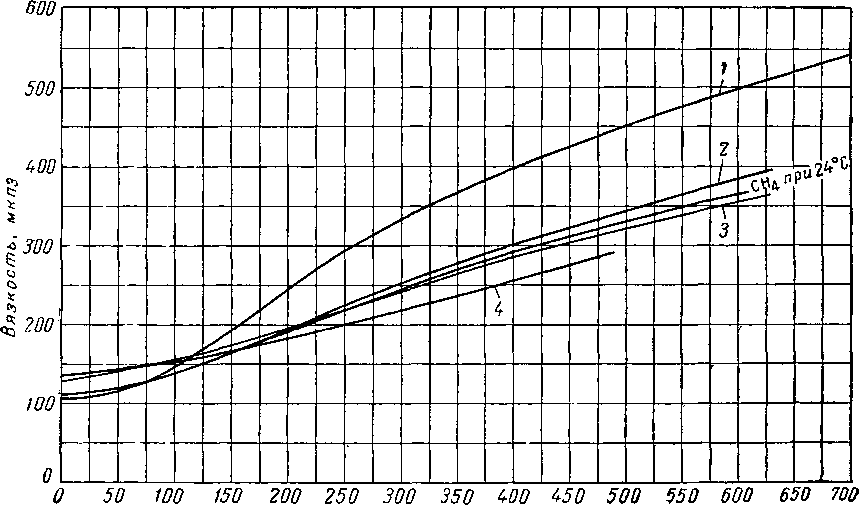
Рис. IV. 105. Вязкость природных газов [IV. 105].
I — газ в при 26° С; 2 — газ J при 29,5° С; 3 — газ Н при №,5° С; ^ г- газ J при 10i,5° С,
Вязкость у, спз
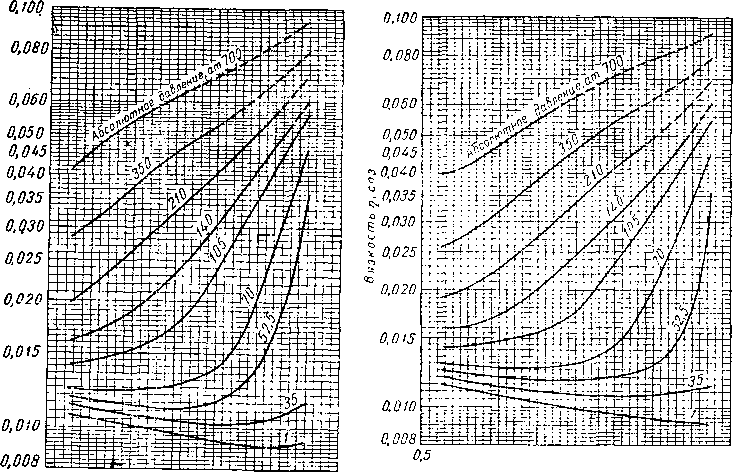
0,5 0,6 0,7 0,8 0,9 1,0 1,\
Удельный бес газа по боздуху
0,6 0,7 0,8 0,9 1,0 1,1 1,2
Удельный бес газа по воздуху 5
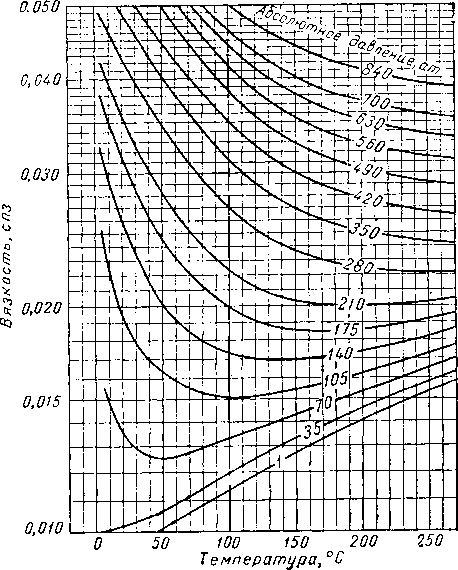
Температура, °С
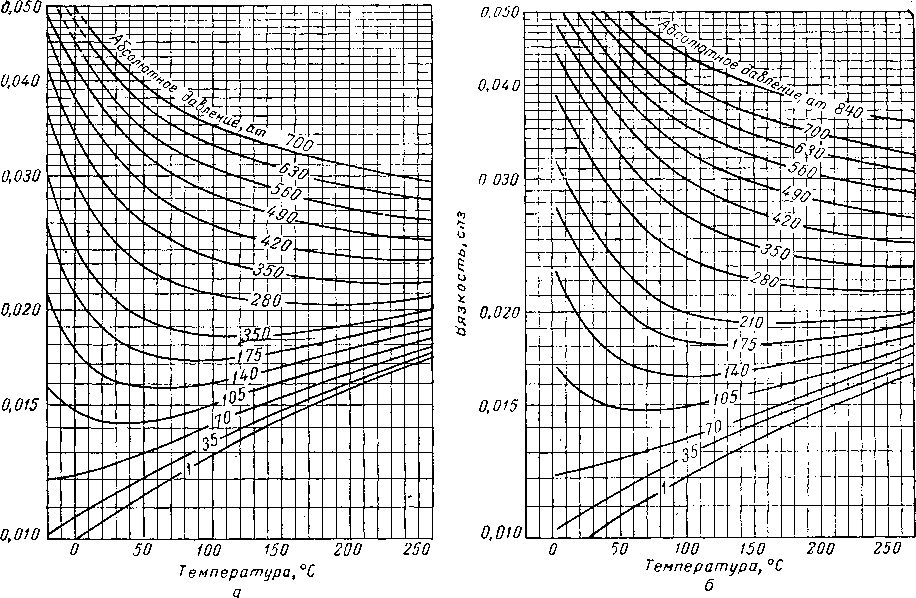
Вязкость, спз Вязкость, СПЗ
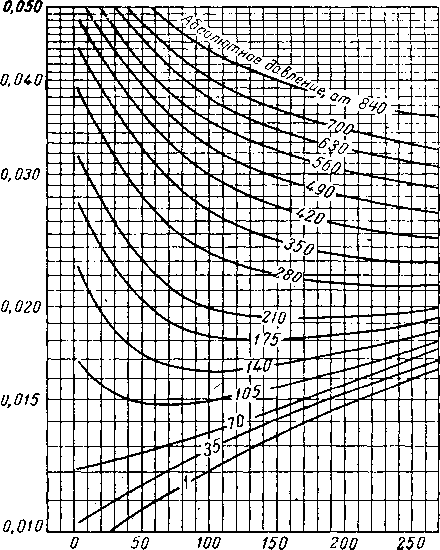
Рис. IV. 107. Вязкость природных газов [11.42]. а — удельный вес 0.6; б — удельный вес 0,7; в — удельный вес 0,8; г — удельный вес 1. в-420, 7 - 350; « — 280; 9 210; 19 — 175; Л — 140; 12 « 105; 13 — 70; 14— 35; 15— 1.
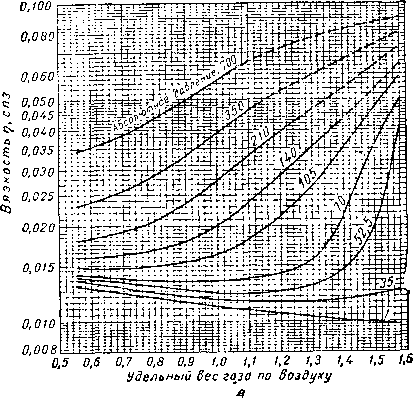
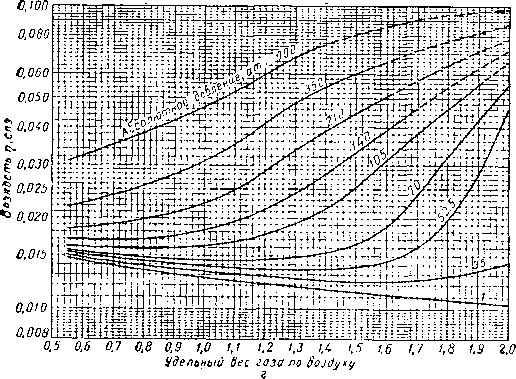
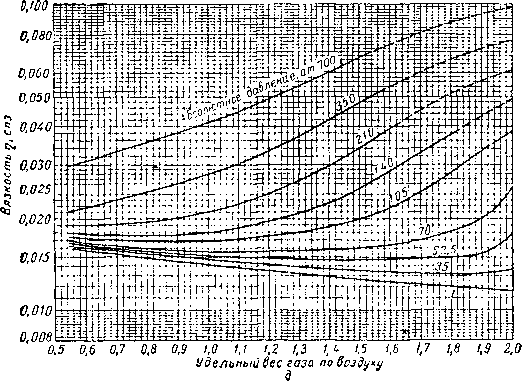
Рис. IV. 106. Вязкость природных газов. а — при 15,5° С; 6 — при 37,8° С; в — при 93,3° С; г при 149° С; д — при 204,5° С.
На рис. IV. 104 сравниваются экспериментальные значения вязкостей со значениями, рассчитанными по уравнению (IV, 50), в котором величина рк определялась из уравнения состояния Бенедикта — Вебба — Рубина.
На рис, IV, 105 даны значения вязкости трех природных газов при абсолютном давлении до 700 ат и двух температурах, полученные Карром (Carr) [IV. 105]. Состав этих газов приведен в табл. IV. 24.
Таблица IV. 24
Состав природных газов, данные вязкости которых приведены на рис. IV. 105
| Природный газ G | Природный газ Я |
Природный газ J | |||
|
компонент | % мол. |
компонент | % мол. | компонент]% мол. | |
|
Метан . . . | 73,5 |
Метан . . . | 73,1 | Метан , | 95,6 |
| Этан . . . |
25,7 | Этан , . , |
6,1 | Этан |
3,6 |
| Азот . . . | 0,6 | Азот . . . | 15,8 | Азот | 0,3 |
|
Пропан . . | 0,2 |
Пропан . . | 3,4 |
Пропан | 0,5 |
| Гелий . . . | 0,8 | ||||
| «-Бутан . . |
0,6 | ||||
| Изобутан . |
0,2 | ||||
На рис. IV. 106 приведены значения вязкости природных газов при температурах 15,5, 38, 93, 149 и 204° С в зависимости от их удельного веса. Зависимость вязкости газов удельного веса 0,6, 0,7, 0,8 и 1 от температуры и давления представлена на рис. IV. 107, Графики (рис. IV. 106 и IV. 107) построены на основании данных, приведенных на рис. IV. 102 и IV. 103, и могут быть использованы для определения вязкости смесей по удельным весам смесей газов, определяемым из рис. IV, 22.
Для газов, содержащих некоторое количество азота, углекислого газа или сероводорода, псевдокритические условия могут рассчитываться по составу газа. Далее, используя эти псевдокритические значения по рис. IV. 102 и IV. 103, можно определить вязкость. Если известен удельный вес газа и содержание неуглеводородного компонента, то по рис, IV. 108 [IV. 106] можно найти поправки к псевдокритическим температуре и давлению, определенным по рис. IV. 22, а затем воспользоваться графиками рис, IV. 102 или IV. 103 для определения вязкости газа.
Пример
Требуется определить вязкость природного газа удельного веса 0,702 при температуре 90° С и абсолютном давлении, равном 127.
Решение
Определяем псевдокритические параметры. Из рис. IV. 22 и далее находим следующие параметры.
Псевдоприведенное давление при абсолютном значении рс, равном
127
Ро = If = 2,72.
Псевдаприведенная температура при Тс, равном 217° К,
Из рис. IV, 103 для полученных значений рт и Тт находим т]/т]х = 1,28,
Из рис. IV. 97 для газа удельного веса 0,702 определяем, чтрт)3= 0,0122 спз.
m
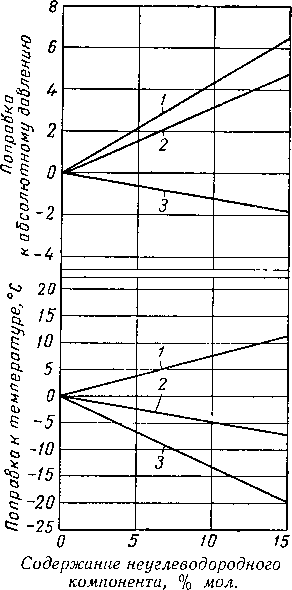
Рис. IV. 108. Поправки к псевдо-критическим давлениям и температурам, определяемым по рис. IV, 22, для газов, содержащих N2, СОг и H2S.
1 — сероводород; 2—углекислый газ;
3 — азот.
При температуре 90° С и абсолютном давлении, равном 127,
% = 0,0122 X 1,28 = 0,0156 спз.
Из графика на рис. IV, 107 для газа удельного веса 0,7 непосредственно находим вязкость, равную 0,0155 спз.
Из рис, IV. 106:
при температуре 93° С и абсолютном давлении, равном 127, % = 0,0157;
при температуре 38° С и абсолютном давления, равном 127, т] = 0,0163.
Путем интерполяции находим, что при температуре 90° С и абсолютном давлении, равном 127, вязкость газа составляет 0,0158 спз.
з. вязкость жидкостей
Вязкость жидкостей с ростом температуры уменьшается, а с ростом давления, наоборот, увеличивается. На рис. IV. 109 представлены значения вязкости индивидуальных соединений, определенные Американским нефтяным институтом [I, 15]. Хокотт и Бакли (Hocott and Buckley) [IV, 112] измеряли вязкость нефтей, содержащих растворенный газ (рис, IV, 110), Состав насыщенных нефтей, взятых ими для исследований, приведен в табл, IV. 25, Седж, Леси [IV. 125; IV, 126; IV. 128] и другие авторы [IV, 138а] исследовали вязкость жидкостей при различных давлениях.
Бил (Beal) обобщил данные о вязкости различных нефтей. На рис. IV. 111 представлена зависимость вязкости разгазированных нефтей от удельного веса, а на рис. IV. 112 показано влияние на вязкость пластовой нефти растворенного в ней газа.
На рис. IV. 113 показано повышение вязкости для жидкости постоянного состава на каждые 70 ат увеличения давления.
5
<Г 1 5
сэ
*
§
%
5 ' !
Иногда вязкость нефтей выражают в секундах Сейболта при данной температуре. В табл. IV. 26 [IV. 2] приведены значения вязкости по Сейболту и соответствующие им значения кинематической вязкости в сантистоксах. Кинематическая вязкость, выраженная в сантистоксах, деленная на плотность жидкости (г/см3), дает вязкость, выраженную в сантипуазах.
Рис. IV. 110. Вязкость глубинных проб нефти [IV. 112, IV. 99].
Г — газовый фактор м*/м*; рн —плотность нефти вг/сл8? Тр “* УДельный вес газа. 1 — пермские отложения (Западный Техас); 2 — лесчаник Фрно (Глоф Кост); 5 —Пало Пинто (известняк. Северный Техас)*. 4 — песчаник Фрио (Юго-Западный Техас),
|
1 | 1 1 | ||||||||
| 1 |
§ 1 | n | «781, | ||||||
| \ |
31 | ||||||||
| \ |
|||||||||
| 5-. | |||||||||
|
ч SI | H | -2 | |||||||
| ч | •is ft* S3 | 3°C:! |
'=52,1 | ;S>h=C |
,818; | >=r,f |
7 ? | ||
| I 1 Давление насыщен |
ия | ||||||||
| Г-777Г---1_‘_1 ¦ — ' | “ =« 788; fr=0,84 | | — 6- |
||||||||
•o'
6
(J
о
V
"3
«tj

Рис. IV. 109. Вязкость жидких углеводородов [I. 15].
150 200
50 100 150 200
Нефть А
Нефть В
Нефть С
Нефть D
молекулярный вес
молекулярный вес
молекулярный вес
молекулярный вес
удельный вес
весовые %
удельный вес
весовые %
весовые °/
весовые %
удельный вес
удельный вес
0,83
1,41
0,71
0,42
0,97
1,17
0,28
1,64
92,57
4,38
1,05
0,35
0,11
0,05
0,34
93,72
7,93
1,65
1,80
0,84
1,42
1,07
1,23
3,64
80,42
1.50 0,93 3,42 0,83
3.51 1,40 2,24 4,02
82,15
0,8896
0,8076
250
229
0,8974
215
147
0,8418
100,00
100,00
100,00
100,00
Метан . . Этан . . . Пропан . . Изобутан . и-Бутан Изолента н н- пентан . Гексаны .
Более тяжелые фракции
Вязкость нефти при атмосферном давлении и 70° С равна 0,950 спз
Вязкость нефти при атмосферном давлении и температуре 53° С равна 1,84 спз
Вязкость нефти при атмосферном давлении и температуре 73° С равна 5,4 спз
Вязкость нефти при атмосферном давлении и температуре 38° С равна 8,25 спз
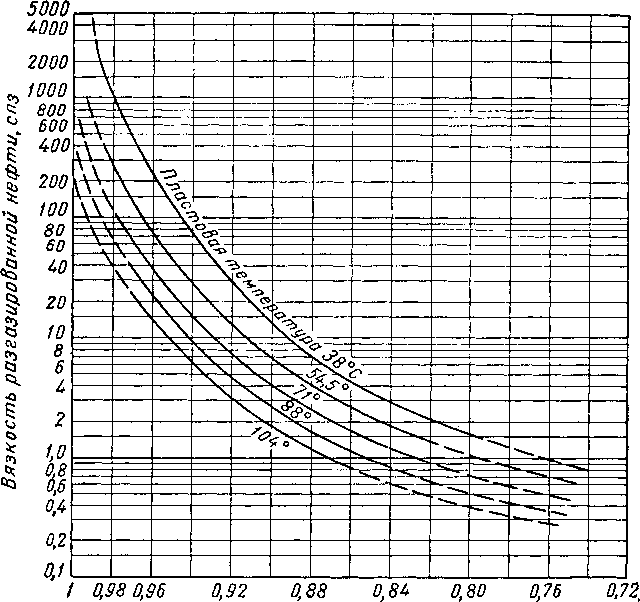
Плотность нефти при 15,5°С и атмосферном давлении Рис. IV. III. Вязкость разгазированных нефтей [IV. 99].
О 25 50 75 100 125 150 175 200 225 250
А О
Количество растворенного 8 нефти газа при пластовом давлении, м/м
Рис. IV. П2. Влияние растворенного газа на вязкость пластовой нефти [IV. 99]. Цифры на кривых —¦ вязкость разгазированной нефти при пластовой температуре в спз.
Таблица IV. 26 Перевод вязкости по Сейболту в кинематическую вязкость
| Кинемати ческая вязкость, сст |
Вязкость по Сейболту, сек | Кинемати ческая вязкость, сст |
Вязкость по Сейболту, сек | ||
| при 38е С | при 99° С | при 38° С | при 99* С | ||
| 2 |
32,6 | 32,9 | 15 |
77,4 | 77,9 |
|
3 | 36,0 | 36,3 |
20 | 97,8 | 98,5 |
| 4 | 39,1 |
39,4 | 25 | 119,3 |
120,1 |
| 5 |
42,4 | 42,7 | 30 |
141,3 | 142,3 |
|
6 | 45,6 | 45,9 |
35 | 163,7 | 164,9 |
| 7 | 48,8 |
49,1 | 40 | 186,3 |
187,6 |
| 8 |
52,1 | 52,5 | 45 |
209,1 | 210,5 |
|
9 | 55,5 | 55,9 |
50 | 232,1 | 233,8 |
| 10 | 58,9 |
59,3 | |||
Рис. IV. ИЗ. Влияние давления на вязкость пласто-. вых нефтей постоянного состава при постоянной температуре [IV. 99].
Поправка к вязкости нефти при давлении насыщения при увеличении давления на каждые 100 am, СПЗ
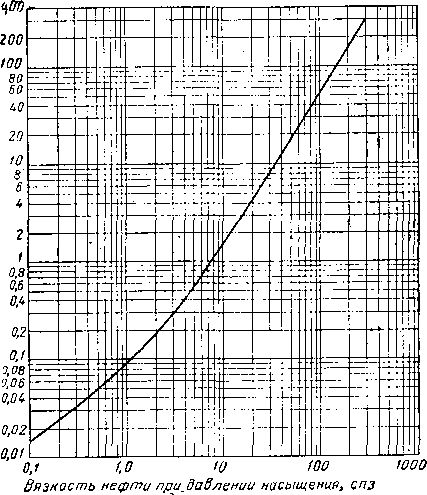
Таблица IV; 27
Экспериментальные значения теплопроводностей газов при атмосферном давлении
§ 7. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ
Теплопроводность является основным физическим свойством вещества, определяющим скорость переноса тепла, и выражается уравнением Фурье, выведенным первоначально для твердых тел:
ял —
dt ~ дл dx ’
dQ
где —перенос тепла только посредством проводимости в кал]сек; К — коэффициент теплопроводности ве-кал 1 см
щества в —— X —i X А — площадь, перпендикуляр-
сак см v_>
ная направлению потока тепла, в см"1; х — расстояние в см; Т — температура в СС.
В данном параграфе рассматривается зависимость теплопроводности индивидуальных газов от давления и температуры. Для определения теплопроводности смесей газов приводятся лишь ориентировочные корреляции, так как отсутствуют экспериментальные данные для природных газовых смесей.
Имеется лишь небольшое количество экспериментальных данных, касающихся теплопроводности индивидуальных компонентов, обычно входящих в состав природных газов.
1. ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ
При экспериментальном определении теплопроводности газов обычно пользуются различными модификациями формулы (IV. 51), подставляя в нее эксперимен-
dQ
тально измеренные поток тепла расстояние распространения тепла х и температуры Т. Наиболее общей методикой определения теплопроводности является «метод нагретой проволоки» Шлаермахера (Schleiermacher) [IV. 175], сущность которого состоит в измерении количества тепла, выделяемого при пропускании электрического тока по проволоке, натянутой вдоль оси цилиндрической трубки. Газ, чья теплопроводность должна быть измерена, помещается в кольцевое пространство между проволокой и внутренней стенкой трубки.
В табл. IV.27 приведены значения теплопроводности индивидуальных углеводородов, азота, углекислого газа и гелия при атмосферном давлении, а в табл. IV. 28 приводится литература по вопросу теплопроводности некоторых газов при высоких давлениях.
2. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ ПРИ ВЫСОКИХ ДАВЛЕНИЯХ
Оценка влияния давления на теплопроводность газов сделана Энекогом (Enskog) [IV. 145]. Комингс и Натан (Comings and Nathan) [IV. 140], пользуясь уравнениями Энскога, рассчитали теплопроводность индивидуальных газов при высоких давлениях для известных значений их вязкости и плотности. Позднее Линоир, Джанк и Комингс (Lenoir, Jung and Comings) [IV. 167] измерили и обобщили теплопроводность индивидуальных неполярных газов в зависимости от давления и температуры. На рис. IV. 114 и IV. 115 представлена зависимость отношения теплопроводностей от приведенных давления и температуры по экспериментальным данным, в основном взятым из работ, указанных в табл. IV. 28. Отношение теплопроводностей определяется как отношение теплопроводности газа при данной температуре и высоком давлении к теплопровод-
(IV. 51)
| Газ | Температура эксперимента, °С | ka ¦ 10». кал | Литера тура |
|
см-сек-° С | |||
|
Метан | 0 |
IV. 181 | |
| 0 |
6,89 | IV. 191 | |
| 7 | — |
IV. 192 | |
| 0 и 100 | 7,493 | IV. 194 | |
| — 182, —76 и 0 | 7,145 | IV. 147 |
|
| 0 | 7,145 |
IV. 171 | |
| 0 | 7,200 | IV. 189 |
|
| 0 и 10 |
7,210 | IV. 169 | |
| 0 | 7,205 |
IV. 186 | |
| От —176 до 4-110 | 7,336 |
IV. 156 | |
| 41 | — | IV. 166 |
|
| От 100 до 500 |
— | IV. 176 | |
| 53 | — |
IV. 167 | |
| 53, 150, 250 и 300 | — |
IV. 161 | |
| Этан | 0 и 100 | 4,981 |
IV. 194 |
| —70, —38 и 0 | 4,260 | IV. 147 | |
| 0 и 100 | 4,306 | IV. 171 |
|
| 0 и 10 |
4,360 | IV. 169 | |
| 42, 57 и 67 |
•.—. | IV. 167 | |
| 52 | — |
IV. 161 | |
|
Пропан | 0 и 10 |
3,600 | IV. 169 |
| 0 | 3,549 |
IV. 186 | |
| к-Б у тан | 0 и 10 |
3,220 | IV. 169 |
|
к-Пентан | 0 и 20 |
2,933 | IV. 171 |
| 0 | 3,120 |
IV. 169 | |
|
к-Гексан | 0 и 20 |
2,604 | IV. 171 |
| 0 | 2,96 |
IV. 169 | |
|
к-Гептан | 100 | IV. 171 | |
|
Изобутан | 0 и 10 |
3,32 | IV. 169 |
| Изопентан | От 0 до 178 | 2,912 | IV. 171 |
| Этилен |
0 | IV. 181 |
|
| 0 | 4,53 |
IV. 191 | |
|
От 0 до 100 | — |
IV. 193 | |
| 0 | _ | IV. 144 |
|
| 0 | 4,02 |
IV. 163 | |
| —70, —38 и 0 | 4,07 | IV. 147 | |
| 0 |
4,07 | IV. 171 | |
| 42 и 67 | — | IV. 166 | |
|
72 и 152 | — |
IV. 161 | |
|
Углекислый | 0 | IV. 181 | |
|
газ | 0 | _ | IV. 164 |
|
0 | 3,55 | IV. 191 | |
| 0 |
— | IV. 193 | |
| 0 | 3,091 |
IV. 150 | |
| От 0 до 100 | 3,27 | IV. 174 | |
| 0 |
..—. | IV. 144 | |
| 0 | 3,07 |
IV. 192 | |
| От —78 до 0 | 3,434 |
IV. 143 | |
| 55 | — | IV. 184 |
|
| От 22 до 546 |
_ | IV. 180 | |
| —78, 0 и 100 |
3,37 | IV. 146 | |
| 0 | 0,34 |
IV. 171 | |
| 0 |
3,393 | IV. 189 | |
| От 0 до 13 |
3,604 | IV. 151 |
| Газ | Температура эксперимента, °С | *о ' I»*- кал см • сек • ® С | Литера тура |
| Углекислый |
0 | 3,44 | IV. 190 |
| газ |
От 0 до 13 | 3,375 |
IV. 186 |
|
0 | 3,43 | IV. 158 | |
| От 0 до 320 | 3,47 | IV. 139 | |
| От —87 до 110 | 3,485 | IV. 156 | |
| От 0 до 600 | 3,50 | IV. 188 | |
| От 0 до 1000 | 3,57 | IV. 183 | |
| 42, 57 и 67 | — | IV. 166 | |
| От 32 до 65 |
— | IV. 165 | |
| От 0 до 777 |
3,50 | IV. 173 | |
| Галий | 0 |
33,86 | IV. 177 |
| От —252 до +100 |
33,60 | IV. 147 | |
| 0 | 33,60 |
IV. 171 | |
|
0 | 34,38 | IV. 180 | |
| 0 |
— | IV. 148 | |
| 0 | — | IV. 141 | |
|
От —193 до +110 | 33,90 |
IV. 156 | |
|
43 | — | IV. 166 | |
| Азот |
8 | _ | IV. 192 |
| 0 |
5,694 | IV. 153 | |
| 55 | — | IV. 184 | |
|
От—191 до +100 | 5,68 |
IV. 146 | |
|
0 | 5,68 | IV. 171 | |
| 0 |
5,66 | IV. 189 | |
| От 5 до 13 |
5,80 | IV. 152 | |
| 0 | 5,81 |
IV. 142 | |
|
От 0 до 45 | 5,72 |
IV. 188 | |
| От 0 до 1000 | 5,77 | IV. 183 | |
| От 0 до 400 | 5,816 | IV. 162 | |
| 42 |
— | IV. 166 | |
| 0,50 и 150 |
5,74 | IV. 160 | |
| От 100 до 200 |
— | IV. 176 | |
| От 32 до 65 |
— | IV. 165 | |
| 53 | _ |
IV. 167 | |
|
От 0 до 777 | 5,76 |
IV. 173 |
Таблица IV. 28
Экспериментальные работы по определению теплопроводности газов при высоких давлениях
| Газ | Литература | Газ |
Литература | ||
|
Метан | IV. |
182 | Гелий |
IV. | 166 |
| IV. | 166 |
||||
|
IV. | 167 |
Аргон | IV. |
166 | |
| IV. | 161 | IV. |
167 | ||
| IV. |
187 | ||||
| Этан |
IV. | 167 | |||
| IV. | 161 | Азот |
IV. | 182 | |
| IV. | 162 | ||||
|
Этилен | IV. |
166 | IV. |
166 | |
| IV. | 161 | IV. | 160 | ||
|
IV. | 178 |
IV. | 157 | ||
| IV. |
170 | ||||
|
Углекислый | IV. |
182 | IV. |
167 | |
| газ | IV. | 166 |
|||
|
IV. | 160 | ||||
| IV. | 157 | ||||
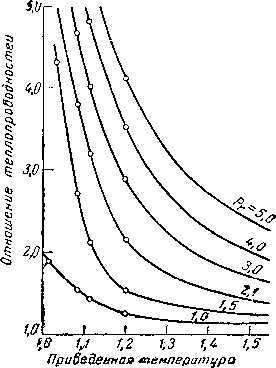
Рис. IV. 114. Зависимость отношения теплопроводностей от приведенной температуры
[IV. 167].
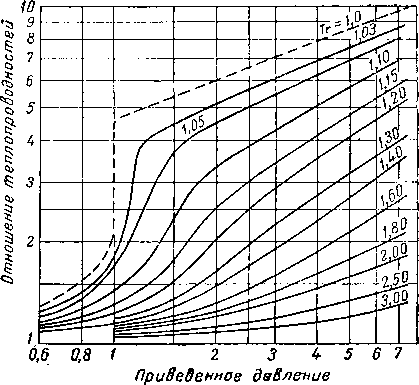
Рис. IV. 115. Зависимость отношения теплопроводностей от приведенного давления [IV. 167].
ности при той же температуре, но при атмосферном давлении.
Гамсон (Gamson) [IV. 149] построил зависимость приведенной теплопроводности газа от приведенных давления и температуры.
Приведенная теплопроводность определяется как отношение теплопроводности при давлении и температуре опыта к теплопроводности при критических условиях. Для смесей газов применяются среднемолярные значения критических давлений, критических температур и критических теплопроводностей входящих в смесь компонентов.
| 70 | |
| > | 60 |
|
* 4? | 50 |
| СЭ С> |
40 |
| «а ? са | за |
| § ? |
го |
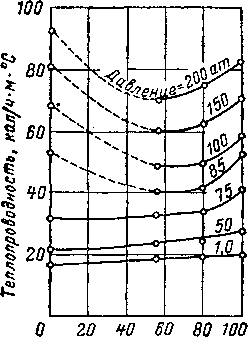
Содержание этилена,%
Су +
К-
(IV. 53)
(С + 5-«),
+ 4М/
(IV. 54)
Рис. IV. 117. Теплопроводность смесей СО2 — С2Н4 [IV. 1571.
Рис. IV. 116. Теплопроводность смесей N2 — С2Н4 [IV. 157].
Джанк и Комингс [IV. 167] нашли, что средняя ошибка опытов при определении теплопроводности системы азот — этилен (рис. IV. 114) составляет 5%, а для системы углекислый газ — этилен эта ошибка равна 36%.
Можно было бы привести и другие примеры, когда теплопроводность газов, определенная экспериментально, не совпадала с теплопроводностью, найденной по обобщенному графику. Так, найдено, что экспериментальные значения отношения теплопроводностей для этана, полученные Лилоиром, Джанком и Комингсом [IV, 167], на 30% ниже, чем по данным обобщенного графика. С другой стороны, теплопроводность этилена
Известно несколько работ по исследованию теплопроводности смесей газов при высоких давлениях. На рис. IV. 116 и IV. 117 представлены графики зависимости теплопроводности смесей азот — этилен и углекислый газ — этилен при температуре 42°С для разных значений давления [IV. 157]. Эти данные при сравнении с обобщенным графиком показывают, что значения теплопроводности смеси газов определяются с меньшей степенью точности, чем значения вязкости. Линоир,
|
л /к/ /ы Г чу | ||||
|
i | ||||
| а/ | ||||
| л | ||||
| rd |
У |
> | ||
| 1— | f.o |
|||
О 20 4-0 60 80 WO Содержание этилена, %
находится в хорошем соответствии с данными для других газов, исследованных в работах, упомянутых в табл. IV. 28.
Возможные доводы о неприменимости приведенных давления и температуры в качестве коррелирующих параметров с точки зрения кинетической теории обсуждались Линоиром, Джанком и Комингсом (Lenoir, Jung and Comings) [IV. 167], Пиддаком (Pudduck) [IV. 172] и Юкеном (Eucken) [IV. 147]. Несмотря на то. что обобщение, приведенное в данной работе, и обобщение Гамсона (Gamson) [IV. 149] не дают возможности сопоставить все неполярные газы (см. этан) и смеси газов (см. углекислый газ—этилен), в настоящее время использование этих обобщений является единственным средством практической оценки влияния .давления на теплопроводность газов.
Значения приведенных давлений и приведенных температур подсчитываются в соответствии с определениями, изложенными в разделе, касающемся вязкости газов.
3. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ ПРИ ДАВЛЕНИЯХ, БЛИЗКИХ К АТМОСФЕРНОМУ
В настоящее время имеется небольшое количество экспериментальных работ, посвященных определению теплопроводности индивидуальных газов и природных смесей газов при давлениях, близких к атмосферному. Это обстоятельство заставило прибегнуть к применению для этих целей теоретических уравнений, справедливых для неполярных газов. Эти уравнения были выведены применительно к углеводородам парафинового ряда.
Чапман и Каулинг (Chapman and Cowing) [IV. 24] и Юкен (Eucken) [IV. 147] дали соотношение, связывающее теплопроводность обычных газов с их вязкостью и теплоемкостью при постоянном объеме. Соотношение Чапмана и Каулинга, предполагающее, что молекулы представляют собой жесткие шары, имеет следующий вид:
К = hCv, (IV. 52)
где ^^теплопроводность; f—постоянная величина, равная 2,5 для гладких шарообразных симметричных молекул и 2,522 для молекул, представляющих собой жесткие эластичные шары; il —вязкость; С (/ — теплоемкость при постоянном объеме.
Это соотношение успешно применялось для определения теплопроводности газов, составленных из несложных молекул, по данным их вязкости и теплоемкости при постоянном объеме.
Уравнение Юкена [IV. 155, IV. 154] для определения теплопроводности газов по значениям их вязкости и теплоемкости имеет вид:
где К — теплопроводность в кал[см ¦ сек• °С; Н, V — слождые коэффициенты взаимодействия между парами молекул, R — газовая постоянная в кал/моль-°С\ М — молекулярный вес; т| — вязкость в г/см • сек; Cv—молярная теплоемкость при постоянном объеме в кал/моль • °С.
Если в уравнение [IV.53] вместо Су подставить его значение, найденное из соотношения Cv — Cv = то уравнение примет вид:
где Ср—теплоемкость в кал/г • °С.
Н у] V М
Рис. IV. 118. Зависимость /
величины у от температуры.
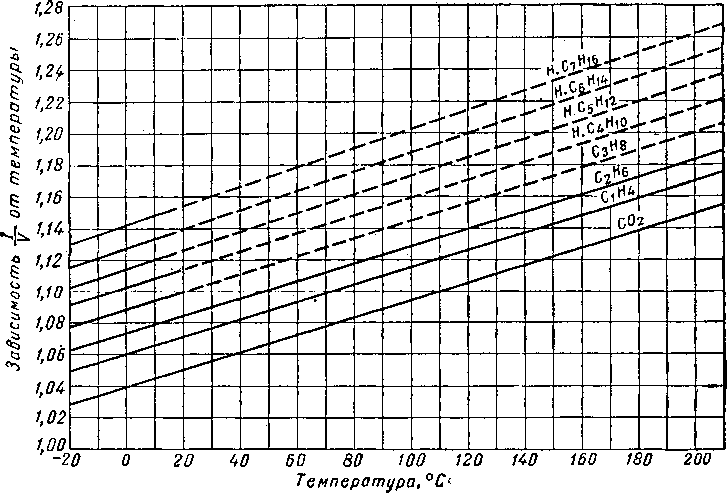
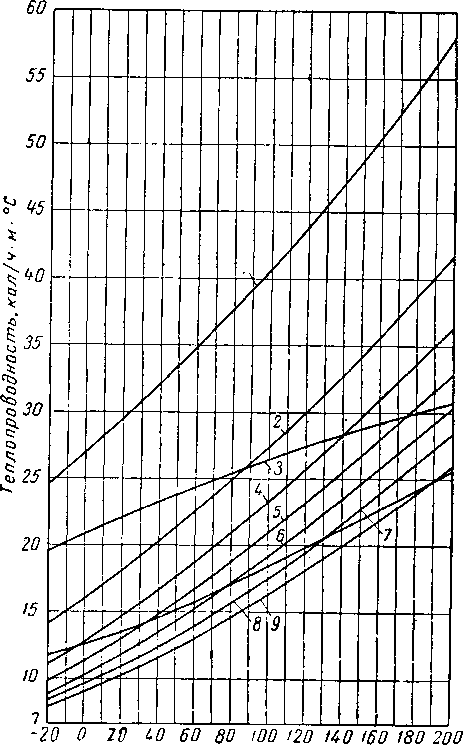
висимость
V
Т е мпература, °С
Значение у подсчитывается из уравнения [IV. 54]
по экспериментально определенному значению тепло-
Н
проводности. При этом значения у, рассчитанные
подобным образом, не соответствуют значениям этой величины, полученным из молекулярной теории [IV. 154]. Н
Рассчитанные значения -у для углекислого газа, метана
и этилена зависят от температуры и природы газа. Для азота в интервале температур от минус 75 до 200° С это значение равно примерно 1,0. На рис. IV. 118 при-
Н
ведены графики зависимости величины у от температуры для различных газов, необходимые при расчетах теплопроводности газов. Ввиду того, что теплопроводность пропана и углеводородных газов более высокого молекулярного веса экспериментально измерена лишь
г!
в узком пределе температур, величина р линейно
экстраполирована от значений в пределе 0—20° С. Предположено, что наклон линий, представляющий за-Н
чистого метана и углекислоты.
После того как были сделаны приведенные выше расчеты, было выведено следующее соотношение для легких углеводородных газов:
МК
— = 1,04 + 1,29С„,
•Г] 1 Р’
где М — молекулярный вес в г; К — теплопроводность в кал/см ¦ сек °С\ т}—вязкость в г/см- сек; Ср — теплоемкость в кал/моль ¦ °С.
Значения теплоемкости, использованные для вычисления теплопроводности, взяты из работы, выполненной в Американском нефтяном институте [I. 15]. Значения вязкостей газов взяты из соответствующего раздела
Рис. IV. 119. Теплопроводность газов при атмосферном давлении.
/ — метан; 2— этан; 3 — азот; 4— пропан: 5 — «-бутан:
6 — «-пентан: 7 — углекислый газ; 8 — (к-гексан; 9 -* д-гептан.
от температуры, тот же, что наклон для
to
•. чо *
§
6
<J
1
"I 30 &
I ?
25
60
+
¦И
1 +
*1,2
Рис. IV. 120. Рассчитанные значения теплопроводности бинарных смесей газов при 12Г С. книги. На рис. IV. 119 приведены значения теплопроводности индивидуальных углеводородных газов. На рис. IV. 121 значения теплопроводности для различных температур даны в виде зависимости от молекулярного веса.
Для определения теплопроводности смесей газов по значениям теплопроводностей входящих в смесь компонентов некоторыми авторами [IV. 24, IV. 41, IV. 159, IV. 168] были предложены аналитические выражения. Соотношение, выведенное Линдсеем и Бровли (Browley) [IV. 168], было с успехом применено для вычисления теплопроводности газовых смесей. Это соотношение выражает теплопроводность смеси как функцию теплопроводностей, вязкостей, молекулярных весов и коистаит Сатерленда индивидуальных компонентов, входящих в смесь, а также состава газа и температуры.
Теплопроводность газовой смеси /Сем может быть определена по формулам (IV. 55) и (IV. 56). По формуле (IV, 56) подсчитываются значения А, которые затем подставляются в формулу (IV. 55).
К,- =-:-^----+
*8 *8
где /(i, Кг, Кз... — теплопроводности индивидуальных компонентов, xi, хг, х3 ... — молярные доли компонентов. Если Aii = Aix то
Ъ (Мг\Ч* 1+SJT Щ 1 + Sl-a/r
I l+s^r '
(IV. 56)
где ij — вязкость; М —¦ молекулярный вес; S — константа Сатерленда (табл. IV. 29); ?[ 9= (SiS2)>/г; Т — абсолютная температура в °К.
21
|
СНй \ | ||||
| V | ||||
|
V' \у | i\ \\ | |||
| \\\ \\ \> Сз | \ к \ | |||
| ^Чх CiHio |
_ Кг__
1 + Аа. 1* + Л2. з * + а2. 4 7* + • • •
*1 ДГв . Ха
1 +'А3. 1^г + А3, 2Z + А3.4Хл + -
/0 20 30 40 50
Молекулярный бес
+
Таблица IV. 29 Значения констант Сатерленда для газов
| Г аз | г, °к |
Литера тура |
|
198 | IV. 124 | |
| 287 | IV. 132 | |
| Пропан........ |
341 | IV. 132 |
| 377 | IV, 132 | |
| н-Пентан ....... |
382,8 | IV. 132 |
| н-Гексаи ........ |
436,1 | IV. 132 |
| 102,7 | IV. 185 | |
| Углекислый газ .... | 274 | IV. 179 |
10 20 30 40 50 60 70 80 90 100 НО Молекулярный Вес
Рис. IV. 121. Зависимость теплопроводности газов от их молекулярного веса.
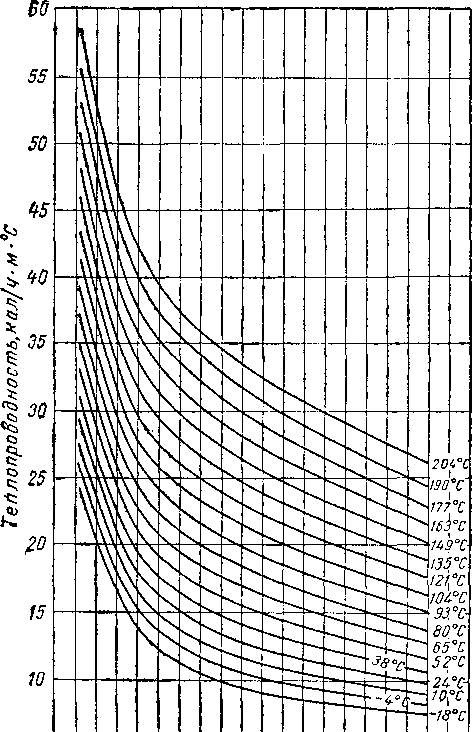
По уравнению (IV. 55) были определены теплопроводности искусственных смесей. При этом предполагалось, что константы Сатерленда не зависят от температуры, хотя фактически они для реальных газов изменяются при изменении температуры. Было установлено, что сравнительно большое изменение констант Сатерленда приводит к небольшому изменению рассчитываемых значений теплопроводности.
Рассчитанные значения теплопроводности некоторых бинарных углеводородных смесей при 120° С приведены на рис. IV. 120. Сравнение кривой, приведенной на рис. IV. 121, при соответствующей температуре 120° С с кривой, изображенной на рис. IV. 120, показывает степень приближения, с которой определяется теплопроводность сложных смесей непосредственно по значениям молекулярных весов этих смесей.
Расчеты показывают, что природные газы, содержащие в своем составе до 35% азота и углекислого газа (или одного из этих газов), вполне соответствуют кривым, приведенным на рис. IV. 121. Вообще использование кривых, приведенных на рис. IV. 121, для природных углеводородных смесей дает малоколеблющиеся значения теплопроводности.
Уравнения (IV. 55) или (IV. 56) вместе со значениями отношения теплопроводностей, полученными из рис. IV. 114 или IV. 115, могут быть использованы для определения абсолютных значений теплопроводностей газов высокого давления.
Вопрос о теплопроводности жидкостей здесь не рассматривается. В табл. IV. 30 приведены значения теплопроводностей лишь некоторых жидких углеводородов и воды.
Таблица IV. 30 Теплопроводности жидкостей
| Жидкость |
Температура, °С |
Теплопроводность, К •' Ю—\ кал/см-сек’° С |
|
Вода | 0 |
1,405 |
| 38 | 1,487 | |
|
93 | 1,610 | |
| 149 | 1,619 | |
| н-Пентан |
30 | 0,320 |
| 75 | 0,303 |
|
| н-Гептан |
30 | 0,332 |
| 60 | 0,324 |
|
| Нонан | 30 | 0,344 |
|
60 | 0,336 | |
| Газолин | 30 |
0,320 |
|
Керосин | 20 |
0,352 |
| 75 |
0,332 | |
|
Этиленгли- коль |
0 | 0,628 |
| Примечание. Данные взяты |
из [IV. 121а]. | |

