Влагосодержание природных газов
ГЛАВА V
ВЛАГОСОДЕРЖАНИЕ ПРИРОДНЫХ ГАЗОВ
Вода содержится в природном газе на всем пути его движения, начиная от пласта до потребителя. Особенно нежелательно, чтобы в природном газе при высоких давлениях находилась вода.
Давление способствует образованию соединений воды с природным газом в виде твердых газовых гидратов при положительной температуре. Образование газовых гидратов, напоминающих мокрый снег, должно быть устранено, поскольку они нарушают режим работы трубопроводов.
Для инженера представляют интерес сведения
о равновесном содержании воды в природных газах при различных температурах и давлениях, а также условия, при которых образуются гидраты.
Данные о содержании воды в природных газах позволяют определять количество воды, которое должно быть удалено при обезвоживании газа, чтобы в газопроводах при транспорте газа не наблюдалось конденсации паров воды. Поскольку небольшие количества воды, растворяемые в пропане, бутане и других легких углеводородных жидкостях также должны быть удалены, необходимо знать их влагосодержание.
Понимание физико-химических соотношений, определяющих поведение структур, содержащих углеводороды и воду, помогает инженеру в решении проблем, связанных с контролем содержания влаги в природных газах и легких углеводородных жидкостях.
Количественный анализ содержания воды в газах и углеводородных жидкостях необходим для решения многих инженерных задач. Сведения о природе газовых гидратов и равновесных условиях, при которых они образуются в присутствии воды, позволяют определить для влажных природных газов температуру и давление, при которых не происходит образования гидратов. Поскольку измерения точки росы паров воды и определение абсолютного содержания воды в природных газах имеют большое значение, методика ее определения рассматривается в данной главе и во многих работах Катца, Рзаса (Katz and Rzasa) [1.9] и Дитона и Фроста (Deaton and Frost) [I, 21].
§ I. ОСНОВНЫЕ ФАЗОВЫЕ СООТНОШЕНИЯ СИСТЕМ УГЛЕВОДОРОДЫ —ВОДА
Бинарные системы воды и одного чистого углеводорода представляют собой простейшие фазовые соотношения в системах вода — углеводород. Эти системы при температурах выше 0° С будут рассмотрены перед тем, как перейти к более сложным системам.
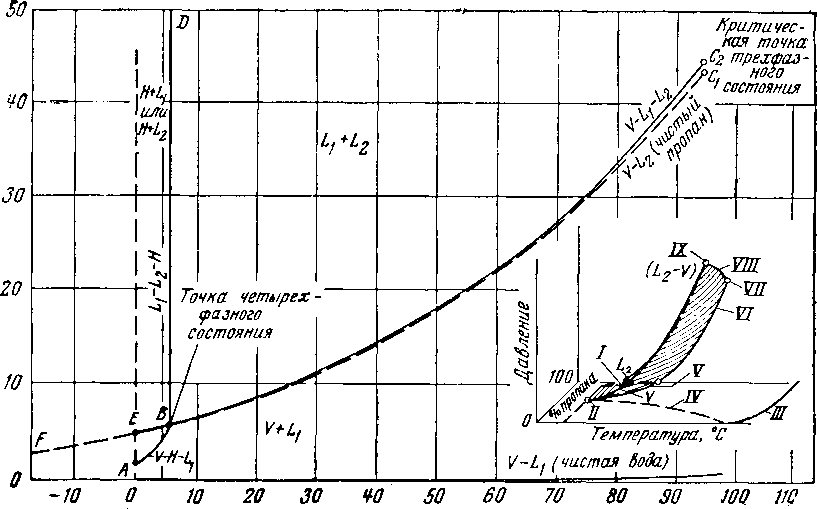
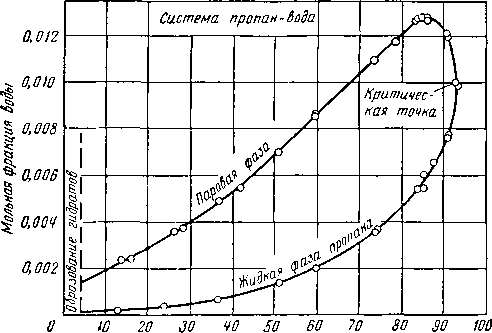
На рис. V. 1 показаны фазовые соотношения системы пропан—вода при температуре выше 0° С. При положительной температуре пропан как чистое вещество будет в виде пара при низком давлении и в виде жидкости при высоком давлении или же как равновесная смесь пара и жидкости на протяжении кривой упругости паров ВСь
Для системы вода—углеводород применяются следующие обозначения: G — газ; L\—жидкая вода;
Z.2 — жидкий углеводород; Н — гидрат; / — лед; М — твердый метан; Р — твердый пропаи; X — концентрация компонента; V—паровая фаза.
По правилу фаз согласно уравнению (III. 1) определяется степень свободы (см. таблицу).
Таким образом, фазовые соотношения пропана и воды с фазами пар V, жидкость — вода L\, жидкость — пропан Z.2 представляется кривой ЕВС2, иногда называемой трехфазной кривой упругости пара. Эта кривая представляет проекцию на плоскость р—Т при дан
| Число компонен тов | Число фаз | Изображение на диаграмме р-Т |
|
2 | 2 |
Плоскость |
| 2 |
3 | Линия |
| 2 | 4 |
Точка |
| 3 |
3 | Плоскость |
| 3 | 4 |
Линия |
ном соотношении компонентов на р—Т—х диаграмме, как показано на пространственной диаграмме (рис. V. I). Кривая упругости паров FCi заканчивается в критической точке Ci для чистого пропана и трехфазная кривая упругости паров ?ВС2 кончается в критической точке между газом и жидким пропаном С2.
Пары пропана и жидкая вода образуют гидраты г/ри 0°С п абсолютном давлении, равном 1,65 (точка А). При увеличонии давления температура образования гидратов также повышается, пока кривая не пересечет кривую V—L\—Z.2 в точке В.
Температура, °C
1
i
4
Рис. V. 1. Фазозое состояние пропано-водвой системы при температуре выше 0° С.
/ — фаза пропан — жидкость, насыщенная парами: // —точка четырехфазного состояния; /// — давление паров чистой воды: IV — насыщенный пар с фазой вода—жидкости; V — насыщенный пао <• фазой пропан — жидкости; VI — давление паров чистого пропана: VII — критическая точка чистого пропана: VIII ~ кривая местонахождения критических точек; IX — критическая точка трехфазного состояния.
В этой критической точке В система неизменна, поскольку представлены четыре фазы. Жидкий пропан и жидкая вода образуют гидраты при давлении выше трехфазной кривой упругости паров и при температуре ниже критической точки. В любой системе гидраг, вода и жидкий пропан находятся в равновесии на протяжении почти вертикальной линии A + D + D. В области графика при температурах ниже кривой DBE присутствуют либо гидраты и жидкая вода L\, либо гидраты и жидкий пропан Z.2 в зависимости от того, какой компонент имеется в избытке.
Фазовые соотношения для метана и воды в области температуры свыше 0° С могут быть представлены в виде кривой р—Т, представляющей условия, при которых гидраты, вода и газ находятся в1 равновесии (рис. V. 2).
Изучение Виллардом (Villard) в 1888 г. [V. 85] системы метан—вода показало, что метан образует гидраты при абсолютном давлении до 280 ат, Виллард ожидал критическую температуру для образования гидратов метана, равную 21,5° С. Кобаяши и Катц (Kobayashi and Katz) [V. 42] показали, что метан не имеет критической температуры гидратообразования до абсолютного давления, равного 830 ат.
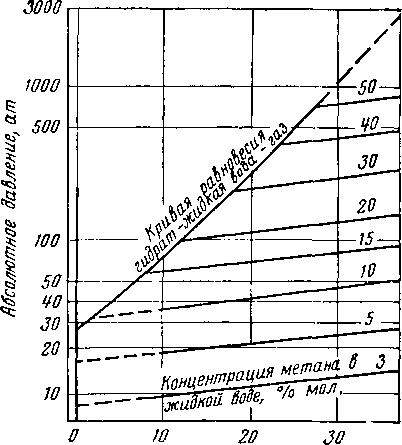
Кривые появления пузырьков газа из воды, содержащей растворенный метан, характеризуют концентрацию газа в воде, образующей гидраты.
Фазовые соотношения для системы метан—вода показаны на рис. V. 3 и V. 4, а фазовые соотношения для системы пропан—вода приведены на рис. V. 5 и V. 6. Рис. V. 3 и V. 5 представляют собой проекцию давления— температуры при 'равновесных условиях, которые возникают в системах.
Температура, °С
Рис. V, 2. Фазовое состояние метано-водной системы при температуре выше 0° С.
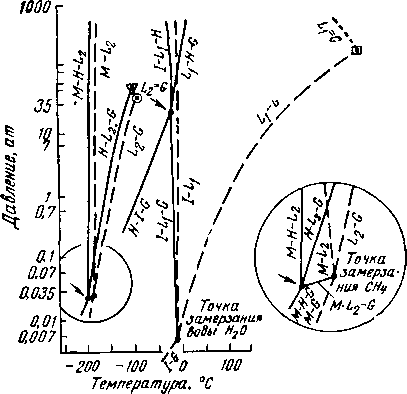
Рис, V. 3. Фазовая диаграмма метано-водной системы для условий гетерогенного равновесия [V. 42].
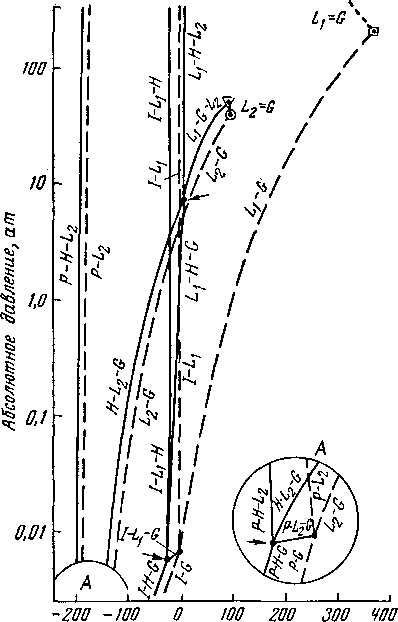
Я — гидрат; Li — вода; L2 — жидкий углеводород: G — газ; I — лед, I — два компонента: 2 — один компонент;
3 — критическая кривая; 4 — критическая точка метана; 5 — критическая точка воды; 6 — точка равновесия четы* рех фаз; 7 — трехфазная критическая точка.
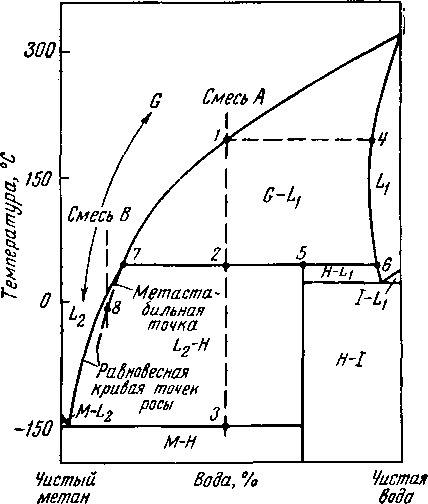
Рис. V. 4. Фазовая диаграмма для системы .метам —вода при давлениях выше критических для метана [V. 42].
®Ч 7
Рис. V. 5. Фазовое состояние пропано-водной системы при гетерогенном равновесии.
/—.два компонента; 2— один компонент; 3—критическая кривая; 4 — критическая точка пропана; 5 — крити-ческая точка воды; 6 — трехфазная критическая точка; / — точка равновесия четырех фаз.
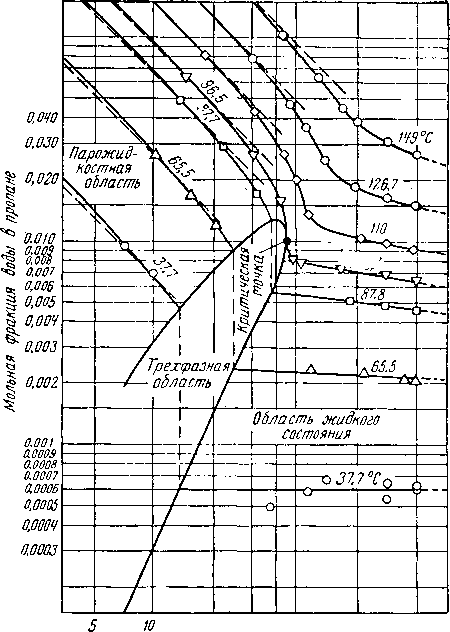
Поскольку общая растворимость углеводородов и веды обычно незначительна, не было сделано попытки представить рис. V. 4 и V. 6 при соизмеримом масштабе. Рис. V. 4 является схематической диаграммой зависимости температура — состав системы метан—вода, взятой при давлении, несколько превышающем критическое давление чистого метана, которое встречается в газопроводах. Подобная диаграмма (рис, V. 6) была построена для системы вода—пропан, для давления несколько ниже критического давления чистого пропана. Это давление было выбрано для иллюстрации условий, при которых сосуществуют две жидкие и одна газовая фазы.
При однородном состоянии фазовый состав и состав смеси идентичны и имеют одно и то же значение. При двухфазном состоянии до стабилизации давления и температуры задается состав фаз. Все негоризонтальные сплошные линии на рис. V. 4 и V. 6 отражают эти составы. Трехфазное состояние системы определяется пограничными линиями, так как в этом случае правило фаз дает одну степень свободы, что приводит к един-
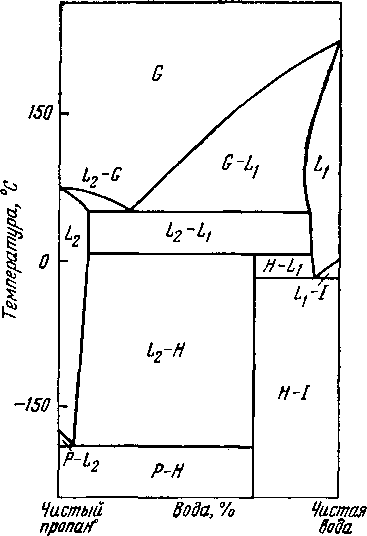
Рис. V. 6. Фазовая диаграмма пропано-вод-ной системы при давлениях ниже критического давления пропана [V. 39]
ственио возможной функциональной связи между давлением и температурой. Для указанных на рис. V. 4 и V. 6 точек, в которых одновременно присутствуют четыре фазы, значения давления, температуры и состава зависят от конкретных условий.
По рис. V. 4 для системы метан—вода можно определять фазовые превращения, происходящие во время охлаждения смеси А при постоянном давлении. Смесь находится в однофазном газовом состоянии до достижения точки 1. Фазовая граница, на которой находится точка 1, является точкой росы паров воды. При этой температуре однофазное состояние в виде жидкости достигается в точке 4. Дальнейшее охлаждение газожидкостной смеси до точки 2 вызывает образование дополнительной фазы — гидрата СН4 • 53/4Н20 [V. 14].
Дальнейший отвод тепла при постоянной температуре определяемой точки 2 приводит к исчезновению жидкой воды в точке 6, которая переходит в шдраты в точке 5, над которыми в равновесном состоянии находятся пары (точка 7). При низкой температуре равновесие М—L2—Н может наступить в точке 3.
Метано-водная смесь другого состава вызовет фазовый переход при других условиях. Хотя такая фазовая диаграмма не может полностью представлять систему природный газ — вода, основные закономерности поведения такой системы сохраняются. Три фазы существуют в определенном диапазоне температур, но для данного газа при данном давлении равновесная температура может быть определена для начала двухфазных условий пар—жидкость. Подобным же образом трехфазные граничные условия для возникновения равновесия пар—жидкость — твердое вещество могут быть определены для данного газа [V. 21, V. 90]
§ 2. РАСТВОРИМОСТЬ ВОДЫ В ПРИРОДНЫХ ГАЗАХ И ПРИРОДНЫХ ГАЗОВ В ВОДЕ
Здесь рассмотрены количественные данные по взаимной растворимости воды и углеводородов в растворах, вода в газе, вода в жидких углеводородах и углеводороды в воде.
Диапазон экспериментальных данных систем вода— углеводороды приведен в табл. V. 1. При определении фазового состояния необходимым условием является гермодинамическая непрерывность поведения в различных фазах, хотя все три растворителя рассматриваются отдельно. Определение содержания воды в газах является довольно сложным процессом, и поэтому вначале будут рассмотрены методы определения влаго-содержания.
1. МЕТОДЫ ОПРЕДЕЛЕНИЯ ВЛАГОСОДЕРЖАНИЯ ПРИРОДНЫХ ГАЗОВ
В настоящее время разработано большое количество методов определения влагосодержания природных газов. Каждый из методов применим в определенных условиях. Единого метода определения влагосодержания для любых условий пока не существует. В табл. V. 2 приведены некоторые методы, применяемые на практике. Из методов, перечисленных в табл. V. 2, будут рассмотрены следующие: 1) метод для определения точки росы паров воды при помощи прибора; 2) метод адсорбции твердыми поглотителями; 3) абсорбция жидкостью с последующим титрованием реагентом Карла Фишера (Karl Fischer),
Прибор для определения точки росы, созданный Горным бюро, широко применяется со времени его создания в 1938 г. [V. 22]. Прибор позволяет визуально определять температуру, при которой вода конденсируется из газа на посеребренное зеркало (рис. V. 7), что важно, поскольку при этом отражается фактическая равновесная температура насыщения газа для температур выше температуры гидратообразования. При температурах, не соответствующих равновесным условиям гидратообразования, прибор отражает условия мета-сгабильного равновесия между газом и жидкой водой.
На рис. V. 7 показан поперечный разрез прибора (без подводящих линий и источников охлаждения). Газ, входящий в аппарат через клапан А, отклоняется соплом В таким образом, что поток газа ударяется об охлажденное зеркало С. Зеркало охлаждается через медную охлаждающую штангу F путем испарения хладагента (пропана, углекислого газа и др.) в холодильнике G. Манометр и термометр используются для регистрации давления и температуры начала конденсации и образования тумана на посеребренном зеркале.
При отсутствии взаимодействующих веществ точность замеров температуры составляет от ±0,1 ниже 0°С и ±0,2 от 0 до —17° С (IV. 2). Прибор рассчитан на давление до 175 ат и температуру до —50° С при применении в качестве охладителя смеси сухого льда и ацетона [V. 78].
Дитон и Фрост (Deaton and Frost) с помощью этого прибора определили точку росы для нескольких природных газов при давлениях До 42 ат и температурах
Система
Водород — вода Метан — вода
Исследуемые фазы
Этан — вода
Этилен — вода Пропан — вода
к-Бутан — вода
И зо бутан Бутан — вода
к-Бутан — метан — вода Гек сан — вода
Жидкая вода.....
То же.........
Жидкая вода......
То же.........
» .........
Жидкий углеводород . . Зона гидратообразования То же.........
Жидкая вода......
Жидкий углеводород . . Зона гидратообразования
То же.........
» .........
Жидкая вода .....
Трехфазная область
Жидкая вода.....
Жидкий углеводород . . Трехфазная область . . Зона гидратообразования Трехфазная область . .
Жидкая вода.....
То же.......• .
Жидкий углеводород . .
Жидкий углеводород . . Трехфазная область . .
Жидкая вода.....
Жидкий углеводород . Трехфазная область . .
Двухфазная область . . Трехфазная область . .
Трехфазная область . .
| Абсолютное давление, ат |
Температура, °С |
Литература |
|
19—1000 | 0—100 |
V. 88 |
| 52—155 |
25 | III. 20 |
| 14—703 | 25—171,1 | V. 18 |
|
41,5—477 | 26,7—148,9 |
V. 53 |
|
41,5—120 | 25 |
III. 20 |
| 37—68Э | 25 | V. 16 |
| 14—703 |
37,8—237,8 | V. 56 |
| 17,5—490 |
—12-н+7,2 | V. 28 |
| 17—110 |
—14ч-+13,3 | V. 69 |
| 31—310 |
—1,1ч—(-21,1 | V. 85 |
| 7—703 |
37,8—171,1 | V. 17 |
| 14—703 | 37,8—237,8 | V. 62 |
|
2,8—10,5 | —12-г-+7,2 |
V. 28 |
|
2,8—70,3 | —12-т-+15,5 |
V. 69 |
|
6,3—44,0 | —1,1^—(-12,8 |
V. 85 |
|
7,7—525 | 35—100 |
V. 6 |
| 32—105 |
15,5—25,5 | V. 23, V. 24 |
| 7—198 |
37,8—148,9 | V. 40 |
| 7—198 | 37,8—148,9 | V. 40 |
|
5,6—45 | 4,4—96,1 |
V. 40 |
| 8,2—62,5 | 5-6,1 | V. 90 |
| 7—28 |
15,5—86,1 | V. 60 |
| 70—703 | 37,8—104,4 | V. 8 |
|
0,7—703 | 37,8—237,8 |
V. 64 |
| 70—703 | 37,8—104,4 | V. 8 |
| 0,7—703 |
37,8—237,8 | V. 64 |
| 3,5—43,8 |
37,8—148,9 | V. 63 |
| 4,4—703 |
37,8—154,4 | V. 46 |
| 4,4—703 |
37,8—154,4 | V. 46 |
| 3,5—70 | 37,8—137,8 | V. 9 |
|
14—210 | 37,8—137,8 |
V. 51 |
| 14—210 | 37,8—137,8 | V. 51 |
| _ | — |
V. 75 |
Таблица 1Л 2
Методы определения влагосодержания природных газов
| Метод |
Область применения |
Замечания | Литература |
|
| Визуальное определение точки, росы | В |
лабораторных и полевых условиях | Производится под давлением при температурах до минус 45,6° С |
V. 21, V. 22 V. 78 |
|
Адсорбционный | В | лабораторных условиях |
Может быть применен при наличии жидких углеводородов | V. 51, V. 80 |
| Абсорбционный метод реагентом Карла Фишера с последующим титрованием |
То же | Может быть использован в полевых условиях |
V. 7 | |
|
Вымораживание с последующим взвешиванием | » | Используется при низких точках кипения газов | V. 56 |
|
| Спектроскопический |
» | Аппарат портативный, дает комплексные показания | V. 83 | |
| Спектроскопический |
» |
Использовался для пропан — водной системы (5—29) | V. 29, V. 83 | |
|
Элсктрогидрометрический |
В | полевых условиях | Применяется при измерениях в стратосфере | V. 26, V. 86 |
Рис. V. 7. Прибор для определения точки росы [V. 22; V. 21].
А — входной вентиль; В — сопло; С — зеркало; D — выходной вентиль; Е — линза? ^ — втулка; <5— холо
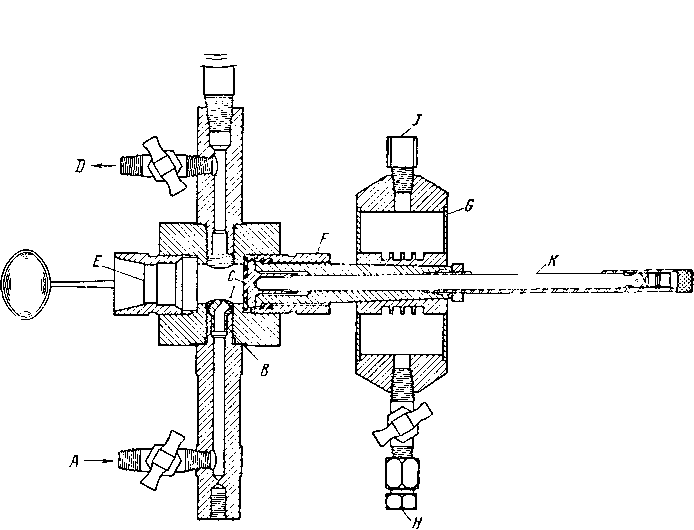
дильник; Н — вход хладагента; / — выход хлада
гента: К — термометр.
до —23° С [V. 21]. Они получили фотографии зеркала при конденсации паров воды и кристаллов льда и описали условия их образования.
Кривые точки росы приведены на графике для различных температур (применен масштаб 1/Т) при постоянном давлении. Отсутствие разрыва этих кривых около 0° С указывает, что конденсация при этой температуре появляется при метастабильном равновесии. Фактически точка росы, наблюдаемая в приборе, соответствует упругости паров метастабильной или переохлажденной воды. При подсчете количества воды в газе при температурах ниже 0°С и умеренном давлении рекомендуется использовать упругость паров над переохлажденной водой [IV. 2].
На рис. V. 4 схематически показана фазовая диаграмма для определения точки росы паров воды. Г аз обычно существует в однофазной области G. Постепенное охлаждение смеси А приводит к образованию дополнительной жидкой фазы в точке /. При визуальном определении температуры конденсации с помощью таких приборов, как прибор Горного бюро [V. 22], устанавливают лишь начало конденсации паров воды. Дальнейшее охлаждение вызывает дополнительное выделение воды, но для определения количества воды в газе нужна только начальная точка росы. Смесь В, содержащая меньшее количество воды, имеет пониженную точку росы, соответствующую метастабильному состоянию (точка 8).
Это, очевидно, есть точка росы, определенная при температуре ниже температуры образования гидратов [V. 41].
Ризенфельд и Фразия (Riesenfeld and Frazier) [V. 68] во время определения точки росы природных газов, осушенных диэтиленгликолем, убедились в непригодности данного метода в этих условиях. Они предложили метод определения абсолютного содержания воды в газах при наличии гликоля.
Кампбелл и Лауренц (Campbell and Laurence) дали расчет материального баланса входного и выходного потоков некоторых установок осушки газа триэтилен-гликолем [V. 11]. Средняя ошибка при определении влагосодержания данным методом составила 6,6%. Максимальное отклонение для нескольких измерений составило 18,9%. Газ пропускался предварительно через сепаратор, в котором отделялась капельная влага.
Охлаждение природных газов часто приводит к конденсации углеводородов, что следует отличать от точки росы паров воды.
В большинстве случаев при экспериментальном определении влагосодержания чистых газов и их смесей использовались твердые сорбенты [V. 40, V. 45, V.51, V. 64]. С помощью твердых химических сорбентов можно наиболее точно определять влагосодержание газа при взвешивании сухого и насыщенного сорбентов. При этом нельзя допускать перенасыщения сорбента, так как могут исказиться результаты.
В качестве твердых сорбентов используют силикаты, которые дают хорошие результаты при низких давлениях. При высоких давлениях и наличии тяжелых углеводородов данный метод дает значительные ошибки.
Точное определение длагооодержания производится С помощью перхлората магния или реагента Карла
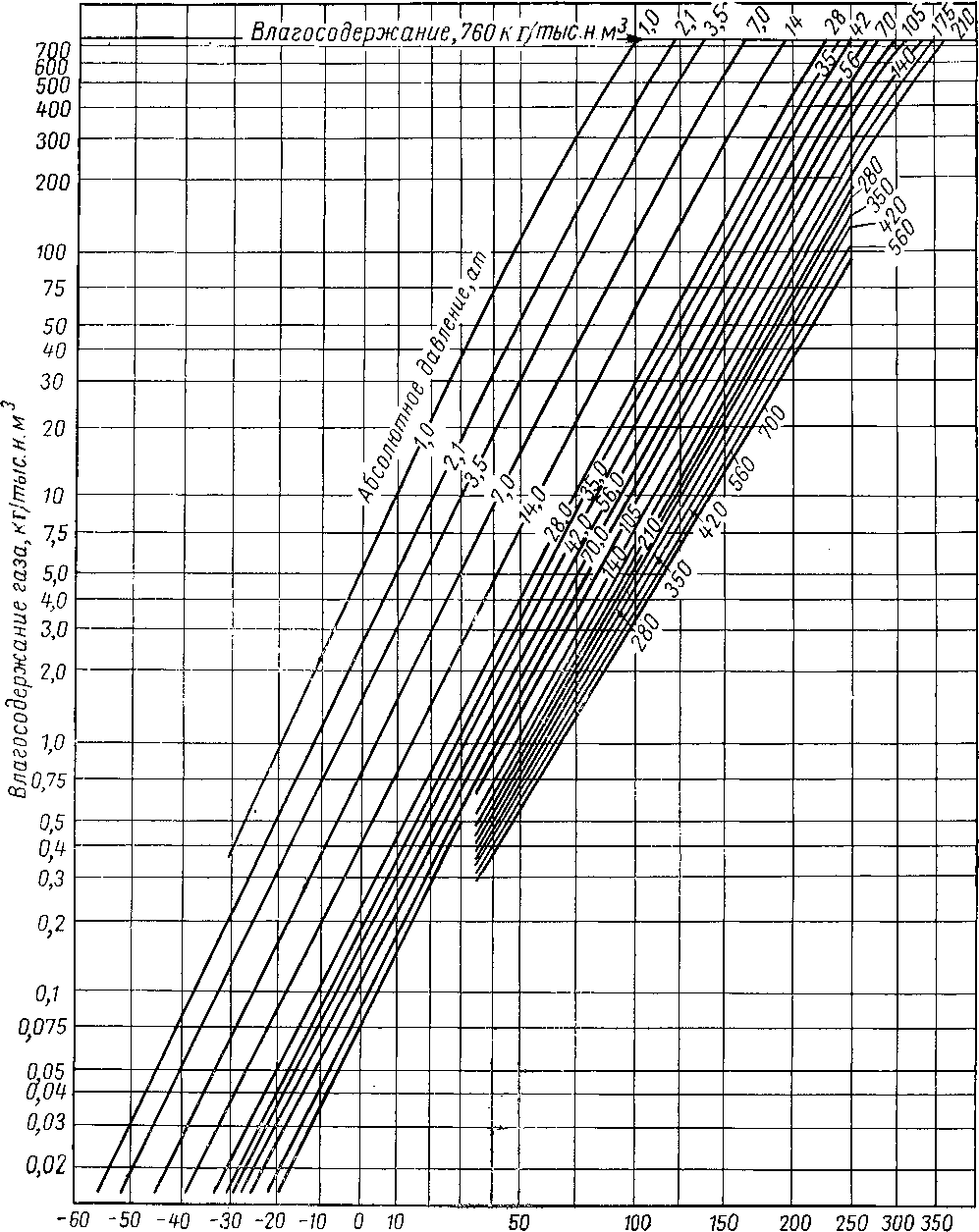
Рис. V. 8. Влагосодержание природных газов в равновесии с жидкой водой.
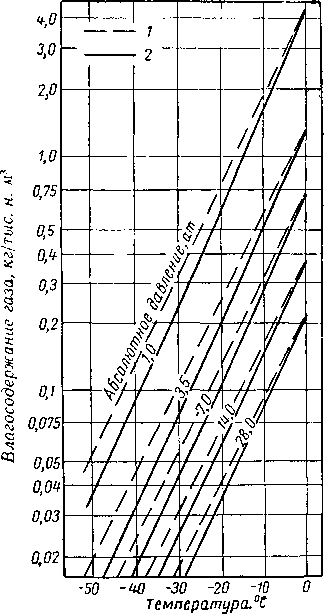
Рис. V.9. График корректировки влагосодержания газа в равновесии со льдом.
/ —> линии равновесного влагосодержания газа в равновесии с метастабильной водой (из рис. V. 8); 2 —линии равновесного влагосодержания газа в равновесии со льдом.
| /8 |
У | |
| / 2 | ||
| // / /Аб / Зс /' сеп | -олюти гдление 1рации | ое 84 |
15
О:
15
13
cl
0
| ' | /ш°с | ||
| / | /о / / 4 / се |
бсолт давлеш параци | •ное te и 63 |
| V |
¦15
15
-15
Точка росы парод воды,°С
Рис. V. 10. Точки росы паров воды в равновесии с гидратами и жидкой
водой [V. 66].
I —* экспериментальные данные; 2 —линии
одинаковых температур*
Фишера (Karl Fischer), при использовании которого реакция протекает следующим образом:
2НаО + S02 (C5H5N2)2 + J2 + 2C5H5N = =(C5H5N)2 ¦ H2S04 + 2 (C5H5N ¦ HJ).
Количество влаги в газах, содержащих метанол или диэтилеигликоль, определяется абсорбцией соответствующими реагентами с последующим титрованием раствора до полного отделения воды, абсорбированной из газового потока.
Митчел и Смит (Mitchell and Smith) [V. 79] посвятили целую книгу методам титрометрического определения влагосодержания газов с помощью реагента Карла Фишера.
Питерс и Джангникел (Peters and Jungknikel) [V. 59] нашли, что стабильность реагента Карла Фишера может быть улучшена после замены в реагенте метанола на метилцеллосил.
Брикелл (Brickell) [V. 7] применил метод Карла Фишера для определения воды в углеводородных газах, который дает хорошие результаты как при низких, так и при высоких давлениях. Допустимая точность метода Брикелла считается равной 0,01 кГ/тыс-н'м3 газа. Метод может быть, несомненно, усовершенствован для получения еще большей точности.
2. ДИАГРАММА ВЛАГОСОДЕРЖАНИЯ ПРИРОДНЫХ ГАЗОВ
В настоящее время имеется несколько номограмм, предложенных различмыми авторами, для определения влагосодержания природных газов [V. 21, V. 78, V. 52, V. 56].
На рис. V. 8 приведена номограмма влагосодержа-кия природного газа, не содержащего азот, в условиях насыщения. Эта номограмма построена по результатам ряда экспериментальных работ [V. 21, V. 22, V. 56 V. 78, V. 25].
В области, где отсутствует гидратообразование, эта номограмма находится в хорошем соответствии с номограммами, полученными Маккетта и Катцем (Mcketta and Katz) [V. 62], Маккарти, Бойдом и Рейдом (McCarthy, Boyd and Reid) [V. 50].
При температурах ниже равновесных температур гидратообразования влагосодержание определяется из условия метастабильного равновесия паров воды над переохлажденной во-дой, а не над гидратом и льдом.
На рис. V. 8 влагосодержание газа дано в г/м3 при 1 ат и 15,5° С в зависимости от температуры при различных изобарах. При содержании воды менее 0,8 кг/тыс. н ¦ м3 ошибка при определении влагосодержания газа не превышает 0,1 %. Несоответствие влагосодержания газа в пределах 24 и 32 кг/тыс. н- м3 в области низких температур по данным Скиннера [V. 78] и соответствующих линий при высоких температурах по данным Додзона и Стэндинга [V. 25] и Олдса, Сейджа и Лацея [V. 56] не могут быть объяснены.
Скиннером были получены данные о влагосодержании природного газа удельного веса 0,7 в пределах до 100 ат путем определения точки росы, а при высоких температурах влагосодержание было определено из условия равновесия фаз.
Й'З
<3
<3 a CO ^
a
?<§<§
!¦§«>
<o C*
Q <o ft) C5
s 8
§ 3
<§ S 5 §
Ч о а ч. Й 10 § 3
g-o
ci
s^
S5
C3
?
0,60
давлении, равном
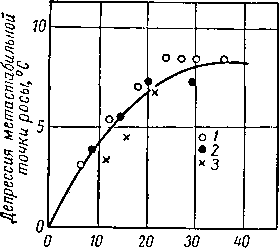
Рис. V. 11. Депрессия метастабиль-ной точки росы гидратами.
t — 63 ат; 2 — 84,5 ат; 3 — 105 ат.
гиипиисьния ii/cM/icfJuiiiyjja auvpw
тообразоВания , минус фактическая,0 С
0,90
0,80
0.70
| <-q. |
|||||||||||
|
\ |
? | ||||||||||
| \ |
\ | • | |||||||||
| \ | |||||||||||
| х 1 о 2 + 3 • 4 °5 |
% | ||||||||||
| N | |||||||||||
0 100,000 200,000 300,000
Ha 1 млн. частиц растворенной соли, частей.
Рис. V. 12. Корректирование влагосодержания природного газа в равновесии с рассолом при атмосферном давлении.
1— NaCl; 2— NaOH; 5— MgCl2; 4 — CaCl,; J _ NaHCOa; 6 — растворение соли при
абсолютном единице.
1,00
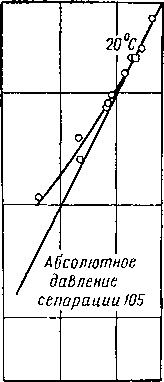
Точка росы газов, находящихся в равновесии с гидратами, например в низкотемпературных сепараторах (рис. V. 10), будет ниже, чем равновесная температура [V. 33, V. 66]. На рис. V. 10, полученном Ракордом и Селли, показано такое отклонение. Это снижение точки росы ниже температуры контакта с гидратами объясняется тем фактом, что измеряемые точки росы находятся из метастабильного равновесия [V. 41]. Из рис. V. 4 можно видеть, что метастабильная точка росы ниже, чем равновесная точка или точка гидратообразования.
Рис. V. 11, построенный по данным рис. V. 10, объясняет понижение точки росы как функцию разности между температурой, при которой газ будет первоначально образовывать гидрат, и фактической температурой образования гидрата. Например, при 63 ат газ согласно рис. V. 11 первоначально образует гидрат при 16° С. При равновесной температуре —9,4° С точка росы наблюдается при —17,8° С. Разница между начальной температурой 16° С и равновесной температурой —9,4° С нанесена на график как функция снижения температуры от —9,4 до —17,8° С.
При метастабильном равновесии- между газом и льдом для корректировки точки росы может быть использован рис. V.9.
Растворенные твердые вещества, находящиеся в воде, понижают парциальное давление паров воды в газовой фазе в равновесии с водным раствором. Додзоя и Стэн-динг [V. 25] определили влияние раствора соли на содержание воды в природных газах.
Понижение упругости паров воды при атмосферном давлении в равновесии с растворами таких солей, как хлористый натрий, хлористый магний, хлористый кальций и бикарбонат натрия, можно определить из рис. V. 12.
3. ВЛИЯНИЕ СОСТАВА ГАЗА НА ВЛАГОСОДЕРЖАНИЕ
Учитывая упругость паров воды при данной температуре, можно вычислить содержание воды в газовой фазе при низких давлениях. Упругость паров воды, отнесенная к общему давлению, определяет молярную фракцию воды для идеальных газов. Для реальных газов молярная фракция воды определяется умножением коэффициента сжимаемости газа на отношение упругости паров воды к общему давлению. В табл. V. 3 сравниваются экспериментальное и расчетное влагосодержа-ние азота, водорода и смесей водорода и азота. Эги данные показывают, что при высоком давлении содержание воды зависит от состава газа.
Поинтгинг [V. 47] установил, что внешнее давление должно увеличивать упругость паров жидкости или тьердых веществ. Поправки Поинтинга к растворимости воды в газах только частично учитывают увели-
Таблица V. 3
Влагосодержание водорода и азота
|
Температура, *С | Давление, am | Коэффици ент сжимаемости | Количество % эксперимент | воды, в газе. мол. j расчет |
| Водород |
||||
| 50 |
103 | 1,06 |
0,139 | 0,129 |
| 203 | 1,117 | 0,0785 | 0,068 |
|
| 412 |
1,250 | 0,0468 |
0,038 | |
| 620 | 1,370 | 0,0363 | 0,0268 | |
|
1050 | 1,615 |
0,0284 | 0,0197 | |
| Азот |
||||
| 50 |
103 | 1,006 |
0,156 | 0,122 |
| 203 | 1,058 | 0,0979 | 0,0644 | |
| 412 |
1,251 | 0,0695 |
0,0381 | |
| 620 | 1,476 | 0,0585 | 0,0299 | |
|
1050 | 1,940 |
0,0405 | 0,0236 | |
| 75% водорода и |
25% азота | |||
|
25 | 103 |
1,058 | 0,0440 |
0,033 |
| 203 | 1,118 | 0,0285 | 0,0174 | |
|
412 | 1,266 |
0,0208 | 0,0099 | |
| 620 | 1,424 | 0,0199 | 0,0074 | |
| 1050 |
1,738 | 0,0197 |
0,0054 | |
| 50 |
103 | 1,053 |
0,151 | 0,128 |
| 203 | 1,112 | 0,094 | 0,067 |
|
| 412 |
1,251 | 0,064 |
0,038 | |
| 620 | 1,398 | 0,059 |
0,0283 | |
|
1050 | 1,698 |
0,055 | 0,0207 |
|
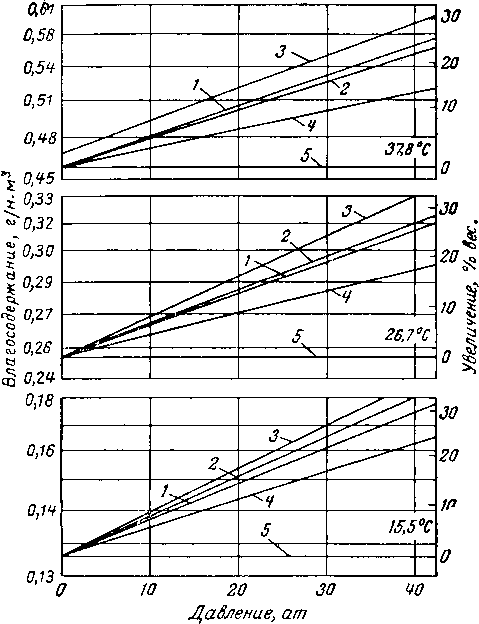
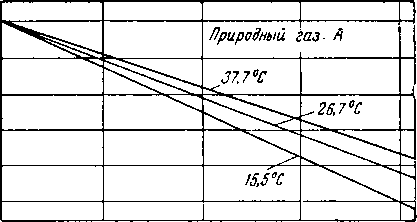
Рис. V. 13. Влагосодержание различных природных газов при указанных давлениях и температурах [V. 21].
1,00
ass
0,96
0,94
0,92
0,90
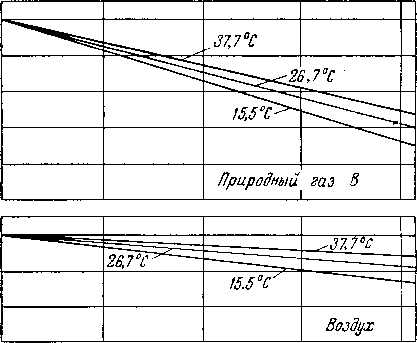
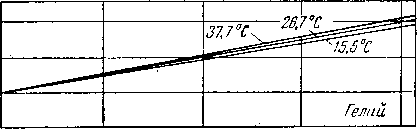
1 — газ состава А (из табл. V. 4); 2 — газ состава В (из табл. V. 4); 3 — газ состава С (из табл. V. 4): 4 — газ состава D ( из табл. V. 4).
N
%
53
0,97
1,02 1,01
Рис. V. 14. Коэффициент сжимаемости природных газов, указанных на рис. V. 13 [V. 21].
чение растворимости воды в углеводородных газах с увеличением давления [V. 4, V. 56]. С точки зрения бинарной системы вода должна обладать очень высокой летучестью при достижении критического давления. При этом концентрация паров воды с повышением давления, как видно из табл. V. 3, возрастает. Наиболее растворимые в воде газы достигают критических условий при более низких давлениях. Данные по растворимости воды в углекислом газе [V. 88] и в сероводороде показывают, что влагосодержание природных газов, содержащих эти компоненты, увеличивается.
Дитон и Фрост (Deaton and Frost) определили (рис. V. 13), что влагосодержание природных газов уменьшается с увеличением содержания азота [V. 21]. На рис. V. 14 показано влияние давления на отклонение от законов идеального газа для природных газов; некоторые газы содержат значительное количество азота (см. табл. V. 4). Азот, содержащийся в природных газах, снижает влагосодержание, так как он способствует уменьшению отклонения от законов идеального газа и менее растворим в воде.
Состав газа (к рис. V. 13)
| Составляющие |
% мол. | |||||
|
Природный газ | ||||||
| А | в | с | D | воздух | гелий | |
|
Воздух .... | _ |
_ | _ |
_ | 100 | _ |
| Двуокись угле |
||||||
| рода .... | 0,3 | 0,8 | 0,2 |
0,6 | — | - |
| Азот..... |
9,4 | 25,0 |
1,1 | 1,00 |
— | 2,0 |
|
Гелий .... | 98,0 | |||||
|
Метан .... | 79,4 |
67,4 | 87,9 |
94,36 | — |
— |
| Этан..... | 5,9 | 3,7 |
4,4 | 2,64 |
— | — |
|
Пропан .... | 3,3 |
1,9 | 4,9 |
0,96 | — |
— |
| Бутан .... | 1,7 | 1,2 |
1,5 | 0,44 |
— | — |
| 100,0 | 100,0 | 100,0 | 100,0 |
100,0 | 100,0 |
|
![]()
0,000? 0,001 0,002 0,004 0,01 0,02 0,04 0,1 0,2 0.4
Мольная фракция боды
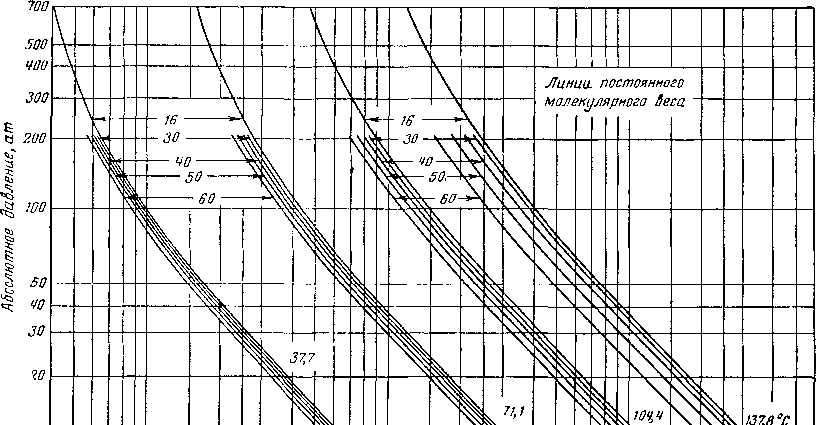
Рис. V. 15, Влияние молекулярного веса на влагосодержание системы метай — бутан — вода [V, 52].
Из мольного состава газов, приведенных на рис, V. 13, видно, что на влагосодержание газа наряду с отклонением от законов идеального газа влияют его растворимость в воде и другие факторы.
Температура, "С
Маккетта и Катц (Mcketta and Katz) [V. 51, V, 52] определили содержание паров воды в равновесном состоянии в метано-бутановодной системе. Влияние добавления бутана к метану показано на рис. V. 15. Влияние молекулярного веса на влагосодержание увеличивается с повышением температуры. Так как в природных газах от метана до газов удельного веса 1,0 молекулярный вес изменяется от 16 до 30, по данным метан-бутановых смесей влиянием снижения влагосодержания природных газов с увеличением их молекулярного веса в технических расчетах можно пренебречь.
4. РАСТВОРИМОСТЬ ВОДЫ В ЖИДКИХ УГЛЕВОДОРОДАХ
Кобаяши и Катцем (Kobayashi and Katz) [V. 39,
V. 40] было исследовано влагосодержание пропана и других газов при различных условиях. На рис, V. 16 показано влагосодержание в газовой и жидкой фазах в системе пропан — вода в трехфазной области при докритическом состоянии. На рис. V. 17 приведено влагосодержание различных природных газов при критических условиях в области трехфазного состояния.
Рис. V. 16. Концентрация воды в насыщенном пропане в трехфазной области [V, 40].
воды изображена как функция температуры, фазового молярного объема и молекулярного веса [V. 40]. Этот график имеет общий характер и может быть применим к углеводородам в жидкой и газообразной фазах. Фазовый молярный объем, выраженный в см3/моль, может быть вычислен по коэффициенту сжимаемости или по графикам плотности.
Константы равновесия для воды могут быть получены для систем углеводорода в области трехфазного состояния L\—Z.2—С.
мольная фракция воды в парах ^ мольная фракция воды в углеводородной жидкости
На рис. V. 18 приведено влагосодержание пропана в области двухфазного состояния. При высоких давлениях равновесная система может рассматриваться как жидкость (пропан)—жидкость (вода), в то время как при низких давлениях и высоких температурах может рассматриваться как равновесие пар (пропан) — жидкость (вода).
На рис. V. 19 приведены кривые растворимости воды в различных углеводородных жидкостях.
На рис. V. 20, а и б показан характер растворимости воды в газе и жидких углеводородах, где концентрация
0.100
6.090
дмо
0.070
0.060
0.050
20 30 40 50 /00 200
ЙЗсолютное да5ление,ат
1,0
8
в
Ч
0,1
%
§
I
О*
I
I
0,01
8
В
Ч
W1
а
в
тог
O.OOOJS
Рис. V. 18. Влагосодержание пропана в области двухфазного состояния [V. 40].
| Soda |
|||||||
|
/ у | |||||||
| 57 |
% | ||||||
|
С,-с» л) |
/Сц | ||||||
| /С,-Су | |||||||
| Г.~ | |||||||
|
/ | 3 | ||||||
|
/ | |||||||
| А к | ¦сн |
||||||
| ( | |||||||
| / ' | 1 \llfJUUJ |
шзительно) | |||||
'0.0002
50 100 150 200 250 300 350
Трехфазная критическая температура, °С
Рис. V. 17. Состав углеводородной фазы в условиях трехфазиопо критического состояния [V. 40]. (Углеводород*вода)
Рис. V. 19. Растворимость в жидких углеводородах.
|
Наименование | Моле куляр ный вес |
Литера тура |
|
Газолин (/) ... | 90 |
V-1 |
| Изобутен (2) . . . | 56 | V-45 |
| Тяжелая нефть («?) | 434 | V-1, V-31 |
| Нефть (4) .... | 147 | V-31 |
| Керосин (5) ... |
173 | V-1, V-31 |
|
Пропан (б) . . . . | 44 |
V-39. V-32 |
| «-Бутан (7) ... | 58 | V-63 |
|
/з | ||||||
| / у У/У | Л/ | |||||
| /гЛ | ||||||
|
'jS/ | ||||||
| // | ||||||
| S' /у | ||||||
| /' | / X/ // У 5 / | V | ||||
| ?' |
--~ss | |||||
| / / |
||||||
| / / | ||||||
|
6 / '7 |
100
Температура,
0,5
0,1
0,05
0,01
0,005
«I
воды
I
§
ч>
§
Ц- 0,001
10.0005
I
t)
a;
0,0001
0,0000!
0,00/
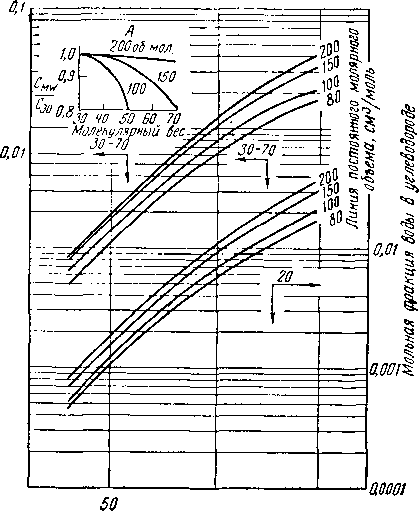
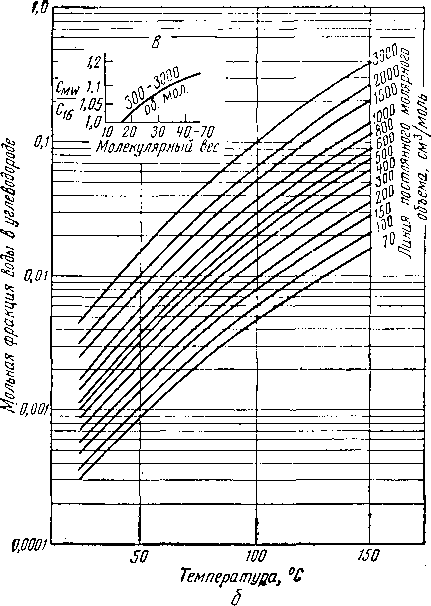
Рис. V. 20. Влагосодержание углеводородов, определенное по фазовой плотности.
Л корректировка иа молекулярный вес при 30—70 м, в. для вязких мол. объемов; В — корректировка на молекулярный вес.
На рис. V. 21 приведены константы равновесия, которые могут быть использованы для подсчета распределения воды между газовой и жидкой фазами в природных газах. График приведен для системы метан — бутан — вода, изученной Маккетта и Катцем (Mcketta and Katz) [V. 51]. Если вода присутствует при температурах выше 93,3°С, константы равновесия углеводородов при расчетах парожидкостных смесей могут значительно отличаться от .констант равновесия безводных смесей [V. 51]. Поетмат и Диен (Poettmann and Dean) fV. 60] и Джантри и Гюнтер (Gentry and Gunther) [V. 32] определили константы равновесия для пропана и пропилена.
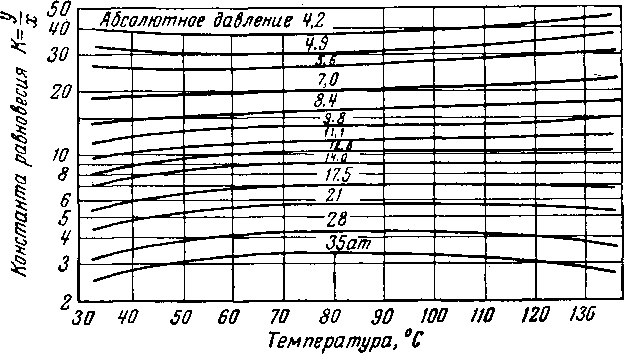
Рис. V. 21. Коиотанты равмовеоия для воды между raaoiBoft и жидкой фазами углеводородов природных газолиновых систем.
Р_
xsp
(V.2)
к-
|
Температура, •С |
Давление, ат |
Мольная фракция воды | |
|
расчетная | эксперименталь ная | ||
| 37,8 |
70,3 | 0,00179 |
0,00173 |
|
421,9 | 0,00159 |
0,00162 | |
|
703,0 | 0,00158 |
0,00158 | |
| 71,1 |
70,3 | 0,00571 |
0,00554 |
|
421,9 | 0,00431 |
0,00493 | |
|
703,0 | 0,00398 |
0,00455 | |
| 104,4 |
70,3 | 0,01272 |
0,01445 |
|
421,9 | 0,01005 |
0,01180 | |
|
703,0 | 0,00915 |
0,01085 | |
| 137,8 |
70,3 | 0,294 |
0,0322 |
|
421,9 | 0,0211 |
0,0260 | |
|
703,0 | 0,0190 |
0,0229 | |
Леланд (Leland) [V. 45] вычислил растворимость воды в чистых углеводородах, использовав концепции внутримолекулярной потенциальной энергии [V. 72] и результаты исследований Х'илдебранда и Скотта (Hildebrand and Scott) [V. 37]. Этот метод основан на молекулярных моделях, для которых сделаны следующие допущения.
1. Взаимная энергия двух молекул зависит от расстояния между ними и не зависит от других соседних молекул и температуры.
2. Распространение молекул свободное.
3. Изменения в объеме при смещении (молекул) при постоянном давлении равно нулю.
Леланд затем предложил эмпирический метод для объединения вириальных коэффициентов чистых газов. В табл. V. 5 приведены результаты сравнения расчетных и экспериментальных величин растворимости насыщенных углеводородов в системе изобутен — вода.
Таблица V. 5 Растворимость воды в изобутене [V. 46]
где Х\ — мольная фракция боды; — парциальная молярная энтальпия раствора; /0— молярная энтальпия чистой жидкости в растворе; R—-газовая постоянная; Т — абсолютная температура; С — постоянная интегрирования.
Предполжение, что разница / ^не зависит от температуры, удовлетворяет условиям растворимости воды в углеводородных жидкостях, за исключением области, близкой к критической температуре углеводородного растворителя [V. 40; V. 45].
Растворимость воды в различных жидких углеводородах в области трехфазного состояния L\—L2—g показана на рис. V. 19 в форме, предполагаемой уравнением (V. 1).
При низких и средних давлениях значения растворимости могут быть использованы для определения равновесного соотношения концентрации воды в газовой фазе концентрации в жидких углеводородах на основе законов Дальтона и Генри (Dalton and Henry) [V. 30].
где К — константа равновесия при общем давлении и температуре Г; у—мольная фракция воды в газовой фазе; х — молярная фракция воды в жидком углеводороде; Р — упругость паров воды при температуре Т\ Xs — молярная фракция воды при насыщении; р—общее давление системы.
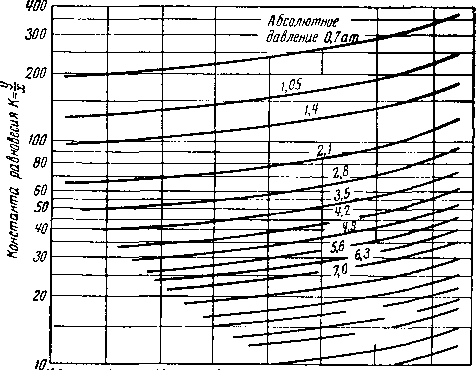
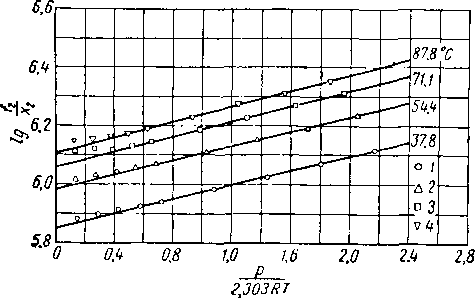
Величины xs при известном молекулярном весе углеводорода можно определить на рис. V. 19. Общее давление системы может быть взято как сумма упругости паров углеводородов и воды без значительной погрешности, пока растворимость в углеводородах не достигает нескольких молярных процентов. Фактическое давление системы будет несколько превышать сумму упругости паров углеводородов и воды. По уравнению (V. 2) были определены константы равновесия К воды с углеводородами молекулярного веса около 170 (рис. V. 22).
У нго %2о
Робин и Водар (Robin and Vodar) [V. 70] применили потенциал Ленарда — Ионеса (Lennard — Jonec) к растворимости метанола, воды и ксенона в сжатых газах. Ргсчет их основан на предположении, что растворимость жидкостей (или твердых веществ) в сжатых газах происходит вследствие двух явлений; 1) увеличения упругости паров жидкости от давления; 2) взаимодействия молекул жидкости и сжатого газа, стремящегося обычно увеличить количество жидкости, содержащейся в газовой фазе.
220
Явление 1 характеризуется эффектом Поинтинга (Poyntings) с учетом поправок для реального газа. Соответствие между экспериментальными и расчетными данными находится в пределах 100—200 ат, но в дальнейшем несоответствие становится значительным. Эти расчеты необходимы для общего объяснения растворимости воды в таких газах, как метай и легкие углеводороды, которые рассматриваются как неполярные.
Леланд (Leland) [V. 45] и Хибберд и Шелло (Hubbard and Schallo) [V. 36] рекомендуют следующее уравнение для построения графика растворимости воды в жидких углеводородах;
1°
г.
— + С,
RT
Температура ‘С
Рис. V. 22. Константы равновесия для воды между газовой и жидкой фазой углеводородов молекулярного веса 170.
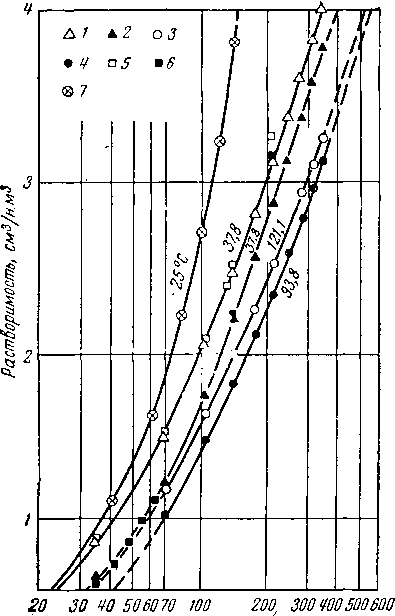
Рис. V. 24. Растворимость природных газов в жидкости [V. 52].
1 — 37.8° С 1 природный газ — вода [V. 25];
2— 121,1 “С/
3 — 37,8е С 1 природный газ — рассол 34 ООО частей
[V. 25];
Мсолютное давление, ат
Температура, °с
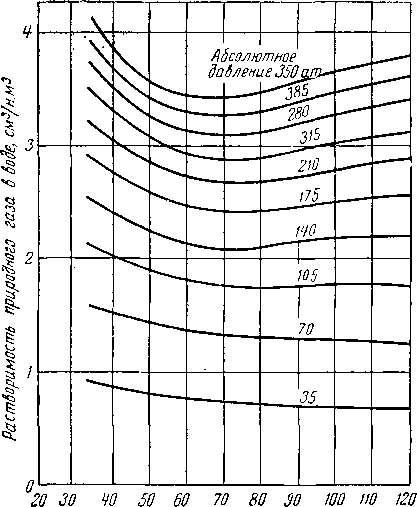
Рис. V. 23. Растворимость природного газа в воде [V. 25].
Растворимость чистых углеводородов и природных газов в воде изучалась многими авторами [V. 9, V. 16, V. 19, V. 25, V. 40, V. 46]. Парафиновые углеводороды очень слабо растворяются в воде даже при высоких давлениях. Вследствие водородной ненасыщенности может увеличиваться растворимость углеводородов в воде [V. 46].
Додсон и Стендинг (Dodson and Standing) [V. 25], определявшие растворимость природного газа в воде, нашли, что растворимость природных газов имеет те же особенности, что и метан, при растворении в воде.
На рис. V. 23 приведены кривые растворимости природного газа в воде при давлениях до 350 ат и температуре до 125° С.
Растворимость природного газа в воде уменьшается в присутствии растворенных твердых частиц в жидкости. На рис. V. 24 приведены кривые растворимости метана в воде, природного газа в воде и природного газа в растворе соли.
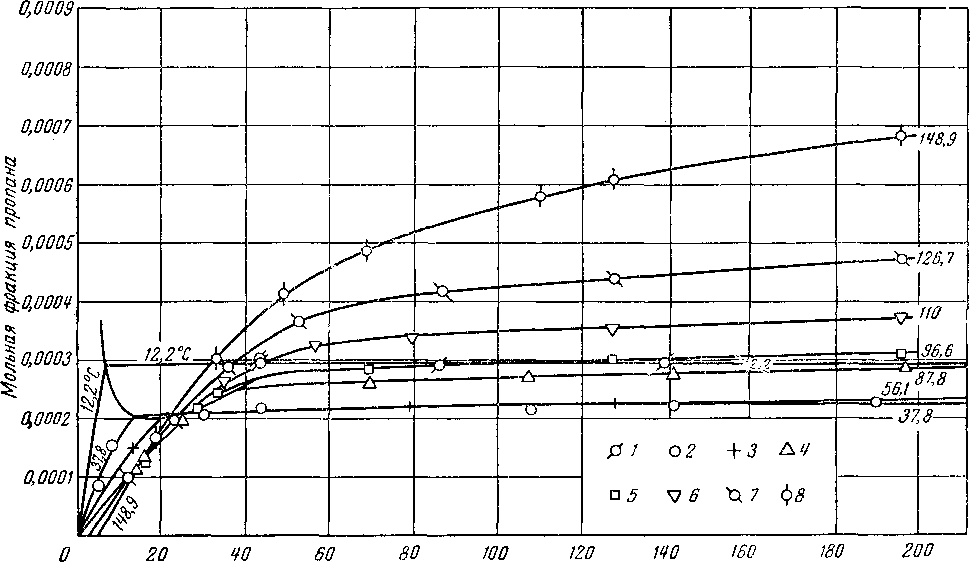
Кулберзда и Маккетта (Culberson and Mcketta) опубликовали данные по растворимости метана и этана
0 10 20 30 "VO
Общая растВоримость 6 рассоле, частей на 1тыс.
в воде при давлении до 700 ат (рис. V. 25 и V. 26) [V. 17, V. 18]. Кобаяши и Катц (Kobayashi and Katz) определили растворимость пропана в воде (рис. V. 27),
Растворимость углеводородов в воде может быть определена на основе закона Генри для разбавленных растворов pi = Hxi (V. 3), где газ ведет себя как идеальный [V. 3], или/1 = #л:1 (V. 4), где газ ведет себя как реальный [V. 4]. Здесь pi — парциальное давление компонента 1; Х\— концентрация компонента / в растворе; Н—константа закона Генри; fi — парциальная летучесть компонента 1.
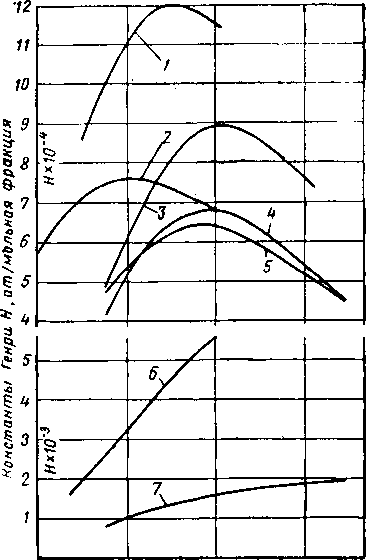
Для данного вещества константа закона Генри есть функция только температуры, поскольку она оценивается при низких давлениях для условий идеального газа и разбавленных растворов. На рис. V. 28 приведены константы закона Генри для отдельных составляющих природных газов. Каждый газ имеет характерный максимум константы при определенной температуре.
Более строгий подход к вопросу растворимости неполярных газов в жидкостях был предложен Кричев-ским и Казарновским [V. 44] и Уибе и Гедди [V. 88].
4 — 93.3° С J
5 — 37.8° С \ метан — бутан — вода [V. 511;
6 — 137,8 "С
7 — 25е С —метан — вода [V. 20].
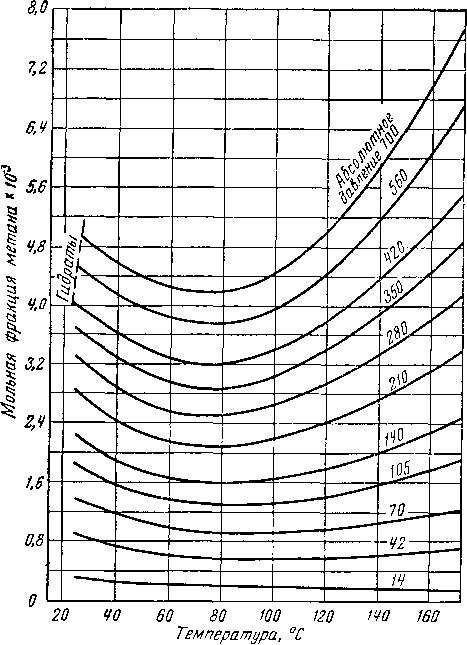
Рис. V. 25. Растворимость метана в воде [V. 18] Рис. V. 26. Растворимость этана в воде [V. 17]
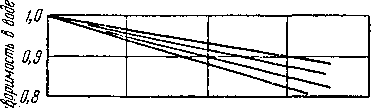
йдсолютног даВле.чие, с.т Рис. V.27. Растворимость пропана в воде [V. 40] (пропан — вода),
/ —12,2°С; 3 —38.0°С: 3 — 56,0° С; ?™88,0°С; 5 — 98,5° С; в— MOJO0 С; 7~127,0°С; Я— 149,0* С.
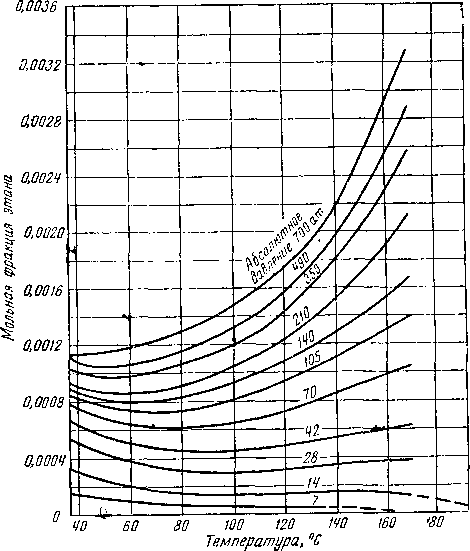
ОО 50 100
Теипвратура’С
150
Рис. V. 28. Константы Генри для определения растворимости углеводородов в воде [V. 40].
In
(V. 5)
/ — азот [V. 44, V.89]; 2 — водород ( V. 44, V. 88];
3—пропан [V. 39J; 4—этан Г V. 17, V. 39]; 5 — метан [V. I7f V. 39]; 6 '— окись углерода[ V. 87, V. 88J; 7 — сероводород [V.77J.
Уравнение, данное Кричевским и Казарновским, было преобразовано Леландом [V. 45] к виду
- In H+pf (р-рв),
где fi — парциальная летучесть растворенного газа; а'2 — молярная фракция растворенного вещества; V2 — парциальный мольный объем газа, растворенного в воде (принято рассматривать как функцию только температуры); рв—давление насыщения чистой воды; Т — абсолютная температура; Н — константа закона Генри при Р = Рв.
Кобаяши и Катц (Kobayashi and Katz) [V. 40] применили это соотношение к фазе жидкой воды в бинарной системе вода—углеводород для определения величин V2 (рис. V. 29) [V. 30]. Леланд, Маккетта и Кобе (Leland, Mcketta and Kobe) [V. 46] применили это уравнение к двум жидким системам: изобутен — вода. При приближении к критической точке углеводорода отклонение от изотермического графика ln(^/^2) в зависимости от р—рв показывает, что величина V2 не может быть принята независимой от давления.
Более общему применению уравнения (V. 5) мешает отсутствие данных о парциальной летучести и парциальном объеме для смесей. Уравнение (V. 5) может быть с успехом использовано в настоящее время путем экстраполяции данных промежуточного давления к более высоким давлениям.
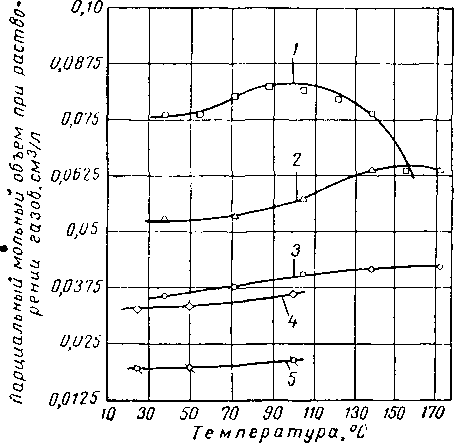
Рис. V. 30. Парциальный мольный объем чистых угле-иодородов Нг и N2, растворенных в воде [V. 40].
/ — пропан; 2— этан; 3 — метан; 4— азот; 5—водород.
Рис. V. 29. График определения растворимости пропана в воде при использовании парциального объема и константы Генри [V. 40].
§ 3. ГИДРАТЫ УГЛЕВОДОРОДНЫХ ГАЗОВ
Гаммершмидт (Hamrnerschmidt) [V. 33] обратил внимание на то, что «замораживание» газопроводов происходит вследствие образования гидратов. Большая предварительная работа была проделана учеными Европы, которые исследовали свойства различных веществ [I. 9]. Фарадей (Faraday) впервые обнаружил газовые гидраты в своих исследованиях гидратов хлора [V. 27]. Обзор исследований образования гидратов в метане, этане и двуокиси углерода приводится в работе Шредера (Schroeder) [V. 76].
Гаммершмидтом были описаны условия образования гидратов природного газа. Поскольку проблема образования гидратов приобрела практическое значение, были проведены большие исследования при изучении гидратов Дитоном и Фростом (Deaton and Frost) [V.21, V. 28], Катцем с сотрудниками [V. 12, V. 90, V. 43, V. 38, V. 42, V. 55, V. 84] и другими [V. 77, V. 49, V. 65, V. 69, V. 2, V. 3, V. 48] для бинарных и многокомпонентных смесей углеводородов и воды.
Недавно были исследованы структуры гидратов теоретически [V. 14, V. 57, V. 81] и при помощи рентгеноструктурного анализа [V. 15, V. 82].
1. СВОЙСТВА ГИДРАТОВ УГЛЕВОДОРОДНЫХ ГАЗОВ
Гидраты углеводородных газов обладают рядом свойств, которые приписываются отдельным химическим компонентам, но, с другой стороны, они ведут себя как растворы газов в твердых кристаллах.
В результате экспериментальных исследований и термодинамических анализов были получены формулы, характеризующие состав гидратов.
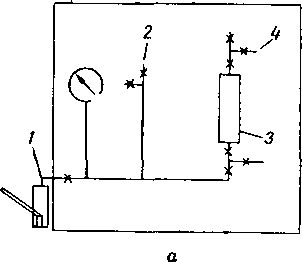
Неустойчивость гидратов при низких давлениях повлияла на неточность экспериментальных исследований, Экспериментальное определение образования гидратов проводится обычно в аппаратуре, имеющей окна для наблюдения. На рис. V. 31 приведена схема камеры со стеклянным окном, использованная для определения гидратообразования для системы метан—пропан—вода [V. 12].
Равновесная точка гидратообразования определяется путем понижения температуры смеси природных газов, насыщенных водой до начала образования гидратов при постоянном давлении. При этом гидраты образуются только в присутствии жидкой воды.
По внешнему виду гидратные кристаллы напоминают лед или мокрый спрессованный снег. Когда давление снижается, чтобы вызвать распад кристаллов, кристаллы не меняют внешнего вида. При уменьшении давления кристаллы издают слабый треск (который слышен, если приложить ухо), что указывает на распад кристаллов. Кристаллы гидратов природного газа подобно льду плавают на поверхности воды и имеют удельный вес от 0,88 до 0,90 Г [см?.
Большие рентгеноструктурные исследования показывают, что имеются два типа решеток: пентагондо-дэкаэдр (кубический) и решетка «бриллиант». Основные данные этих решеток приведены в табл. V. 6. Основные гипотезы, используемые Клауссеном (Claussen) [V. 13], следующие.
Таблица V. 6 Физические показатели решетки гидратов [V. 13]
| Фактор |
Тип решетки «бриллианта» |
Кубиче* ский тип решетки |
| Постоянная решетки А..... | 17 | 12 |
| Число молекул воды, образующих | 136 | 46 |
|
решетку........... | ||
|
Число малых полостей...... |
16 | 2 |
|
Число средних полостей..... |
0 | 6 |
|
Число больших полостей .... |
8 | 0 |
|
Гипотетическое число гидратов: при заполнении всех полос | ||
| тей ............ |
516/з* | 517/4 |
| при заполнении только боль | ||
|
ших полостей....... | 17 | 72/з |
* [V. 13].
Рис. V. 31, Аппаратура (схема) для образования гидратов. а — контрольный пункт; б — аппарат гид* ратообразования, 1 — насос; 2 — патрубок к цилиндру гидратообразования; 3 — бомба-накопитель газа; 4 — патрубок к газовому цилиндру; 5 — бомба-реактор (ци-лиидр гидратообразования).
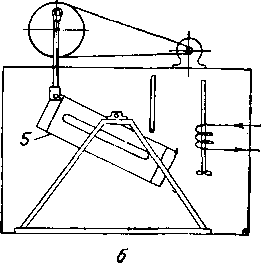
Гидратоб нет
-Л
н- СНЧ; Hz5 X
PH 3
5^ПгО
I1
!
I
гь
'а
1
I
f
СН3С1
Сг Нб CHjSH - В г,
7ф Hz0
8^
-СнгС12;СИС13
СНгС1СНгС1 -
cs2
СН 2 Вг*2 С3И,С1
C2HsCl 7Л
СН3 СИС1г C2HS: UC,HI0
17 Н20
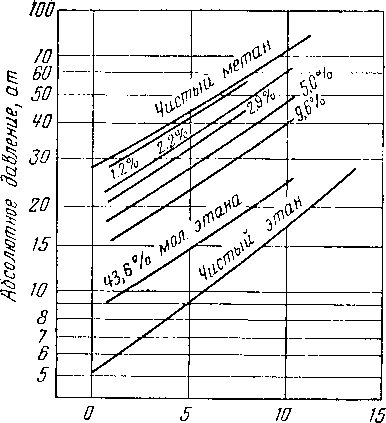
ЗА-
ЧЛ-
Рис. V. 33. Условия образования гидратов метан-этановой смеси [V. 21].
5А-
СИгС1СНгС1
Гидратоб нет
Рис. V. 32. Номограмма для определения размера молекул гидрата [V. 13, V. 14, V. 81].
- Н. н=Щ„
8А-
гидрата А ' 4V4H2O [V. 20]. Пропан дает гидраты с теоретической формулой СзН8' 17Н20.
Наибольшей молекулой из углеводородов, которая образует гидраты, является циклопентан [V. 48]. Изопен-тан и метилциклопентан не образуют гидратов [V. 48]. Незначительные концентрации этана или пропана в метане сильно понижают давление, требуемое для образования гидратов (рис. V. 33 и V. 34) [V. 21]. Во время исследований молекулярной модели углеводородов и кристаллической структуры гидратов определили, что молекулы свободно вращаются в пустотах, образуемых между молекулами воды [V. 20, V. 81].
Число молекул воды, связанное каждой молекулой газа, показано на рис. V. 32. При экспериментальных работах получают иное число молекул, связанных одной молекулой газа, однако точного значения их числа еще не имеется. Бутан имеет критическую температуру гидратообразования +1°С и узкий диапазон температуры гидратообразования выше 0°С [V. 90]. Однако в присутствии других газов бутан дает гидраты и при более высокой температуре. Гидраты являются твердыми растворами. Изучение системы метан—пропан—вода показывает, что нон-вариантная точка (точка наличия четырех фаз) имеет одну степень свободы (рис. V. 35), которая соответствует одной твердой фазе. При изучении составов углеводородных гидратов было получено плавное изменение в составе в зависимости от температуры (рис, V, 36).
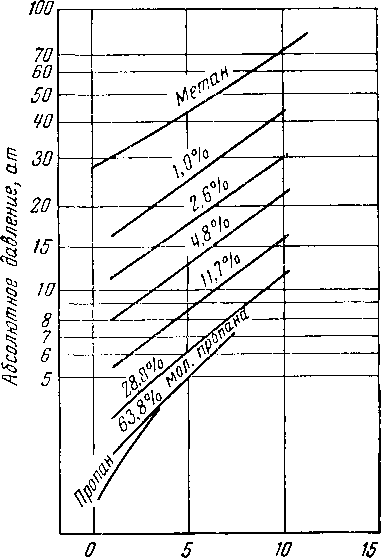
Рис. V. 34. Условия гидратообразования ме-тан-пропаиовой омеси [V. 21].
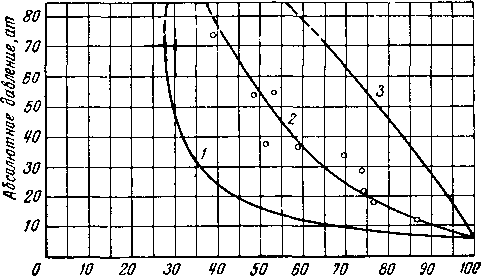
% мол пропана в Soffe
Рис. V. 36, Фазовый состав системы метан—пропан вода [V. 12].
1 —> пары углеводородов; 2 — гидрат; 3 — жидкость.
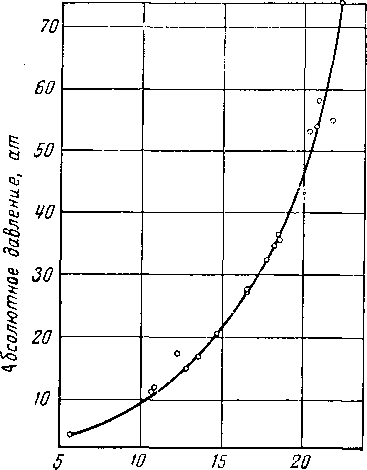
Рис. V. 35. . Кривая точек четырехфазного состояния системы метан—пропан — вода [V. 12].
800
700
600
500
V00
300
Z00
2. УСЛОВИЯ ОБРАЗОВАНИЯ ГИДРАТОВ
Для данного состава газа начальные условия образования гидратов могут быть представлены равновесными кривыми на графике в координатах давление — температура. Условия образования гидратов для бинарных систем парафиновых углеводородов при наличии жидкой воды приведены на рис. V. 37, который построен на основе работ [V. 12, V. 21, V. 42, V. 69, V. 76, V. 85, V. 90, I, 9]. Пентан и гексан гидратов не образуют. Если они и образуют гидраты, то из рис. V. 37 можно сделать вывод, что они образуют гидраты только при температуре ниже 0° С. Другие газы образуют гидраты при насыщении парами воды, как показано на рис. V. 38; равновесная привая гидрат — вода пересекает кривую V—L—Z.2 в точке, в которой находятся в равновесии четыре фазы — гидрат, вода, жидкие углеводороды и газ. Выше этой точки равновесная кривая образования гидратов идет почти вертикально. На рис. V. 33 и V. 34 показано влияние концентрации этана и пропана в газовой фазе на условия гидратообразования для систем метан—этан—вода и метан—пропан—вода. Небольшие изменения г> концентрации этана и пропана в газовой фазе вызывают значительные изменения в равновесной кривой гидратообразования.
§ 100 $ 14
I 60 Ц 50
& зо
I»
I
^ 10
7
В
5
Ч
3
2
40
Некоторыми исследователями [V. 21, V. 90] получены равновесные кривые гидратообразования для некото рых природных газов (рис. V. 39).
На рис. V. 40 приведены равновесные кривые гидратообразования, полученные Катцем [V. 38] для природных газов различного удельного веса (по воздуху). Азот, находящийся в природном газе, значительно влияет на условия образования гидратов [V. 21]. Равновесные графики образования гидратов природных газов содержащих различное количество азота, приведены на рис. V. 41.
25 °С
-5
| У |
^- | ||||||
| / | |||||||
| / | у' |
||||||
| / у | У / |
||||||
| / | |||||||
| "а | й- р | ||||||
| IX |
\____ | 2 | |||||
| __if — 1 |
У | ||||||
| 1 ? |
|||||||
| ь |
.3 | ||||||
|
—^=ч -л 1 | * у | ||||||
| 1 | о / |
||||||
| 'i | |||||||
|
/ | ^5 |
||||||
5 10 15 20
Температура, °С
Рис. V. 37. Условия образования гидратов парафиновых 'углеводородов.
1 — метан; 2 — этан; 3—пропан; 4 — изобутан; 5 — /*-бутан«
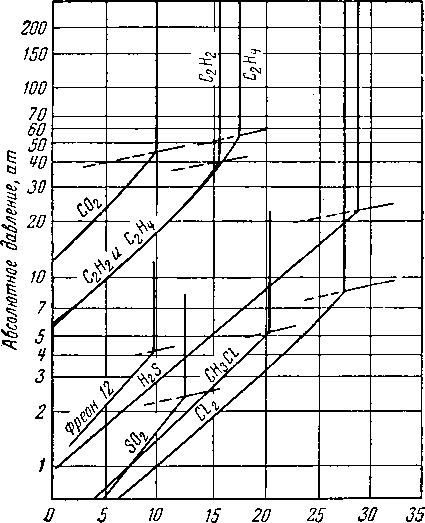
Рис. V. 38. Условия гидратообразования для ие-углев'одородных газов.
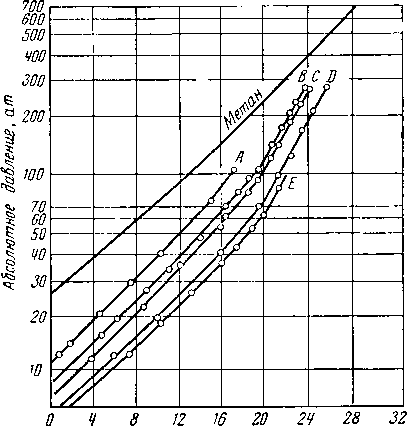
Температура, °С
Рис. V. 39. Условия гидратообразования природных газов [V. 21, V. 90, V. 42].
3. ОПРЕДЕЛЕНИЕ УСЛОВИЙ ОБРАЗОВАНИЯ ГИДРАТОВ ПО КОНСТАНТАМ РАВНОВЕСИЯ
Как указано выше, твердые газовые гидраты ведут себя до некоторой степени как растворы газов в твердых кристаллах. Плотность газов, выделяющихся при
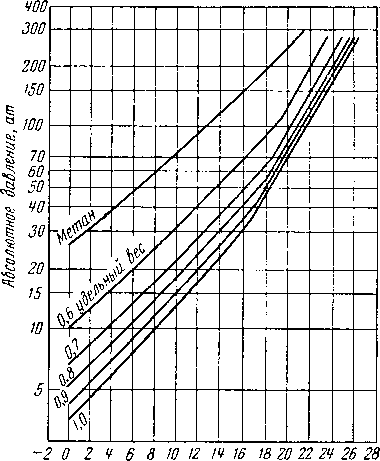
Температура, °С
Рис. V. 40. Условия гидратообразования природных газов в зависимости от удельного веса (по воздуху) [V. 38].
разложении гидратов природных газов [V. 12, V. S0], постепенно увеличивается, и таким образом газы напоминают твердые растворы. По аналогии с равновесием жидкость — пар Вилкокс, Карсон и Катц (Wilcox, Carson and Katz) [V. 90] предположили, что условия образования гидратов могут быть определены на основе эмпирически определяемых констант равновесия пар — твердое вещество
KV-s=f’ (V‘6)
где у — молярная фракция углеводородов в газовой фазе, насыщенной парами воды; х, — молярная фракция углеводорода в гидрате.
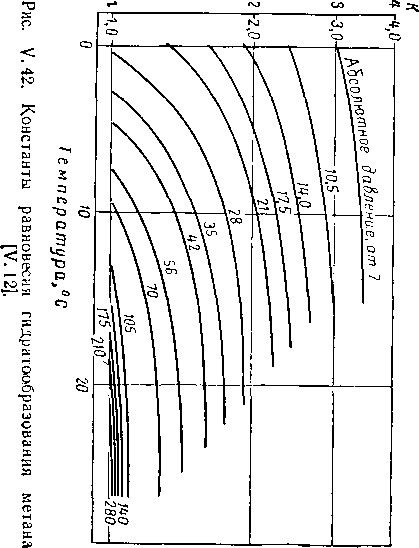
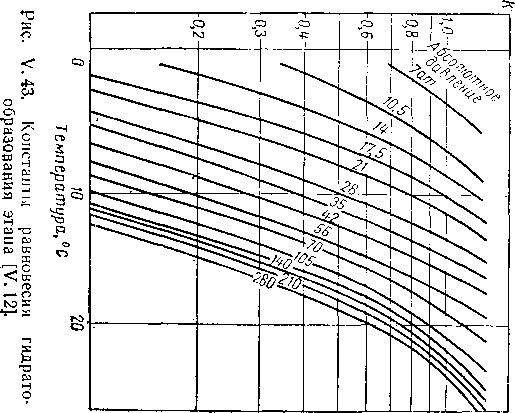
Карсон и Катц (Carson and Katz) дают равновесные константы для метана, этана, пропана и изобутана. В позднейших исследованиях константы равновесия пар — твердое вещество были определены для трехкомпонентной смеси метана, двуокиси углерода и воды [V. 84], а также метана, сероводорода и воды [V. 55]. Эти константы равновесия представлены на рис. V. 42— V. 47. В присутствии легких углеводородов константы равновесия для низкой концентрации к-бутана могут быть взяты как константы этапа.
Для азота и углеводородов тяжелее бутана равновесные константы берутся как бесконечность, так как они затрудняют образование смешанных гидратов. Константы равновесия принимаются как функция только давления и температуры, но фактически они зависят и от состава газа.
Начальные условия образования гидратов определяются отношением
2 тг— = 1,0. (V. 7)
Kv—s
Расчет аналогичен расчетам точки конденсации для газовых смесей. В табл. V, 7 приведены результаты расчетов условий гидратообразования для природного газа при 10° С.
Температура,°С
Рис. V. 41. Условия гидратообраэования природных газов, содержащих азот.
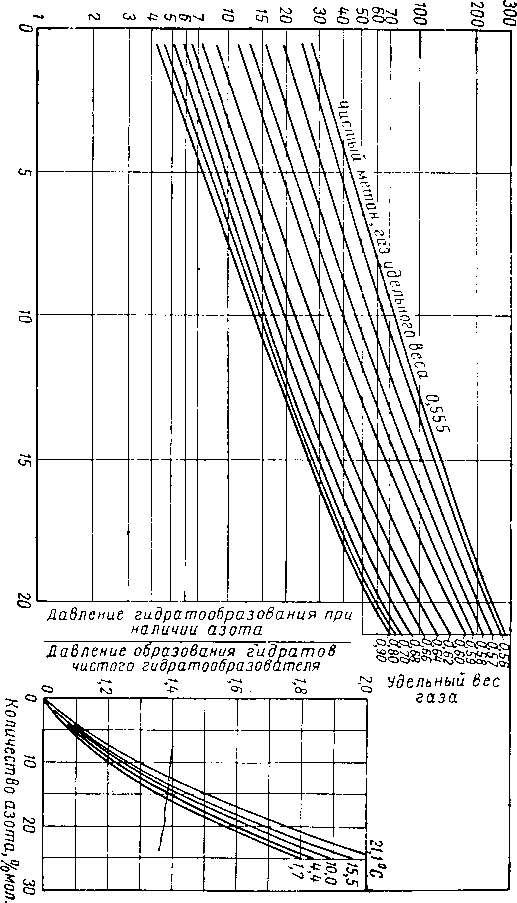
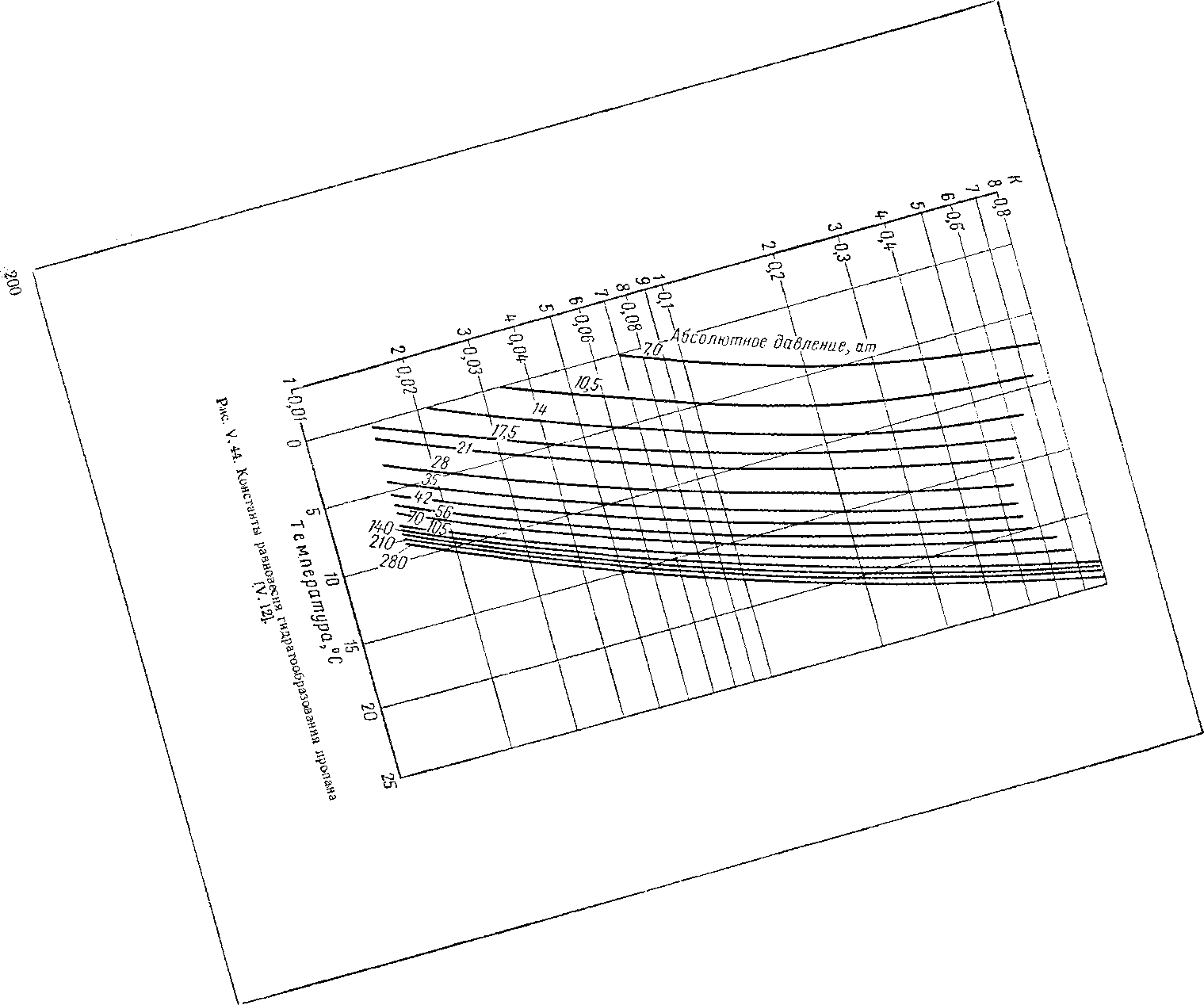
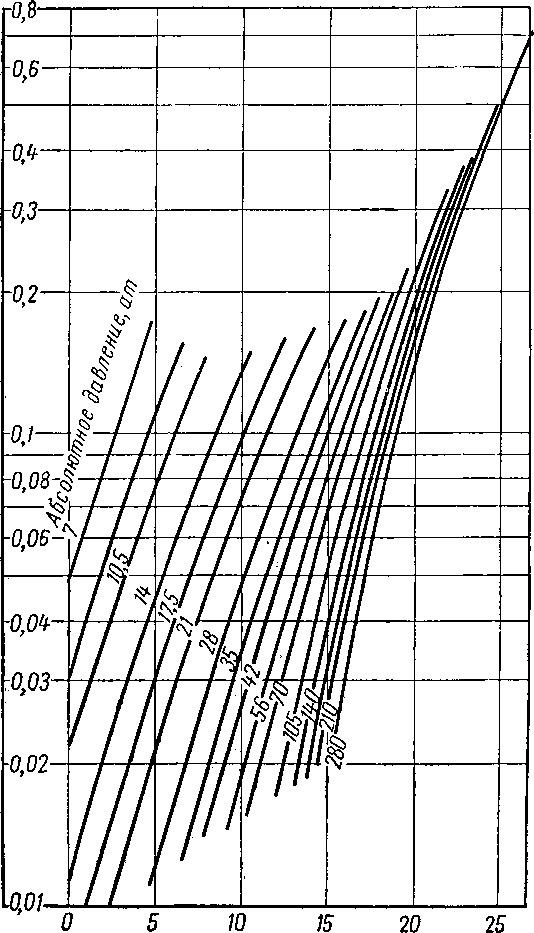
Рис. V. 45. Константы равновесия гидратообразования изобу-тана [V. 12].
U,В
| / / |
/ / //И | ч | |
| / / / / / | ' / //III У / / > / / |
/ | |
| /^/' |
/ ///// | ||
| у | N \ \\ \ N . \ |
/ / / / / / / //// ' //// | |
| Уу/% | |||
| У | |||
К
2.0
10
0,8
0,4
О 5 to 15
Температура, °С
Рис. V.46. Константы равновеаия гидратообразо-¦вашия окиси углерода [V. 84].

0,4
0,3
0,08
0,06
0,04
Температура, °С
Рис. V. 47. Константы равновесия гидратообразования сероводорода [V. 55].
Расчет давления гидратообразования для природного газа при 10° С
|
Компонент | Мольная фракция в газе |
Абсолютное давление, ат | |||
| Р-- | = 21,1 |
р | = 24.6 | ||
|
К | У/К |
К | У/К | ||
| Метан .... | 0,784 | 2,04 | 0,3841 |
1,9 | 0.4126 |
| Этан..... | 0,060 | 0,79 | 0,0759 |
0,63 | 0,0952 |
| Пропан .... |
0,036 | 0,113 |
0,3185 | 0,086 |
0,4186 |
| Изобутан . . . | 0,005 |
0,0725 | 0,0689 |
0,058 | 0,0862 |
| и-Бутан . . . | 0,019 | 0,79 | 0,0240 |
0,63 | 0,0301 |
| Азот..... | 0,094 | — | 0,0000 |
— | 0,0000 |
| Углекислый | |||||
| газ .... | 0,002 |
3,0 | 0,0007 |
2,3 | 0,0008 |
| Итого . . | 1,000 |
0,8721 |
1,0435 | ||
Вычисленное абсолютное давление, равное 23,7, практически совпадает с экспериментально полученным абсолютным давлением, равным 22,9.
В табл. V. 8 сравниваются рассчитанные и экспериментально определенные температуры гидратообразования при различных давлениях. Учитывая трудности, встречаемые при экспериментальных работах с твердой фазой, можно принять, что расчеты подтверждают гипотезу о том, что гидраты природных газов ведут себя как твердые растворы.
Таблица V. 8
Сопоставление расчетных и экспериментальных условий образования гидратов
Состав газа
| Компонент | Газы | ||||||
| D | в | с |
4Н | 5 | 6 к | 7А | |
|
Метан............. | 0,8641 | 0,9320 | 0,8800 | 0,7516 | 0,8250 | 0,674 | 0,9497 |
| Этан.............. |
0,0647 | 0,0425 |
0,0682 | 0,0595 |
0,0599 | 0,037 |
0,0296 |
|
Пропан............. | 0,0357 | 0,0161 | 0,0254 | 0,0333 | 0,0326 | 0,019 | 0,0081 |
| Изобутан............ |
0,0099 | — |
0,0038 | 0,0050 |
0,0030 | 0,006 |
0,0020 |
|
и-Бутан........... | 0,0114 | — | 0,0089 |
0,0005 | 0,0049 |
0,006 | 0,0036 |
| Пентан............. |
0,0078 | — |
0,0101 | 0,0051 |
0,0007 | — |
0,0028 |
| Углекислый газ......... | — |
0,0051 | _ |
0,002 | 0,002 |
0,008 | 0,0042 |
| Азот............ | 0,0064 | 0,0043 | 0,0036 | 0,143 | 0,0719 |
0,250 | |
|
Источник . . . | IV. 90] | IV. 90, | [V. 20] | [V. 21] | [V. 33] | IV. 2Ц | [V. 73| |
Продолжение табл. V. 8 Равновесные условия гидратообразования
| Газ | Абсолютное давление, am | Температура гидрато эксперименталь ная |
эбразовання в, *С расчетная |
| D | 14 |
6,66 | 6,6 |
| 28 | 12,77 | 12,2 | |
|
56 | 17,5 |
16,4 | |
| 105 | 21,1 | 20,3 |
|
| 280 |
25,0 | 24,3 | |
| 17,5 | 5,0 |
4,8 | |
| В | 35 | 10,8 |
10,8 |
|
70 | 15,8 |
15,4 | |
| 175 | 21,1 | 21,2 |
|
| 280 |
23,0 | 23,2 | |
| С | 14 |
4,45 | 5,0 |
| 35 | 11,7 |
12,3 | |
|
70 | 16,9 |
16,9 | |
| 105 | 19,2 | 19,8 |
|
| 210 |
22,5 | 23,0 | |
| 4 Н | 10,5 |
2,8 | 1,9 |
| 17,5 | 7,0 | 7,1 | |
|
28 | 11,1 |
10,7 | |
| 5 |
17,5 | 6,0 |
7,0 |
| 28,0 | 9,8 | 10,2 |
|
| 56,0 |
15,5 | 15,7 | |
| 6к | 14 |
3,2 | 3,7 |
| 21 | 6,5 |
7,0 | |
|
28 | 8.8 |
9,0 | |
| 7 А | 21 | 3,1 |
3,5 |
|
28 | 6,0 |
8,0 | |
| 35 | 8,0 | 9,2 |
|
| 42 |
9,8 | 11,0 | |
| 56 | 12,2 |
12,8 | |
|
70 | 14,1 |
14,3 |
Катц и другие [V. 38] объединили теоретические и экспериментальные исследования по определению условий гидратообразования для природных газов (рис. V. 40) с термодинамическими энтальпийно-энтро-пийными данными [V. 10] для получения рис. V. 48—V. 50. с*ти графики могут быть использованы для определения максимально допустимого расширения (АЯ = 0) природных газов, насыщенных водой без образования гидратов, а также для определения изменения температуры при расширении природного газа.
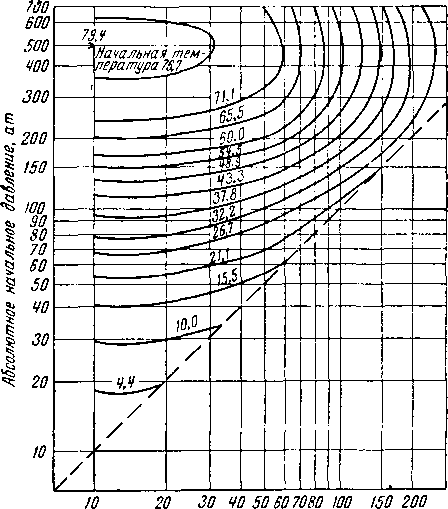
Абсолютное дабление после расширения, am
Рис. V. 48. Допустимое расширение газа удельного веса 0,6 без гидратообразования [V. 38].
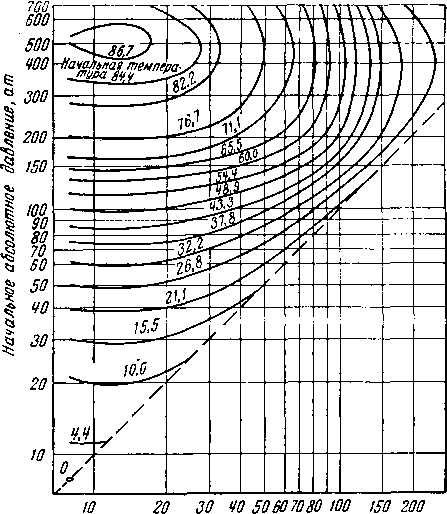
Конечное абсолютное давление, am
Рис. V. 49. Допустимое расширение газа удельного веса 0,7 без гидратообразования TV. 38].
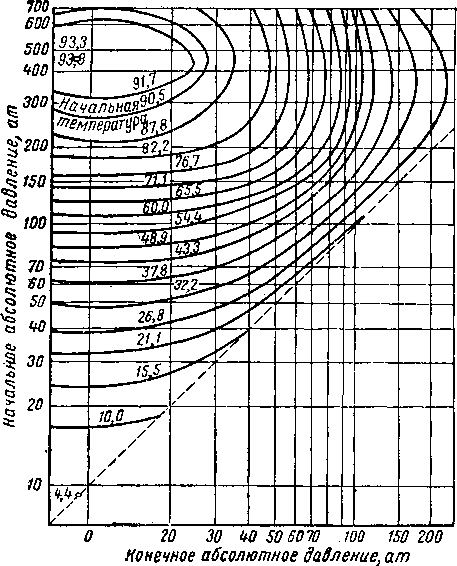
Рис. V. 50. Допустимое расширение газа удельного веса 0,8 без гидратообразования (5—38).
4. ПРЕДОТВРАЩЕНИЕ ГИДРАТООБРАЗОВАНИЯ
Как указано выше, гидраты образуются только, если имеется жидкая вода в газе. Добавление химических веществ к воде может менять ее точку замерзания. В промышленности для снижения температуры образования гидратов обычно применяют метанол.
Было проведено много работ но определению условий предотвращения образования гидратов [V. 5, V. 21,
V. 34, V. 35, V. 43, V. 91].
Вещества, растворимые в воде, препятствуют или задерживают гидратообразование, диполь водорода может разрушить структуру воды [V. 81] или раствор может снизить активность воды [V. 43]. Аммиак препятствует образованию структуры гидратов, соли (такие, как хлористый натрий) снижают активность воды.
I S
S'S
|
ГП | ||||
| /S' 2, | ||||
| / } | А | |||
|
'У | ||||
| Л? | У |
S 10
Температура, °c
IS
Рис. V. 51. Влияние растворения некоторых веществ на условия гидратообразаван'ия.
7_ю %-ный аммиак; 2— 10%-ный метанол; 3— 10%-ный NaCl;
4—10%-ный этанол или 10%-ный СаС12; 5 —чистая вода.
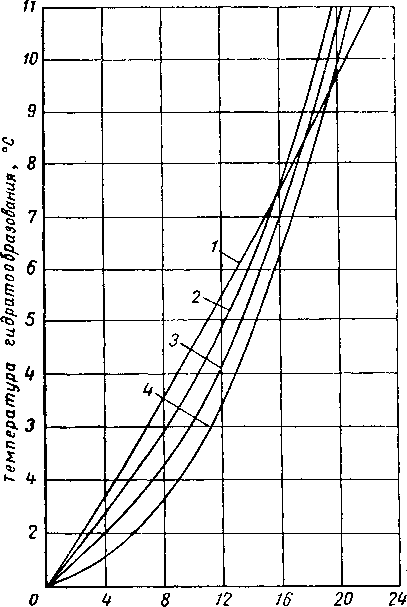
Количество ингибитора, % вес.
Рис. V. 52. Снижение температуры образования гидратов .различными ингибиторами.
1 — метанол на природный газ удельного весз 0,03 (V. 21); 2—NaCl на газ удельного веса 0.G8 (V. 43); 3 — СаС12 на газ удельного веса 0,63 (V.21);
4 — NaCl на газ удельного веса 0,555 (метан) [V. 43]
Изменение условий гидратообразования природных газов, находящихся в равновесии с 10%-ными весовыми водными растворами некоторых ингибиторов, показано на рис. V. 51. Эффективность применения спиртов для предотвращения образования гидратов зависит от степени их летучести в следующей последовательности: метанол, этанол, затем изопропанол.
Влияние концентрации различных растворителей на температуру гидратообразования природного газа показано на рис. V. 52. Концентрация показана как фактическая концентрация жидкости в равновесии с природным газом. Влияние NaCl на пропановый гидрат показано на рис. V. 53. Общее количество летучего ингибитора, требуемое для предупреждения гидратообразования, состоит из ингибитора, насыщающего жидкую и газовую фазы [V. 34].
Для нелетучих ингибиторов можно подсчитать влияние концентрации раствора на степень понижения температуры гидратообразования [V. 43].
Ди- и триэтиленгликоль используются как ингибиторы гидратообразования, кроме того, они применяются для осушки природных газов.
На рис. V. 54 приведены кривые, показывающие влияние концентрации раствора диэгиленгликоля на процесс гидратообразования природного газа удельного веса 0,595 [V. 73]. Присутствие нефти и раствора гликоля еще сильнее задерживает процесс образования гидратов, но при этом общее снижение меньше, чем
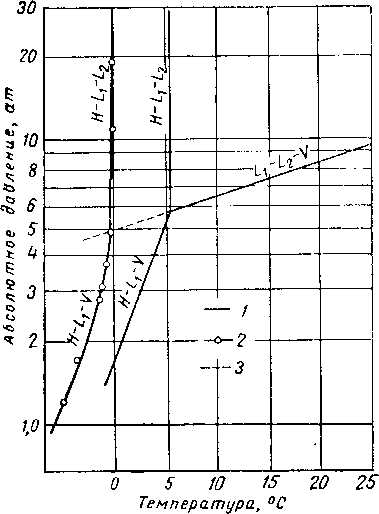
Раю. V. 53. Влияние NaCl на образование гидратов пропана [V. 43].
1 — пропан — вода; 2— пропан — 10 % (вес.) NaCl;
3 — кривая точек четырехфазного состояния;
Я — гидрат; /.i — вода; — жидкий углеводород; V — паровая фаза.
суммарное, когда оба раствора применяются отдельно друг от друга [V. 73J.
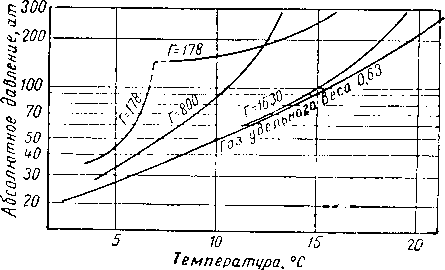
Условия образования гидратов для газа удельного веса 0,595, находящегося в равновесии с соляным раствором, в присутствии различного количества сепарированной нефти удельного веса 0,7935 рассмотрены в работах [V. 73, V. 74].
На рис. V. 55 показано влияние газового фактора на условия образования гидратов.
Хранение газа в гидратах было рассмотрено Миллером и Стронгом (Miller and Strong) [V. 54] и Пэрентом (Parent) [V. 58]. Из рис. V. 36 видим, что в виде гидратов предпочтительнее хранить пропан, а не метан.
Рис. V. 55. Влияние газового фактора на условия гид ратообр азов ания.
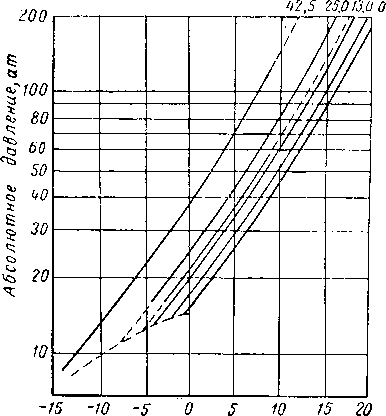
Рис. V. 54. Влияние диэтилеегликоля на условия образования гидратов [V. 73, V. 741 -